Ацилоины или α-гидроксикетоны [1] представляют собой класс органических соединений, которые все имеют гидроксигруппу, смежную с кетонной группой . Названный ацилоин является производным от того факта, что формально они получены в результате восстановительного связывания карбоксильных ацильных групп. [2]
Синтез [ править ]
Существуют классические органические реакции для синтеза ацилоинов.
- Ацилоины конденсация является восстановительной связью эфиров
- Бензоина конденсации является реакцией конденсации между альдегидов , катализируемых с помощью нуклеофильного
- Окисление карбонилов возможно молекулярным кислородом, но не селективно.
- Лучшей альтернативой является окисление соответствующих силиленольных эфиров m CPBA при окислении Руботтома.
- MoOPH окисление карбонилов представляет собой систему с пероксидом молибдена , пиридином и гексаметилфосфорамидом .
Окисление енолятов сульфонилоксазиридинами [ править ]
Еноляты могут окисляться сульфонилоксазиридинами . [3] [4] Енолят реагирует путем нуклеофильного замещения электронно-дефицитного кислорода оксазиридинового кольца.
Этот тип реакции расширен до асимметричного синтеза за счет использования хиральных оксазиридинов, полученных из камфоры (камфорсульфонилоксазиридина). Каждый изомер дает исключительный доступ к одному из двух возможных энантиомеров . Эта модификация применяется в полном синтезе таксола Холтона .
При енолятном окислении циклопентаенона, описанном ниже [5], любым энантиомером камфоры получается транс- изомер, потому что доступ для гидроксильной группы в цис- положении ограничен. Использование стандартного оксазиридина не привело к образованию ацилоина.
Реакции [ править ]
- Восстановление ацилоинов дает диолы .
- Окисление ацилоинов дает дионы .
- α-гидроксикетоны дают положительный результат теста Толленса и Фелинга .
- Некоторые ацилоины перегруппировываются с перестановкой позиций под действием основания в преобразовании Лобри – де Брюйна – ван Экенштейна.
- Похожей реакцией является так называемое аминирование Фойгта [6], при котором ацилоин реагирует с первичным амином и пентоксидом фосфора с образованием α-кетоамина: [7]
- Синтез индола , [8] сравните Bischler-Möhlau
См. Также [ править ]
- Гликолевый , связанная молекула эквивалентно ацилоины с обеими R групп , как водород (и , таким образом альдегид не кетон)
Ссылки [ править ]
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) « acyloins ». DOI : 10,1351 / goldbook.A00126
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) « acyloins ». DOI : 10,1351 / goldbook.A00126
- ^ Дэвис, Франклин А .; Вишвакарма, Лал Ч .; Биллмерс, Джоанн Дж .; Финн, Джон (1984). «Синтез α-гидроксикарбонильных соединений (ацилоинов): прямое окисление енолятов с использованием 2-сульфонилоксазиридинов». J. Org. Chem. 49 (17): 3241–3243. DOI : 10.1021 / jo00191a048 .
- ^ Дэвис, FA; Haque, MS; Улатовский, Т.Г .; Тоусон, JC (1986). «Асимметричное окисление енолятов сложного эфира и амида с использованием новых (камфорилсульфонил) оксазиридинов». J. Org. Chem. 51 (12): 2402. DOI : 10.1021 / jo00362a053 .
- ^ а б Hughes, Chambers C .; Миллер, Обри К .; Траунер, Дирк (2005). «Электрохимический подход к гуанакастепенам» (PDF) . Орг. Lett. 7 (16): 3425–3428. DOI : 10.1021 / ol047387l . PMID 16048308 . Архивировано из оригинального (PDF) 4 сентября 2006 года.
- ^ von Meyer, E .; Войт, Карл (1886). "Ueber die Einwirkung von primären aromatischen Aminen auf Benzoïn" [О влиянии первичных ароматических аминов на бензоин]. J. Prakt. Chem. (на немецком). 34 (1): 1-27. DOI : 10.1002 / prac.18860340101 .
- ^ Лоуренс, Стивен А. (2004). Амины: синтез, свойства и применение . Издательство Кембриджского университета . ISBN 978-0-521-78284-5.
- ^ Рот, Лепке (1972). «Синтез производных индола и карбазола на основе α-гидроксикетоненов и ароматических аминов» [Синтез производных индола и карбазола из α-гидроксикетонов и ароматических аминов]. Archiv der Pharmazie (на немецком языке). 305 (3): 159–171. DOI : 10.1002 / ardp.19723050302 . PMID 5048240 . S2CID 84990819 .

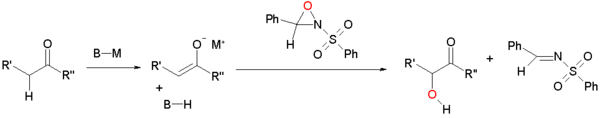

![Пример окисления енолята [5]](http://upload.wikimedia.org/wikipedia/commons/thumb/0/02/Acyloin_example_Hughes.png/500px-Acyloin_example_Hughes.png)