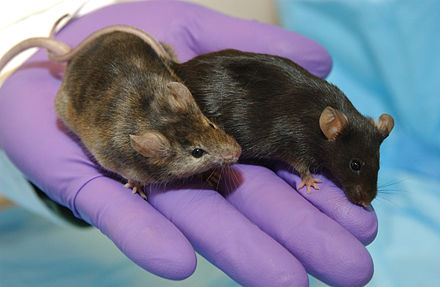
Нокаут ген (сокращенно: КО ) представляет собой генетический метод , в котором один из организма «ы гены производятся в нерабочем состоянии („нокаут“из организма). Однако KO может также относиться к гену, который отключен, или к организму, который несет этот ген. Нокаутные организмы или просто нокауты используются для изучения функции генов, обычно путем исследования эффекта потери генов. Исследователи делают выводы из разницы между организмом с нокаутом и нормальными людьми.
Техника нокаутов - это, по сути, противоположность нокауту гена . Одновременный нокаут двух генов в организме известен как двойной нокаут ( ДКО ). Точно так же термины тройной нокаут ( TKO ) и четверной нокаут ( QKO ) используются для описания трех или четырех генов с нокаутом, соответственно. Однако необходимо различать гетерозиготные и гомозиготные КО. В первом из двух копий гена ( аллелей ) выбивается только одна , во втором - обе.
Методы [ править ]
Нокауты достигаются с помощью различных техник. Первоначально были идентифицированы встречающиеся в природе мутации, а затем необходимо было установить потерю или инактивацию генов с помощью секвенирования ДНК или других методов. [1]
Гомологичная рекомбинация [ править ]
Традиционно гомологичная рекомбинация была основным методом, вызывающим нокаут гена. Этот метод включает создание конструкции ДНК, содержащей желаемую мутацию. Для целей нокаута это обычно включает маркер устойчивости к лекарственному средству вместо желаемого гена нокаута. [2] Конструкция также будет содержать минимум 2 килобайт гомологии с целевой последовательностью. [2] Конструкция может быть доставлена к стволовым клеткам посредством микроинъекции или электропорации . [2]Затем этот метод полагается на собственные механизмы восстановления клетки для рекомбинации конструкции ДНК в существующую ДНК. Это приводит к изменению последовательности гена, и в большинстве случаев ген будет транслироваться в нефункциональный белок , если он вообще транслируется. Однако это неэффективный процесс, так как на гомологичную рекомбинацию приходится только от 10 -2 до 10 -3 интеграций ДНК. [2] [3] Часто маркер выбора лекарства на конструкции используется для отбора клеток, в которых произошло событие рекомбинации.

Эти стволовые клетки, в которых сейчас отсутствует ген, можно использовать in vivo , например, на мышах, вставляя их в ранние эмбрионы. [2] Если полученная химерная мышь содержала генетические изменения в их зародышевой линии, это могло быть передано потомству. [2]
В диплоидных организмах, которые содержат два аллеля для большинства генов и могут также содержать несколько родственных генов, которые сотрудничают в одной и той же роли, выполняются дополнительные раунды трансформации и отбора до тех пор, пока не будет выбит каждый целевой ген. Для получения гомозиготных животных с нокаутом может потребоваться селективное разведение .
Нуклеазы, специфичные для сайта [ править ]
В настоящее время используются три метода, которые включают точное нацеливание на последовательность ДНК с целью введения двухцепочечного разрыва. Как только это происходит, механизмы репарации клетки будут пытаться восстановить этот двухцепочечный разрыв, часто посредством негомологичного соединения концов (NHEJ), которое включает прямое лигирование двух отрезанных концов вместе. [3] Это может быть сделано несовершенно, поэтому иногда возникают вставки или делеции пар оснований, которые вызывают мутации со сдвигом рамки считывания . Эти мутации могут сделать ген, в котором они происходят, нефункциональным, что приведет к нокауту этого гена. Этот процесс более эффективен, чем гомологичная рекомбинация, и поэтому его легче использовать для создания двуаллельных нокаутов. [3]
Цинковые пальцы [ править ]
Нуклеазы «цинковые пальцы» состоят из ДНК-связывающих доменов, которые могут точно нацеливаться на последовательность ДНК. [3] Каждый цинковый палец может распознавать кодоны желаемой последовательности ДНК и, следовательно, может быть модульно собран для связывания с определенной последовательностью. [5] Эти связывающие домены связаны с рестрикционной эндонуклеазой, которая может вызывать двухцепочечный разрыв (DSB) в ДНК. [3] Процессы восстановления могут привести к мутациям, нарушающим функциональность гена.
ТАЛЕНС [ править ]
Эффекторные нуклеазы, подобные активатору транскрипции ( TALEN ), также содержат ДНК-связывающий домен и нуклеазу, которая может расщеплять ДНК. [6] ДНК-связывающая область состоит из аминокислотных повторов, каждый из которых распознает одну пару оснований желаемой целевой последовательности ДНК. [5] Если это расщепление нацелено на кодирующую область гена, а репарация, опосредованная NHEJ, вводит вставки и делеции, часто возникает мутация сдвига рамки считывания, таким образом нарушая функцию гена. [6]
CRISPR / Cas9 [ править ]
Кластерные короткие палиндромные повторы с регулярными интервалами ( CRISPR ) / Cas9 - это метод редактирования генома, который содержит направляющую РНК в комплексе с белком Cas9 . [5] Направляющая РНК может быть сконструирована так, чтобы соответствовать желаемой последовательности ДНК посредством простого комплементарного спаривания оснований, в отличие от трудоемкой сборки конструкций, необходимой для «цинковых пальцев» или TALEN. [7] Связанный Cas9 вызывает двухцепочечный разрыв ДНК. [5] Следуя тому же принципу, что и «цинковые пальцы» и TALEN, попытки восстановить эти двухцепочечные разрывы часто приводят к мутациям сдвига рамки считывания, что приводит к нефункциональному гену. [5]
Knockin [ править ]
Нокаут гена похож на нокаут гена, но он заменяет ген другим вместо его удаления.
Типы [ править ]
Условные нокауты [ править ]
Условный нокаут гена делает возможным удаление гена в ткани в зависимости от времени. Это требуется вместо нокаута гена, если нулевая мутация приведет к гибели эмбриона . [8] Это делается путем введения коротких последовательностей, называемых сайтами loxP, вокруг гена. Эти последовательности будут введены в зародышевую линию посредством того же механизма, что и нокаут. Затем эту зародышевую линию можно скрестить с другой зародышевой линией, содержащей Cre-рекомбиназу, которая представляет собой вирусный фермент, который может распознавать эти последовательности, рекомбинировать их и удаляет ген, фланкированный этими сайтами.
Используйте [ редактировать ]
Нокауты в основном используются для понимания роли определенного гена или участка ДНК путем сравнения нокаутного организма с диким типом с аналогичным генетическим фоном.
Нокаут организмы также используются в качестве скрининга инструментов разработки лекарственных средств , для решения конкретного биологических процессов или недостатков с использованием конкретного нокаута или понять механизм действия в виде препарата с использованием библиотеки нокатирующих организмов , охватывающей весь геном , например как у Saccharomyces cerevisiae . [9]
См. Также [ править ]
- Существенный ген
- Джин нокдаун
- Условный нокаут гена
- Зародышевый
- Подавление гена
- Планируемое вымирание
- Рекомбинирование
- Миостатин
- Бельгийский синий
Ссылки [ править ]
- ^ Гриффитс AJ, Миллер Дж, Сузуки ДТ, Левонтин туалет, Гелбарт WM (2000). Введение в генетический анализ (7-е изд.). Нью-Йорк: WH Freeman. ISBN 978-0-7167-3771-1.
- ^ a b c d e f Холл, Брэдфорд; Лимае, Адвайт; Кулкарни, Ашок Б. (01.09.2009). Обзор: Поколение мышей с нокаутом генов . Текущие протоколы в клеточной биологии . 44 . Вили-Блэквелл. С. Раздел 19.12 19.12.1–17. DOI : 10.1002 / 0471143030.cb1912s44 . ISBN 978-0471143031. PMC 2782548 . PMID 19731224 .
- ^ a b c d e Сантьяго, Иоланда; Чан, Эдмонд; Лю, Пэй-Ци; Орландо, Сальваторе; Чжан, Линь; Урнов, Федор Д .; Холмс, Майкл С .; Гущин Дмитрий; Уэйт, Адам (2008-04-15). «Целенаправленный нокаут гена в клетках млекопитающих с использованием сконструированных нуклеаз цинкового пальца» . Труды Национальной академии наук . 105 (15): 5809–5814. DOI : 10.1073 / pnas.0800940105 . ISSN 0027-8424 . PMC 2299223 . PMID 18359850 .
- ^ Egener T, Granado J, Guitton M, Hohe A, Holtorf H, Lucht JM и др. (2002). «Высокая частота фенотипических отклонений у растений Physcomitrella patens, трансформированных библиотекой нарушения генов» . BMC Plant Biology . 2 (1): 6. DOI : 10,1186 / 1471-2229-2-6 . PMC 117800 . PMID 12123528 .
- ^ a b c d e Гай, Томас; Герсбах, Чарльз А .; Барбас, Карлос Ф. (2013). «Методы на основе ZFN, TALEN и CRISPR / Cas для геномной инженерии» . Тенденции в биотехнологии . 31 (7): 397–405. DOI : 10.1016 / j.tibtech.2013.04.004 . PMC 3694601 . PMID 23664777 .
- ^ а б Джунг, Дж. Кейт; Сандер, Джеффри Д. (январь 2013 г.). «TALENs: широко применяемая технология для целевого редактирования генома» . Обзоры природы Молекулярная клеточная биология . 14 (1): 49–55. DOI : 10.1038 / nrm3486 . ISSN 1471-0080 . PMC 3547402 . PMID 23169466 .
- ^ Ни, Вэй; Цяо, Цзюнь; Ху, Шэнвэй; Чжао, Синься; Реговский, Миша; Ян, Мин; Полежаева Ирина А .; Чен, Чуанфу (04.09.2014). «Эффективный нокаут генов у коз с использованием системы CRISPR / Cas9» . PLOS ONE . 9 (9): e106718. DOI : 10.1371 / journal.pone.0106718 . ISSN 1932-6203 . PMC 4154755 . PMID 25188313 .
- ^ Ле, Юньчжэн; Зауэр, Брайан (2001-03-01). «Условный нокаут гена с использованием рекомбиназы cre». Молекулярная биотехнология . 17 (3): 269–275. DOI : 10.1385 / MB: 17: 3: 269 . ISSN 1073-6085 . PMID 11434315 .
- ^ "YeastDeletionWebPages" . Проверено 21 февраля 2017 года .
Внешние ссылки [ править ]
- Схема целевой замены гена
- Frontiers in Bioscience Gene Knockout Database (доступно только в архиве)
- Международный консорциум Knockout Mouse
- Репозиторий КОМП