Карбоксимидаты (или более общие имидаты ) представляют собой органические соединения, которые можно рассматривать как сложные эфиры, образованные между карбоксимидной кислотой (RC (= NR ') OH) и спиртом , с общей формулой RC (= NR') OR ».
Они также известны как иминоэфиры , поскольку они напоминают имины (> C = N-) с атомом кислорода, связанным с атомом углерода.
Синтез [ править ]
Имидаты могут быть получены несколькими способами синтеза [1], но, как правило, они образуются по реакции Пиннера . Это происходит через катализируемую кислотой атаку нитрилов спиртами.

Полученные таким образом имидаты образуются в виде их гидрохлоридных солей, которые иногда называют солями Пиннера. Carboximidates также образуются в качестве промежуточных продуктов в перегруппировке Mumm и Овермана перегруппировки .
Имидатные / амидатные анионы [ править ]
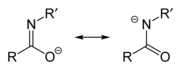
Амидат / имидат анион образуются при депротонировании из качестве амида или imidic кислоты . Поскольку амиды и имидовые кислоты являются таутомерами , они образуют один и тот же анион при депротонировании. Таким образом, два имени являются синонимами, описывающими один и тот же анион, хотя, возможно, имидат относится к вкладчику резонанса слева, а амидат относится к участнику резонанса справа. Однако их различают, когда они действуют как лиганды для переходных металлов, причем O- связанные частицы называют имидатами, а N- связанные частицы - амидатами . Их можно рассматривать как азазамещенные аналоги енолятов с формулой RN = C (O- ) Р.
Реакции [ править ]
Карбоксимидаты являются хорошими электрофилами и подвергаются ряду реакций присоединения; с алифатическими имидатами, как правило, реагируют быстрее, чем ароматические имидаты. [1] Их можно гидролизовать с образованием сложных эфиров и аналогичным способом реагировать с аминами (включая аммиак) с образованием амидинов . Алифатические имидаты реагируют с избытком спирта при кислотном катализе с образованием ортоэфиров RC (OR) 3 , ароматические имидаты также могут быть преобразованы, но гораздо менее легко.
Перестановка Чепмена [ править ]
Названный в честь Артура Уильяма Чепмена , который первым его описал [3], это термическое превращение арил-N-арилбензимидатов в соответствующие амиды. [4] Она концептуально аналогична перегруппировке Ньюмана – Кварта .
Как защитная группа [ править ]
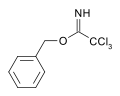
Карбоксимидаты могут действовать как защитная группа для спиртов. [5] Например, катализируемая основанием реакция бензилового спирта на трихлорацетонитрил дает трихлорацетимидат . Этот вид обладает ортогональной стабильностью к ацетатной и TBS- защите и может расщепляться кислотным гидролизом. [6]
См. Также [ править ]
- Амидины
- Сложные эфиры
- Оксазолин - соответствующий 5-членный гетероцикл
Ссылки [ править ]
- ^ a b Роджер, Роберт; Нилсон, Дуглас Г. (1961). «Химия имидатов». Химические обзоры . 61 (2): 179–211. DOI : 10.1021 / cr60210a003 .
- ^ BP Mundy, MG Ellerd, FG Favaloro: Назовите реакции и реагенты в органическом синтезе , 2. Auflage, Wiley-Interscience, Hoboken, NJ 2005 , ISBN 978-0-471-22854-7 , S. 516.
- ^ Чепмен, Артур Уильям (1925). "CCLXIX. - Иминоариловые эфиры. Часть III. Молекулярная перегруппировка N-фенилбензимнофенилового эфира". J. Chem. Soc., Trans . 127 : 1992–1998. DOI : 10.1039 / CT9252701992 .
- ^ Шуленберг, JW; Арчер, С. (1965). «Перестановка Чепмена». Орг. Реагировать. 14 : 1–51. DOI : 10.1002 / 0471264180.or014.01 . ISBN 0471264180.
- ^ Wuts, Питер GM; Грин, Теодора В. (2006). Защитные группы в органическом синтезе (4-е изд.). Хобокен, Нью-Джерси: ВИЛИ. п. 244. ISBN 978-0-471-69754-1.
- ^ Ю, Бяо; Ю, Хай; Хуэй Юнчжэн; Хан, Сювэнь (июнь 1999 г.). «Трихлорацетимидат как эффективная защитная группа для спиртов». Synlett . 1999 (6): 753–755. DOI : 10,1055 / с-1999-2736 .