Было предложено разделить эту статью на статьи, озаглавленные « Алкоксид переходных металлов» и « Алкоксиды щелочных металлов» . ( Обсудить ) ( сентябрь 2020 г. ) |
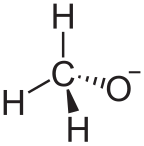
Алкоксид представляет собой сопр женного основания из спирта и , следовательно , состоит из органической группы , связанной с отрицательно заряженным кислородом атома. Они записываются как RO - , где R - органический заместитель. Алкоксиды являются сильными основаниями и, когда R не является объемным, хорошими нуклеофилами и хорошими лигандами. Алкоксиды, хотя обычно нестабильны в протонных растворителях, таких как вода, широко используются в качестве промежуточных продуктов в различных реакциях, включая синтез эфира Вильямсона . [1] [2] Алкоксиды переходных металлов широко используются для покрытий и в качестве катализаторов .[3] [4]
Еноляты представляют собой ненасыщенные алкоксиды, полученные депротонированием связи CH, соседней с кетоном или альдегидом . Нуклеофильный центр простых алкоксидов расположен на кислороде, тогда как нуклеофильный центр на енолятах делокализован как на углеродных, так и на кислородных сайтах. Инолаты также представляют собой ненасыщенные алкоксиды, полученные из ацетиленовых спиртов.
Феноксиды являются близкими родственниками алкоксидов, в которых алкильная группа заменена производным бензола . Фенол более кислый, чем обычный спирт; таким образом, феноксиды соответственно менее основны и менее нуклеофильны, чем алкоксиды. Однако с ними часто легче обращаться, и они дают более кристаллические производные, чем производные алкоксидов.
Структура [ править ]
Алкоксиды щелочных металлов часто представляют собой олигомерные или полимерные соединения, особенно когда группа R мала (Me, Et). [3] Анион алкоксида является хорошим мостиковым лигандом , поэтому многие алкоксиды имеют связи M 2 O или M 3 O. В растворе производные щелочного металла демонстрируют сильное ионное образование пар, как и ожидалось для производного щелочного металла сильноосновного аниона.

Подготовка [ править ]
По реакциям метатезиса [ править ]
Многие алкоксиды получают реакциями солеобразования из хлорида металла и алкоксида натрия:
- n NaOR + MCl n → M (OR) n + n NaCl
Таким реакциям способствует энергия решетки NaCl, а очистка алкоксида продукта упрощается тем фактом, что NaCl нерастворим в обычных органических растворителях.
Для некоторых электрофильных галогенидов металлов преобразование в алкоксид не требует основания. Тетрахлорид титана реагирует со спиртами с образованием соответствующих тетраалкоксидов с выделением хлористого водорода :
- TiCl 4 + 4 (CH 3 ) 2 CHOH → Ti (OCH (CH 3 ) 2 ) 4 + 4 HCl
Реакцию можно ускорить добавлением основания, такого как третичный амин . Вместо титана можно использовать галогениды многих других металлов и основных групп, например SiCl 4 , ZrCl 4 и PCl 3 .
От восстановления металлов [ править ]
Алкоксиды можно получить несколькими способами, начиная с алкоголя . Металлы с высокой степенью восстановления непосредственно реагируют со спиртами с образованием соответствующего алкоголята металла. Спирт служит кислотой , а водород образуется как побочный продукт. Классический случай - метоксид натрия, полученный добавлением металлического натрия к метанолу :
- 2 CH 3 OH + 2 Na → 2 CH 3 ONa + H 2
Вместо натрия можно использовать другие щелочные металлы , а вместо метанола можно использовать большинство спиртов. Другая подобная реакция происходит, когда спирт реагирует с гидридом металла, таким как NaH. Гидрид металла удаляет атом водорода из гидроксильной группы и образует отрицательно заряженный алкоксид-ион.
Электрохимическими процессами [ править ]
Многие алкоксиды можно получить анодным растворением соответствующих металлов в безводных спиртах в присутствии электропроводящей добавки. Металлы могут быть Co , Ga , Ge , Hf , Fe , Ni , Nb , Mo , La , Re , Sc , Si , Ti , Ta , W , Y , Zr и т. Д. Проводящей добавкой может быть хлорид лития., галогенид четвертичного аммония или другие. Некоторые примеры алкоксидов металлов, полученных этим методом: Ti (OCH (CH 3 ) 2 ) 4 , Nb 2 (OCH 3 ) 10 , Ta 2 (OCH 3 ) 10 , [MoO (OCH 3 ) 4 ] 2 , Re 2 O 3 (OCH 3 ) 6 , Re 4 O 6 (OCH 3 ) 12 и Re 4 O 6 (OCH (CH 3 ) 2 ) 10.
Свойства [ править ]
Реакции с алкилгалогенидами [ править ]
Ион алкоксида может реагировать с первичным алкилгалогенидом в реакции SN 2 с образованием эфира посредством синтеза эфира Вильямсона.
Гидролиз и переэтерификация [ править ]
Алкоксиды металлов гидролизуются водой в соответствии со следующим уравнением: [6]
- 2 L n MOR + H 2 O → [L n M] 2 O + 2 ROH
где R - органический заместитель, а L - неуказанный лиганд (часто алкоксид) Хорошо изученным случаем является необратимый гидролиз этоксида титана:
- 1 / n [Ti (OCH 2 CH 3 ) 4 ] n + 2 H 2 O → TiO 2 + 4 HOCH 2 CH 3
Контролируя стехиометрию и стерические свойства алкоксида, такие реакции могут быть остановлены, приводя к оксиалкоксидам металлов, которые обычно представляют собой олигонуклеарные комплексы. Вместо воды можно использовать другие спирты. Таким образом, один алкоксид может быть преобразован в другой, и этот процесс правильно называется алкоголизом (к сожалению, существует проблема терминологической путаницы с переэтерификацией, другим процессом - см. Ниже). Положение равновесия можно регулировать кислотностью спирта; например, фенолы обычно реагируют с алкоксидами с выделением спиртов, давая соответствующий феноксид. Проще говоря, алкоголиз можно контролировать выборочноиспарение более летучих компонентов. Таким образом, этоксиды могут быть преобразованы в бутоксиды, поскольку этанол (точка кипения 78 ° C) более летуч, чем бутанол (точка кипения 118 ° C).
В процессе переэтерификации алкоксиды металлов реагируют со сложными эфирами, вызывая обмен алкильными группами между алкоксидом металла и сложным эфиром. При рассмотрении комплекса алкоксида металла результат такой же, как и при алкоголизе, а именно замена лигандов алкоксида, но в то же время изменяются алкильные группы сложного эфира, что также может быть основной целью реакции. Для этой цели обычно используется метоксид натрия, реакция, которая имеет отношение к производству « биодизеля ».
Образование оксоалкоксидов [ править ]
Многие соединения алкоксидов металлов также имеют оксо- лигандов . Оксолиганды обычно возникают в результате гидролиза, часто случайно, и в результате отщепления эфира:
- 2 L n MOR → [L n M] 2 O + R 2 O
Кроме того, алкоксиды металлов с низкой валентностью подвержены окислению воздухом.
Образование полиядерных и гетерометаллических производных [ править ]
Алкоксиды переходных металлов являются полиядерными, т. Е. Содержат более одного металла. Алкоксиды - это стерически нетребовательные и очень основные лиганды, которые склонны связывать металлы.
При изоморфном замещении атомов металлов, близких по свойствам, образуются кристаллические комплексы переменного состава. Соотношение металлов в таких соединениях может варьироваться в широком диапазоне. Например, замена молибдена и вольфрама на рений в комплексах Re 4 O 6− y (OCH 3 ) 12+ y позволила получить комплексы Re 4− x Mo x O 6− y (OCH 3 ) 12+ y в диапазон 0 ≤ x ≤ 2,82 и Re 4− x W xO 6− y (OCH 3 ) 12+ y в диапазоне 0 ≤ x ≤ 2.
Термическая стабильность [ править ]
Многие алкоксиды металлов термически разлагаются в интервале ~ 100–300 ° C. В зависимости от условий процесса этот термолиз может давать наноразмерныепорошки оксидной или металлической фаз. Этот подход лежит в основе процессов изготовления функциональных материалов, предназначенных для авиастроения, космоса, электронной области и химической промышленности: индивидуальных оксидов, их твердых растворов, сложных оксидов, порошков металлов и сплавов, активных к спеканию. Также изучено разложение смесей моно- и гетерометаллических производных алкоксидов. Этот метод представляет собой перспективный подход, обладающий преимуществом возможности получения функциональных материалов с повышенной фазовой и химической однородностью и контролируемым размером зерна (включая получение наноразмерных материалов) при относительно низкой температуре (менее 500-900 ° C) по сравнению с обычные методы.
Иллюстративные алкоксиды [ править ]
| имя | молекулярная формула | комментарий |
|---|---|---|
| Изопропоксид титана | Ti (O i Pr) 4 | мономерный из-за стерического объема, используется в органическом синтезе |
| Этоксид титана | Ti 4 (OEt) 16 | для золь-гель обработки оксидов Ti |
| Этоксид циркония | Zr 4 (OEt) 16 | для золь-гель обработки оксидов Zr |
| Тетраэтилортосиликат | Si (OEt) 4 | для золь-гель обработки оксидов Si; Si (OMe) 4 следует избегать из соображений безопасности. |
| Изопропоксид алюминия | Al 4 (O i Pr) 12 | реагент для восстановления Меервейна – Понндорфа – Верлея |
| Изопропоксид ванадила | ВО (О и Пр) 3 | предшественник катализаторов |
| Этоксид ниобия | Nb 2 (OEt) 10 | для золь-гель обработки оксидов Nb |
| Этоксид тантала | Та 2 (OEt) 10 | для золь-гель обработки оксидов Ta |
| Трет- бутоксид калия , | К 4 (О т Бу) 4 | основной реагент для реакций органического отщепления |
Дальнейшее чтение [ править ]
- Турова, Наталия Ю. (2004). «Оксоалкоксиды металлов. Синтез, свойства и строение». Российские химические обозрения . 73 (11): 1041–1064. Bibcode : 2004RuCRv..73.1041T . DOI : 10,1070 / RC2004v073n11ABEH000855 .
Ссылки [ править ]
- ^ Уильямсон, Александр (1850). «Теория террификации» . Фил. Mag. 37 (251): 350–356. DOI : 10.1080 / 14786445008646627 . ( Ссылка на отрывок. )
- ^ Бойд, Роберт Нейлсон; Моррисон, Роберт Торнтон (1992). Органическая химия (6-е изд.). Энглвуд Клиффс, Нью-Джерси: Prentice Hall . С. 241–242. ISBN 9780136436690.
- ^ а б Брэдли, Дон К .; Mehrotra, Ram C .; Ротвелл, Ян П .; Сингх, А. (2001). Алкоксо- и арилоксопроизводные металлов . Сан-Диего: Academic Press . ISBN 978-0-08-048832-5.
- ^ Турова, Наталия Юрьевна; Туревская, Евгения П .; Кесслер, Вадим Г .; Яновская, Мария Ивановна (2002). Химия алкоксидов металлов . Дордрехт: Kluwer Academic Publishers . ISBN 9780792375210.
- ^ Ункельбах, Кристиан; О'Ши, Донал Ф .; Штроманн, Карстен (2014). «Взгляды на металлирование бензола и толуола основанием Шлоссера: супербазовый кластер, включающий PhK, PhLi и t BuOLi». Энгью. Chem. Int. Эд. 53 (2): 553–556. DOI : 10.1002 / anie.201306884 . PMID 24273149 .
- ^ Ханаор, Дориан AH; Хирони, Илкай; Карачевцева, Инна; Триани, Джерри; Соррелл, Чарльз К. (2012). «Однофазные и смешанные порошки TiO 2, полученные избыточным гидролизом алкоголята титана» . Успехи прикладной керамики . 111 (3): 149–158. arXiv : 1410,8255 . DOI : 10.1179 / 1743676111Y.0000000059 . S2CID 98265180 .
- ^ Щеглов П.А.; Дробот, ДВ (2005). «Алкоксиды рения». Российский химический вестник . 54 (10): 2247–2258. DOI : 10.1007 / s11172-006-0106-5 . S2CID 195234048 .