| НАДФН-дегидрогеназа | ||||||||
|---|---|---|---|---|---|---|---|---|
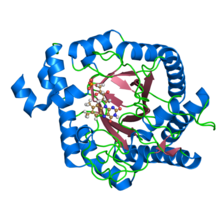 Рентгеновская структура ксенобиотической редуктазы А из Pseudomonas putida . Запись PDB 3l5l | ||||||||
| Идентификаторы | ||||||||
| ЕС нет. | 1.6.99.1 | |||||||
| № CAS | 9001-68-7 | |||||||
| Базы данных | ||||||||
| IntEnz | Просмотр IntEnz | |||||||
| БРЕНДА | BRENDA запись | |||||||
| ExPASy | Просмотр NiceZyme | |||||||
| КЕГГ | Запись в KEGG | |||||||
| MetaCyc | метаболический путь | |||||||
| ПРИАМ | профиль | |||||||
| Структуры PDB | RCSB PDB PDBe PDBsum | |||||||
| Генная онтология | Amigo / QuickGO | |||||||
| ||||||||
В энзимологии , A НАДФН - дегидрогеназа ( EC 1.6.99.1 ) представляет собой фермент , который катализирует в химическую реакцию
- НАДФН + Н + + акцептор НАДФ + + восстановленный акцептор
Три субстрата этого фермента - НАДФН , Н + и акцептор , а два его продукта - НАДФ + и восстановленный акцептор .
Этот фермент принадлежит к семейству оксидоредуктаз , в частности тех, которые действуют на НАДН или НАДФН с другими акцепторами. Систематическое название данного фермента класса NADPH: акцептор оксидоредуктаз . Другие имена в общем пользовании , включают NADPH2 диафораза , НАДФН диафораза , OYE , диафораза , dihydronicotinamide - аденин - динуклеотид фосфат дегидрогеназы , НАДФН-дегидрогеназа , НАДФН-диафораза , NADPH2-дегидрогеназы , старый желтая фермент , восстановленный никотинамидадениндинуклеотид фосфатдегидрогеназы ,TPNH-дегидрогеназа , TPNH-диафораза , трифосфопиридиндиафораза , трифосфопиридиннуклеотид-диафораза , NADPH2-дегидрогеназа и NADPH: (акцепторная) оксидоредуктаза . Он имеет 2 кофактора : FAD и FMN .
Ссылки [ править ]
- Boyer, PD, Lardy, H. и Myrback, K. (Eds.), The Enzymes, 2 ed., Vol. 7, Academic Press, Нью-Йорк, 1963, стр. 477-494.
- АВРОН М., ЯГЕНДОРФ А.Т. (1957). «Некоторые дальнейшие исследования диафоразы TPNH хлоропластов». Arch. Биохим. Биофиз . 72 (1): 17–24. DOI : 10.1016 / 0003-9861 (57) 90169-8 . PMID 13471057 .
- Ягендорф А.Т. (1963). «Хлоропластная диафораза ТПНГ». Методы Энзимол . 6 : 430–434. DOI : 10.1016 / 0076-6879 (63) 06200-5 .
- Теорелл H (1935). «Das gelbe Oxydationsferment». Биохим. Z . 278 : 263–290.
- Теорелл H; Акессон А (1956). «Молекулярный вес и содержание ФМН кристаллического« старого желтого фермента » ». Arch. Биохим. Биофиз . 65 (1): 439–448. DOI : 10.1016 / 0003-9861 (56) 90204-1 . PMID 13373435 .
- Уолтер Ф. Борон; Эмиль Л. Боулпаэп (2008). Медицинская физиология .
[1] [2]
- ^ Дэвис EM, Рингер KL, McConkey Me, Croteay R (2005) Ферментная ментолдегидрогеназа. http://mousecyc.jax.org:1555/META/NEW-IMAGE?type=ENZYME-IN-RXNDISPLAY&object=MONOMER-6721&detail-level=3 (Ссылки на внешний сайт.)
- ^ (1986). Удаление ферредоксина: НАДФН + оксидоредуктаза с тилакоидных мембран, повторное связывание с истощенными мембранами и идентификация сайта связывания. Журнал биологической химии. https://www.researchgate.net/publication
