Оловоорганические соединения или винилстаннаны являются химическими соединениями на основе олова с углеводородными заместителями. Химия оловоорганических соединений является частью более широкой области металлоорганической химии . Первым оловоорганическим соединением был дииодид диэтилолова ((C 2 H 5 ) 2 SnI 2 ), открытый Эдвардом Франкландом в 1849 году. [1] Эта область быстро росла в 1900-х годах, особенно после открытия реактивов Гриньяра., которые полезны для получения связей Sn-C. Область по-прежнему богата множеством применений в промышленности и продолжающейся деятельностью в исследовательской лаборатории. [2]
Структура [ править ]
Оловоорганические соединения обычно классифицируют по степени окисления. Соединения олова (IV) гораздо более распространены и полезны.
Органические производные олова (IV) [ править ]
Тетраорганопроизводные всегда являются тетраэдрическими. Соединения типа SnRR'R''R '' 'были разделены на индивидуальные энантиомеры. [3]
Галогениды олова олова [ править ]
Оловоорганические хлориды имеют формулу R 4− n SnCl n для значений n до 3. Бромиды, йодиды и фториды также известны, но менее важны. Эти соединения известны многими R-группами. Они всегда четырехгранные. Три- и дигалогениды образуют аддукты с хорошими основаниями Льюиса, такими как пиридин . Фториды имеют тенденцию к объединению, так что дифторид диметилолова образует пластинчатые полимеры. Галогениды ди- и особенно триорганотина, например хлорид трибутилолова , проявляют токсичность, приближающуюся к токсичности цианистого водорода . [4]
Гидриды олова олова [ править ]
Гидриды олова олова имеют формулу R 4− n SnH n для значений от n до 4. Родительский член этого ряда, станнан (SnH 4 ), представляет собой нестабильный бесцветный газ. Стабильность коррелирует с количеством органических заместителей. Гидрид трибутилолова используется в качестве источника гидридного радикала в некоторых органических реакциях.
Окислы и гидроксиды олова [ править ]
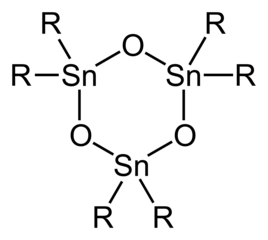
Оксиды и гидроксиды олова-олова являются обычными продуктами гидролиза галогенидов олова. В отличие от соответствующих производных кремния и германия, оксиды и гидроксиды олова часто принимают структуры с пента- и даже гексакоординированными центрами олова, особенно для диоргано- и моноорганопроизводных. Группа Sn-O-Sn называется станноксаном . Структурно простейшими из оксидов и гидроксидов являются производные триорганотина. Коммерчески важным гидроксидом триорганотина является акарицид цигексатин (также называемый пликтраном), ( C 6 H 11 ) 3 SnOH. Такие гидроксиды триорганотина существуют в равновесии с дистанноксанами:
- 2 R 3 SnOH ⇌ R 3 SnOSnR 3 + H 2 O
Имея только два органических заместителя на каждом центре Sn, оксиды и гидроксиды диорганотина имеют более сложную структуру, чем триорганопроизводные. [5] Простые геминальные диолы (R 2 Sn (OH) 2 ) и мономерные станнаноны (R 2 Sn = O) неизвестны. Оксиды диорганотина (R 2 SnO) представляют собой полимеры, за исключением случаев, когда органические заместители очень объемные, в этом случае циклические тримеры или, в случае димеров R = CH (SiMe 3 ) 2 , с кольцами Sn 3 O 3 и Sn 2 O 2. . Дистанноксаны существуют в виде димеров димеров с формулой [R 2 SnX]2 O 2, где группы X (например, хлорид, гидроксид, карбоксилат) могут быть концевыми или мостиковыми (см. Таблицу). Гидролиз тригалогенидов моноорганотина может привести к образованию станнановой кислоты RSnO2H. Что касается оксидов / гидроксидов диорганотина, разновидности моноорганотина образуют структурно сложные комплексы из-за возникновения дегидратации / гидратации, агрегации. Иллюстративным является гидролиз трихлорида бутилолова с образованием [(BuSn) 12 O 14 (OH) 6 ] 2+ .
Шаровидная модель для (t-Bu 2 SnO) 3 .
Структура оксида диорганотина, подчеркивающая обширную межмолекулярную связь.
Сверхкоординированные станнаны [ править ]
В отличие от аналогов углерода (IV), но чем-то вроде соединений кремния, олово (IV) также может быть скоординировано с пятью и даже шестью атомами вместо обычных четырех. Эти гиперкоординированные соединения обычно имеют электроотрицательные заместители. Многочисленные примеры гипервалентности представлены оксидами олова и связанными карбоксилатами и родственными производными псевдогалогенидов. [5] Галогениды оловоорганического соединения для аддуктов, например Me 2 SnCl 2 ( бипиридин ).
Полностьюорганические пента- и гексаорганостаннаты были даже охарактеризованы [6], в то время как в следующем году было сообщено о шестикоординированном тетраорганотиновом соединении. [7] Кристаллическая структура стабильного при комнатной температуре (в аргоне ) полностью углеродного пентаорганостаннана была описана как литиевая соль со следующей структурой: [8]
В этой искаженной тригональной бипирамидальной структуре длины связи углерод-олово (2,26 Å апикальная , 2,17 Å экваториальная) больше, чем регулярные связи C-Sn (2,14 Å), что отражает ее гипервалентную природу.
Катионы триорганотина [ править ]
Некоторые реакции галогенидов триорганотина предполагают роль промежуточных соединений R3Sn +. Такие катионы аналогичны карбокатионам . Они были охарактеризованы кристаллографически, когда органические заместители большие, такие как 2,4,6-триизопропилфенил. [9]
Радикалы олова (органические производные олова (III)) [ править ]
Радикалы олова с формулой R 3 Sn называются станнильными радикалами . [2] Они используются как промежуточные звенья в определенных реакциях переноса атома. Например, гидрид трибутилолова (три-н-бутилстаннан) служит полезным источником «атомов водорода» из-за стабильности радикала трибутитина. [10]
Органические производные олова (II) [ править ]
Оловоорганические соединения (II) встречаются довольно редко. Соединения с эмпирической формулой SnR 2 в некоторой степени хрупки и существуют в виде колец или полимеров, когда R не является объемным. Полимеры, называемые полистаннанами , имеют формулу (SnR 2 ) n .
В принципе, можно ожидать, что соединения двухвалентного олова будут образовывать аналоги алкенов с формальной двойной связью . Действительно, соединения с формулой Sn 2 R 4 , называемые дистанненами , известны определенными органическими заместителями. Центры Sn имеют тенденцию быть высоко пирамидальными. Мономерные соединения с формулой SnR 2 , аналоги карбенов , также известны в единичных случаях. Одним из примеров является Sn (SiR 3 ) 2 , где R - очень объемный CH (SiMe 3 ) 2 (Me = метил). Такие частицы обратимо димеризуются в дистаннилен при кристаллизации: [11]
- 2 R 2 Sn ⇌ (R 2 Sn) 2
Станнены , соединения с двойными связями олово – углерод, представлены производными станнабензола . Stannoles , структурные аналоги из циклопентадиена , демонстрируют мало С-Sn характер двойной связи.
Органические производные олова (I) [ править ]
Соединения Sn (I) встречаются редко и наблюдаются только с очень объемными лигандами. К одному известному семейству клеток получают доступ путем пиролиза 2,6-диэтилфенил-замещенного тристаннилена [Sn (C 6 H 3 -2,6-Et 2 ) 2 ] 3 , который дает кластер кубанового типа и призман . Эти клетки содержат Sn (I) и имеют формулу [Sn (С 6 Н 3 -2,6-Et 2 )] п , где п = 8, 10. [12] stannyne содержит углерод олова тройной связии удаленная тройная связь между двумя атомами олова (RSnSnR). Дистаннины существуют только для чрезвычайно объемных заместителей. В отличие от алкинов , C-Sn-Sn-C ядро этих дистаннинов нелинейно, хотя и является плоским. Расстояние Sn-Sn составляет 3,066 (1) Å, а углы Sn-Sn-C составляют 99,25 (14) °. Такие соединения получают восстановлением объемных галогенидов арилтина (II). [13]
Подготовка [ править ]
Оловоорганические соединения можно синтезировать множеством методов. [14] Классическая реакция реактива Гриньяра с галогенидами олова, например с тетрахлоридом олова . Примером может служить синтез тетраэтилолова: [15]
- 4 EtMgBr + SnCl 4 → Et 4 Sn + 4 MgClBr
Симметричные тетраорганотиновые соединения, особенно тетраалкильные производные, затем могут быть преобразованы в различные смешанные хлориды реакциями перераспределения (также известными как «компропорционирование Кочешкова» в случае оловоорганических соединений):
- 3 R 4 Sn + SnCl 4 → 4 R 3 SnCl
- R 4 Sn + SnCl 4 → 2 R 2 SnCl 2
- R 4 Sn + 3 SnCl 4 → 4 RSnCl 3
Родственный метод включает перераспределение галогенидов олова с алюминийорганическими соединениями .
Смешанные органо-галогеновые соединения олова можно превратить в смешанные органические производные, как показано на синтезе дибутилдивинилолова: [16]
- Bu 2 SnCl 2 + 2 C 2 H 3 MgBr → Bu 2 Sn (C 2 H 3 ) 2 + 2 MgBrCl
Гидриды оловаорганического происхождения образуются путем восстановления смешанных алкилхлоридов. Например, лечение дибутилолов дихлорид с литийалюминийгидридом дает дибутилолов дигидрид, бесцветное масло: дистиллируемое [17]
Вюрец-подобные соединения из алкильных соединений натрия с галогенидами олова выходами tetraorganotin соединений.
Гидростаннилирование включает катализируемое металлами присоединение гидридов олова через ненасыщенные субстраты. [18]
Реакции [ править ]
Важные реакции, обсуждавшиеся выше, обычно сосредоточены на галогенидах олова и псевдогалогенидах с нуклеофилами. В области органического синтеза , то реакция Stille считается важным. Это влечет за собой реакцию сочетания с sp2-гибридизованными органическими галогенидами, катализируемую палладием:
и органостаннановые добавки (нуклеофильное присоединение аллил-, алленил- или пропаргилстаннанов к альдегидам и иминам). Оловоорганические соединения также широко используются в радикальной химии (например, радикальная циклизация , деоксигенация Бартона – МакКомби , декарбоксилирование Бартона и т. Д.).
Приложения [ править ]
Оловоорганическое соединение коммерчески применяется в качестве стабилизатора поливинилхлорида . В этом качестве они подавляют разложение, удаляя аллильные хлоридные группы и абсорбируя хлористый водород. Это приложение потребляет около 20 000 тонн олова в год. Основным классом оловоорганических соединений являются дитиолаты диорганотина с формулой R 2 Sn (SR ') 2 . Связь Sn-S является реактивным компонентом. Карбоксилаты диорганотина, например дилаурат дибутилолова , используются в качестве катализаторов для образования полиуретанов , для вулканизации силиконов и переэтерификации . [2]
Трихлорид н-бутилолова используется в производстве слоев диоксида олова на стеклянных бутылках путем химического осаждения из паровой фазы .
Биологические приложения [ править ]
« Трибутилоловы » используются в качестве промышленных биоцидов , например, в качестве противогрибковых агентов в текстильных изделиях и бумаге, системах целлюлозно-бумажных комбинатов, пивоваренных заводах и промышленных системах охлаждения. Производные трифенилолова используются в качестве активных компонентов противогрибковых красок и сельскохозяйственных фунгицидов. Другие triorganotins используются в качестве акарицидов и акарицидов . Оксид трибутилолова широко используется в качестве консерванта для древесины . [2]
Когда-то соединения трибутилолова широко использовались в качестве агентов против биообрастания в морской среде для повышения эффективности океанских судов. Обеспокоенность по поводу токсичности [19] этих соединений (в некоторых отчетах описывается биологическое воздействие на морскую жизнь при концентрации 1 нанограмм на литр) привела к всемирному запрету Международной морской организацией . В качестве противообрастающих соединений оловоорганические соединения были заменены дихлороктилизотиазолиноном . [20]
- Оловоорганические соединения
Бесцветное масло тетрабутилолова , предшественник других соединений бутилолова
Оксид трибутилолова , жидкость от бесцветного до бледно-желтого цвета, используемая для консервирования древесины.
Ацетат трифенилолова , не совсем белое кристаллическое вещество, используемое в качестве инсектицида и фунгицида.
Хлорид трифенилолова , высокотоксичное белое твердое вещество, используемое в качестве биоцида.
Хлорид триметилолова , токсичное белое твердое вещество, когда-то использовалось в качестве биоцида.
Гидроксид трифенилолова , не совсем белый порошок, используемый в качестве фунгицида.
Азоциклотин , белое твердое вещество, используется в качестве акарицида длительного действия для борьбы с паутинным клещом на растениях.
Цигексатин, белое твердое вещество, используется как акарицид и митицид.
Гексаметилдитин используется в качестве промежуточного продукта в химическом синтезе.
Тетраэтилолово , температура кипения 63–65 ° / 12 мм, является катализатором [21]
Токсичность [ править ]
Токсичность соединений производных трибутилолова и трифенилолова сопоставима с токсичностью цианистого водорода . Кроме того, три- н- алкилоловы являются фитотоксичными и поэтому не могут использоваться в сельском хозяйстве. В зависимости от органических групп они могут быть мощными бактерицидами и фунгицидами . Отражая свою высокую биологическую активность, «трибутилоловы» когда-то использовались в краске против обрастания морских судов . [2]
В отличие от триорганотиновых соединений, монооргано-, диоргано- и тетраорганотиновые соединения гораздо менее опасны. [4]
Однако DBT может быть иммунотоксичным. [22]
См. Также [ править ]
- Добавка органостаннана
- Азид трибутилолова
- Карбастаннатраны
Ссылки [ править ]
- ^ Caseri, Вальтер (2014). «Исходная химия оловоорганических соединений». Журнал металлоорганической химии . 751 : 20–24. DOI : 10.1016 / j.jorganchem.2013.08.009 .
- ^ a b c d e Дэвис, Олвин Джордж. (2004) Organotin Chemistry, 2nd Edition Weinheim: Wiley-VCH. ISBN 978-3-527-31023-4
- ^ Gielen, Марсель (1973). «От кинетики к синтезу хиральных тетраорганотиновых соединений». В соотв. Chem. Res . 6 (6): 198–202. DOI : 10.1021 / ar50066a004 .
- ^ a b Г. Г. Граф (2005). «Олово, оловянные сплавы и соединения олова». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a27_049 .
- ^ а б Чандрасекар, Вадапалли; Нагендран, Сельвараджан; Баскар, Вишванатан (2002). «Оловоорганические сборки, содержащие связи Sn / O». Обзоры координационной химии . 235 : 1–52. DOI : 10.1016 / S0010-8545 (02) 00178-9 .
- ^ Райх, Ганс Дж .; Филлипс, Нэнси Х. (1986). "Литий-металлоидные обменные реакции. Обнаружение комплексов пентаалкил / арилолово лития". Варенье. Chem. Soc. 108 (8): 2102–2103. DOI : 10.1021 / ja00268a067 .
- ^ В.Г. Кумар Дас; Ло Конг Мун; Чен Вэй; Томас CW Мак (1987). «Синтез, спектроскопическое исследование и рентгеновская кристаллическая структура бис [3- (2-пиридил) -2-тиенил-C, N] дифенилолова (IV): первый пример шестикоординированного соединения тетраорганотина»). Металлоорганические соединения . 6 : 10–14. DOI : 10.1021 / om00144a003 .
- ^ Масаичи Сайто; Санаэ Имаидзуми; Томоюки Тадзима; Казуя Ишимура и Сигеру Нагасэ (2007). «Синтез и структура пентаорганостанната, имеющего пять углеродных заместителей». Варенье. Chem. Soc. 129 : 10974–10975. DOI : 10.1021 / ja072478 + . PMID 17705378 .
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8.
- ^ TV RajanBabu, страница PCB BR Бакли «Три-н-бутилстаннан» в энциклопедии реагентов для органического синтеза e-EROS, 2004. doi : 10.1002 / 047084289X.rt181.pub2
- ^ Холлеман, Арнольд Фредерик; Виберг, Эгон (2001), Виберг, Нильс (ред.), Неорганическая химия , перевод Иглсона, Мэри; Брюэр, Уильям, Сан-Диего / Берлин: Academic Press / De Gruyter, ISBN 0-12-352651-5
- ^ Сита, Лоуренс Р. (1994). «Органическая химия тяжелых металлов: строительство с оловом». В соотв. Chem. Res . 27 (7): 191–197. DOI : 10.1021 / ar00043a002 .
- Перейти ↑ Power, Philip P. (2007). «Связывание и реакционная способность более тяжелых аналогов алкинов из 14 элементов». Металлоорганические соединения . 26 (18): 4362–4372. DOI : 10.1021 / om700365p .
- ^ Сандер HL Thoonen; Берт-Ян Дилман; Жерар ван Котен (2004). «Синтетические аспекты тетраорганотинов и оловоорганических (IV) галогенидов» (PDF) . Журнал металлоорганической химии (689): 2145–2157.
- ^ Der Kerk, GJM Van; Луйтен, JGA (1956). «Тетраэтилолово». Орг. Synth . 36 : 86 и далее. DOI : 10.15227 / orgsyn.036.0086 .
- ^ Сейферт, Дитмар (1959). «Ди-н-бутилдивинилолово». Орг. Synth . 39 : 10. DOI : 10,15227 / orgsyn.039.0010 .
- ^ "Металлоорганические синтезы: соединения непереходных металлов" Джон Эйш, изд. Academic Press: Нью-Йорк, 1981. ISBN 0122349504 .
- ^ Смит, Николас Д .; Манкузо, Джон; Лаутенс, Марк (2000). "Гидростанции, катализируемые металлами". Химические обзоры . 100 (8): 3257–3282. DOI : 10.1021 / cr9902695 . PMID 11749320 .
- ^ Гайда, М .; Янцо, А. (2010). «Оловоорганические соединения, образование, использование, видообразование и токсикология». Ионы металлов в науках о жизни . Кембридж: Издательство RSC. 7. Металлоорганические соединения в окружающей среде и токсикология: 111–151. DOI : 10.1039 / 9781849730822-00111 . ISBN 9781847551771.
- ^ Сильва, Ваня; Сильва, Катия; Соарес, Педро; Гарридо, Э. Мануэла; Борхес, Фернанда; Гарридо, Хорхе (2020). «Изотиазолиноновые биоциды: химические, биологические и токсические профили» . Молекулы . 25 (4): 991. DOI : 10.3390 / modules25040991 . PMC 7070760 . PMID 32102175 .
- ^ Organic Syntheses , Coll. Vol. 4, стр.881 (1963); Vol. 36, стр.86 (1956). Связь
- ^ C Gumy; и другие. (2008). «Дибутилтин нарушает функцию рецептора глюкокортикоидов и нарушает индуцированное глюкокортикоидом подавление продукции цитокинов» . PLOS ONE . 3 (10): e3545. Bibcode : 2008PLoSO ... 3.3545G . DOI : 10.1371 / journal.pone.0003545 . PMC 2568824 . PMID 18958157 .
Внешние ссылки [ править ]
- Информационный бюллетень по национальному кадастру загрязнителей для оловоорганических соединений
- Информационный сайт отрасли
- Оловоорганическая химия в синтезе


![Схема реакции Стилла {\ displaystyle {\ ce {{RX} + R'-SnR''3 -> [{\ ce {Pd \ Catalyst}}] {R-R '} + XSnR''3}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/16d2a781e9a7142312c1fd6052ce33fc93f0814a)