Паклитаксел полный синтез в органической химии является одним из основных текущих исследований усилия в общем синтезе из паклитаксела (таксола). [1] Этот дитерпеноид является важным лекарством при лечении рака, но он также является дорогостоящим, поскольку его получают из ограниченного ресурса, а именно из тихоокеанского тиса ( Taxus brevifolia ). Не только синтетическое воспроизведение самого соединения имеет большое коммерческое и научное значение, оно также открывает путь к производным паклитаксела, которые не встречаются в природе, но обладают большим потенциалом.
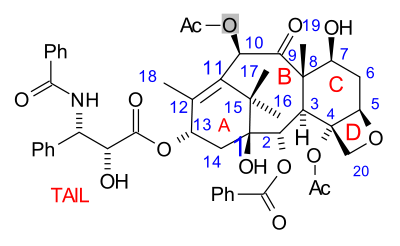
Молекула паклитаксела состоит из тетрациклического ядра, называемого баккатином III, и амидного хвоста. Основные кольца удобно называть (слева направо) кольцом A ( циклогексен ), кольцом B ( циклооктан ), кольцом C ( циклогексан ) и кольцом D ( оксетаном ).
Процесс разработки лекарственного средства паклитаксела занял более 40 лет. Противоопухолевая активность экстракта коры тиса тихоокеанского была обнаружена в 1963 году в результате программы скрининга растений правительства США, которая уже существовала за 20 лет до этого. Активное вещество, отвечающее за противоопухолевую активность, было обнаружено в 1969 году, а выяснение структуры было завершено в 1971 году. Роберт А. Холтон из Университета штата Флорида преуспел в полном синтезе паклитаксела в 1994 году, проекте, который он начал в 1982 году. 1989 Холтон также разработал полусинтетический способ получения паклитаксела, исходя из 10-деацетилбаккатина III . Это соединение является предшественником биосинтеза и содержится в Taxus baccata в больших количествах, чем сам паклитаксел.(Тис Европейский). В 1990 году компания Bristol-Myers Squibb купила лицензию на патент на этот процесс, который в последующие годы принес Университету штата Флорида и Холтону (с долей 40%) более 200 миллионов долларов США .
Полный синтез [ править ]
Полный синтез таксола называют одним из самых горячих споров 1990-х годов [2], к 1992 году около 30 конкурирующих исследовательских групп. Число исследовательских групп, фактически сообщивших о полном синтезе, в настоящее время составляет 10 с группой Холтона (первая статья принято к публикации) и группа Николау (статья опубликована первой) первой и второй в так называемом фотофинише.
Некоторые из них действительно синтетические, но в других включена молекула-предшественник, встречающаяся в природе. Основные данные собраны ниже. Общим для всех стратегий является синтез молекулы баккатина с последующим добавлением хвоста на последней стадии, процесс (кроме одного), основанный на лактаме Одзима .
- Общий синтез таксола Холтона - год: 1994 - предшественник: пачулол - стратегия: линейный синтез AB, затем C, затем D - ссылки: см. Соответствующую статью [3] [4]
- Полный синтез таксола Николау - год: 1994 - предшественник: стратегия слизистой кислоты : конвергентный синтез A и C сливаются с ABC, затем D - ссылки: см. Соответствующую статью [5]
- Полный синтез таксола Данишефски - год: 1996 - предшественник: стратегия кетонов Виланда-Мишера : конвергентный синтез C сливается с D, затем с A сливается с ABCD - ссылки: См. Статью по теме
- Общий синтез таксола Вендера - год: 1997 - прекурсор: стратегия пинена : линейный синтез AB, затем C, затем D - ссылки: [6] [7]
- Общий синтез таксола Кувадзима I. Kuwajima, - год: 1998 - прекурсор: синтетические строительные блоки стратегия: линейный синтез A, затем B, затем C, затем D [8] [9]
- Общий синтез таксола Мукаяма - год: 1998 [10] - Предшественник: стратегия L-серина : линейный синтез B, затем C, затем A, затем D. Ссылки: см. Соответствующую статью.
- Общий синтез Такахаши Таксола - год: 2006 [11] - Прекурсор: гераниол, стратегия: конвергентный синтез A и C сливаются в ABC, затем D
- Полный синтез таксола Sato-Chida - год: 2015, формальный синтез до промежуточного соединения Takahashi [12] [13] [14]
- Полный синтез таксола Накада - год: 2015, формальный синтез до промежуточного продукта Такахаши [15]
- Полный синтез таксола Баран - год: 2020, полный синтез с помощью двухфазного дивергентного синтетического подхода. [16]
Текущие исследования направлены на синтез таксадиеновых и таксадиеноновых промежуточных продуктов. Синтез родственных таксанов decinnamoyltaxinine Е и taxabaccatin III сообщалось [17]
Полусинтез [ править ]
Коммерческий полусинтез (компанией Bristol-Myers Squibb ) паклитаксела, начиная с 10-деацетилбаккатина III (выделенного из тиса европейского), основан на добавлении хвоста так называемого лактама Одзима к его свободной гидроксильной группе:
Другой коммерческий полусинтез (разработанный компанией Natural Pharmaceuticals ) основан на выделении группы производных паклитаксела, выделенных из первичных декоративных таксанов. Эти производные имеют тот же скелет, что и паклитаксел, за исключением органического остатка R концевой амидной группы, который может быть фенилом , пропилом или пентилом (среди прочих), тогда как в паклитакселе это явная фенильная группа. Полусинтез состоит из превращения амидной группы в амин с реактивом Шварца через имин с последующей кислотной обработкой и бензоилированием.
В процессе производства тисы, выращенные в штате Мичиган, созревают за 8 лет, периодически их покрывают и сушат. Этот материал отправляется в Мексику для первой стадии экстракции (содержание паклитаксела 10%), а затем в Канаду для дальнейшей очистки до чистоты 95%. Полусинтез до конечного продукта происходит в Китае. [18]
Биосинтез [ править ]
Путь биосинтеза паклитаксела был исследован и состоит примерно из 20 ферментативных стадий. Полная схема пока недоступна. Известные сегменты сильно отличаются от синтетических путей, опробованных до сих пор ( схема 1 ). Исходное соединение геранилгеранильной дифосфат 2 [19] , которая является димером гераниола 1 . Это соединение уже содержит все необходимые 20 атомов углерода для скелета паклитаксела. Большее закрытие кольца через промежуточное соединение 3 ( таксадиен ) приводит к таксусину 4 . Две основные причины, по которым этот тип синтеза невозможен в лаборатории, заключаются в том, что природа гораздо лучше справляется с управлениемстереохимия и гораздо лучшая работа по активации углеводородного скелета с кислородными заместителями, за которые цитохром P450 отвечает за оксигенацию. Промежуточное соединение 5 называется 10-деацетилбаккатин III.
Сообщалось о биохимическом производстве таксадиена в килограммах с использованием генно-инженерной E. coli в 2011 году [20].
Ссылки и примечания [ править ]
- ^ Обратите внимание, что в оригинальных публикациях о полном синтезе используется название «таксол», которое использовалось как родовое название до того, как оно было принято в качестве товарного знака в 1992 году.
- ^ Нина Холл (2003) «Создание сложности - красота и логика синтеза» Chem. Commun. 2003 (6), 661-664. DOI : 10.1039 / b212248k
- ^ Роберт А. Холтон ; Кармен Сомоса; Хён Байк Ким; Фэн Лян; Рональд Дж. Бидигер; П. Дуглас Боутман; Мицуру Шиндо; Чейз С. Смит; Соэкчан Ким; Хоссейн Надизаде; Юкио Сузуки; Чуньлинь Тао; Фонг Ву; Сухан Тан; Пиншэн Чжан; Кришна К. Мурти; Лиза Н. Джентиле; Цзянвэй Х. Лю (1994). «Первый полный синтез таксола. 1. Функционализация кольца B». Варенье. Chem. Soc. 116 (4): 1597–1598. DOI : 10.1021 / ja00083a066 .
- ^ Роберт А. Холтон ; Хён-Байк Ким; Кармен Сомоса; Фэн Лян; Рональд Дж. Бидигер; П. Дуглас Боутман; Мицуру Шиндо; Чейз С. Смит; Соэкчан Ким; Хоссейн Надизаде; Юкио Сузуки; Чуньлинь Тао; Фонг Ву; Сухан Тан; Пиншэн Чжан; Кришна К. Мурти; Лиза Н. Джентиле; Цзянвэй Х. Лю (1994). «Первый полный синтез таксола. 2. Завершение C и D колец». Варенье. Chem. Soc. 116 (4): 1599–1600. DOI : 10.1021 / ja00083a067 .
- ^ Николау, KC ; Ян, З .; Лю, JJ; Ueno, H .; Nantermet, PG; Гай, РК; Claiborne, CF; Renaud, J .; Куладурос, EA; Paulvannan, K .; Соренсон, EJ (1994). «Полный синтез таксола». Природа . 367 (6464): 630–634. Bibcode : 1994Natur.367..630N . DOI : 10.1038 / 367630a0 . PMID 7906395 .
- ^ Пол А. Вендер , Нил Ф. Бэдхэм, Саймон П. Конвей, Пол Э. Флорианциг, Тимоти Э. Гласс, Кристиан Греничер, Джонатан Б. Хуз, Ян Йеничен, Дэсунг Ли, Дэниел Г. Маркиз, Пол Л. МакГрейн, Вей Мэн, Томас П. Муччаро, Мишель Мюлебах, Майкл Г. Натчус, Хольгер Паулсен, Дэвид Б. Роулинз, Джеффри Саткофски, Энтони Дж. Шукер, Джеймс С. Саттон, Ричард Э. Тейлор и Кацухико Томоока (1997) " Путь пинена к таксанам. 5. Стереоконтролируемый синтез универсального предшественника таксана " J. Am. Chem. Soc. 119 (11), 2755-2756 (Связь) doi : 10.1021 / ja9635387
- ^ Пол А. Вендер , Нил Ф. Бэдхэм, Саймон П. Конвей, Пол Э. Флорианциг, Тимоти Э. Гласс, Джонатан Б. Хуз, Нэнси Е. Краусс, Дэсон Ли, Дэниел Г. Маркиз, Пол Л. Макгрейн, Вэй Менг, Майкл Г. Натчус, Энтони Дж. Шукер, Джеймс С. Саттон и Ричард Э. Тейлор (1997) «Путь пинена к таксанам. 6. Краткий стереоконтролируемый синтез таксола» J. Am. Chem. Soc. 119 (11), 2757-2758 (Связь) doi : 10.1021 / ja963539z
- ^ Коитиро Morihira, Ryoma Хара, Shigeru Кавахара, Тосиюки Нисимори, Nobuhito Накамура, Хироюки Кусама и Исао Kuwajima (1998) "Энантиоселективное Полный синтез таксола" J. Am. Chem. Soc. 120 (49), 12980-12981 (Связь) doi : 10.1021 / ja9824932
- ^ Хироюки Кусама, Риома Хара, Сигэру Кавахара, Тосиюки Нисимори, Хадзиме Кашима, Нобухито Накамура, Коитиро Морихира и Исао Куваджима (2000) «Энантиоселективный полный синтез (-) - таксола» J. Am. Chem. Soc. 122 (16) 3811-3820. DOI : 10.1021 / ja9939439
- ^ Исаму Шиина, Хаято Iwadare, Хироки Sakoh, Masatoshi Hasegawa, Yu-ichirou Tani и Teruaki Mukaiyama (1998) "Новый метод синтеза баккатина III" Chemistry Letters 27 (1), 1-2 DOI : 10,1246 / мл .1998.1
- ^ Такаюки Doi, Синитиро взрыватель, Миямото, Kazuoki Накаи, Дайсуке Sasuga и Такаши Такахаши (2006) «Формальное Полный синтез таксола Помогший автоматизированной Синтезатор» химии: Азиатский журнал 1 (3), 370-383. DOI : 10.1002 / asia.200600156
- ↑ Кейсуке Фукая, Юта Танака, Аяко С. Сато, Кейсуке Кодама, Хирохиса Ямадзаки, Такеру Ишимото, Ясуёси Нодзаки, Юки М. Иваки, Ёхей Юки, Кентаро Умей, Томоя Сугай, Юаки Ямагути, Такэси Ойакэси, Такэси Ойакэси, Такэси Ойакэси и Норитака Чида (2015) «Синтез паклитаксела. 1. Синтез ABC-кольца паклитаксела посредством SmI 2 -опосредованной циклизации» Organic Letters 17 (11), 2570-2573 doi : 10.1021 / acs.orglett.5b01173
- ↑ Кейсуке Фукая, Кейсуке Кодама, Юта Танака, Хирохиса Ямазаки, Томоя Сугай, Ю Ямагути, Ами Ватанабе, Такеши Оиси, Такааки Сато и Норитака Чида (2015) «Синтез паклитаксела. 2. Построение кольца ABCD и формальный синтез» Органические письма 17 (11), 2574-2577 doi : 10.1021 / acs.orglett.5b01174
- ^ DF Taber (5 октября 2015 г.) The Sato / Chida Synthesis of Paclitaxel Organic Chemistry Highlights (www.organic-chemistry.org)
- ↑ Сё Хираи, Масаюки Уцуги, Мицухиро Ивамото, Масахиса Накада (2015), «Формальный полный синтез (-) - таксола через образование восьмичленных карбоциклических колец, катализируемых палладием», Химия: Европейский журнал 21 (1), 355–359 . DOI : 10.1002 / chem.201404295
- ^ Yuzuru Канда, Хью Накамура, Сигэнобу Umemiya, Ravi Kumar Puthukanoori, Venkata Рамана Мурти Appala, Гопи Кришна Gaddamanugu, Bheema Рао Paraselli, и Фил Баран (2020), "Двухфазное Синтез таксола" дои : 10,26434 / chemrxiv.12061620. v1
- ^ Чанся Юань, Иехуа Цзинь, Натан С. Уайлд, Фил С. Баран (2016) «Краткий, энантиоселективный тотальный синтез сильно окисленных таксанов» Angew. Chem. Int. Эд. 55 (29), 8280-8284 DOI : 10.1002 / anie.201602235
- ^ Брюс Ганем и Роланд Р. Франке (2007) «Паклитаксел из первичных таксанов: перспектива творческих изобретений в химии циркония» J. Org. Chem. 72 (11), 3981-3987. DOI : 10.1021 / jo070129s
- ^ MyDoanh Чау, Стефан Jennewein, Кевин Уокер, и Родня Крото (2004) таксол Биосинтез: Молекулярное клонирование и характеристика цитохрома Р450 таксоиды 7 & beta-гидроксилаза химии и биологии , 11 (5), 663-672, DOI : 10.1016 / J. хембиол.2004.02.025
- ^ Ajikumar, Parayil Kumaran; Сяо, Вэнь-Хай; Тио, Кейт Э.Дж.; Ван, Юн; Симеон, Фриц; Леонард, Эффенди; Муха, Оливер; Фон, Тоо Хэн; Пфайфер, Блейн; Стефанопулос, Грегори (2010). «Оптимизация пути изопреноидов для перепроизводства предшественников таксола в Escherichia coli » . Наука . 330 (6000): 70–74. Bibcode : 2010Sci ... 330 ... 70A . DOI : 10.1126 / science.1191652 . PMC 3034138 . PMID 20929806 .
Внешние ссылки [ править ]
- Общий синтез паклитаксела @ SynArchive.com
- Taxolog для исследования Taxol, основанная Holto
- Полная история Taxol от Chemical & Engineering News : Статья
- Обширная статья в Университете штата Флорида
- История полного синтеза таксола