 | |
| Имена | |
|---|---|
| Систематическое название ИЮПАК | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| Номер ЕС |
|
| 492 | |
| КЕГГ | |
| MeSH | Кислород |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 1072 |
| |
| |
| Характеристики | |
| O 2 | |
| Молярная масса | 31,998 г · моль -1 |
| Внешность | Бесцветный газ |
| Температура плавления | -218,2 ° С; -360,7 ° F; 55.0 К |
| Точка кипения | -183,2 ° С; -297,7 ° F; 90.0 К |
| Структура | |
| Линейный | |
| 0 Д | |
| Термохимия | |
Стандартная мольная энтропия ( S | 205,152 Дж.К. -1 моль -1 |
Std энтальпия формации (Δ F H ⦵ 298 ) | 0 кДж моль −1 |
| Фармакология | |
| V03AN01 ( ВОЗ ) | |
| Опасности | |
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Опасность |
| H270 | |
| P220 , P244 , P370 + 376 , P403 | |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Триплетный кислород , 3 O 2 , относится к основному электронному состоянию S = 1 молекулярного кислорода (дикислорода). Это является наиболее стабильным и распространенным аллотропом из кислорода . Молекулы триплетного кислорода содержат два неспаренных электрона, что делает триплетный кислород необычным примером стабильного и часто встречающегося бирадикала : [2] он более стабилен как триплет, чем синглет . Согласно теории молекулярных орбиталей , электронная конфигурация триплетного кислорода состоит из двух электронов, занимающих две π- молекулярные орбитали.(МО) равной энергии (то есть вырожденные МО ). В соответствии с правилами Хунда они остаются непарными и параллельными по спину, что объясняет парамагнетизм молекулярного кислорода. Эти наполовину заполненные орбитали имеют антисвязывающий характер, снижая общий порядок связи молекулы до 2 с максимального значения 3 (например, диазот), который возникает, когда эти антисвязывающие орбитали остаются полностью незанятыми. Термин символ молекулярная для триплетного кислорода 3 Σ-
г. [3]
Спин [ править ]
В ы = 1 / 2 спины двух электронов в вырожденных орбиталей приводит к 2 × 2 = 4 независимых спиновых состояний в общей сложности. Обменное взаимодействие разбивает их на синглетное состояние (общий спин S = 0) и набор из 3 вырожденных триплетных состояний ( S = 1). В соответствии с правилами Хунда , триплетные состояния энергетически более выгодны и соответствуют основному состоянию молекулы с полным электронным спином S = 1. Возбуждение в состояние S = 0 приводит к гораздо более реакционному метастабильному синглетному кислороду .[4] [5]
Структура Льюиса [ править ]
Поскольку молекулы в основном состоянии имеет ненулевой спин магнитный момент , кислород является парамагнитным ; т. е. его можно притягивать к полюсам магнита . Таким образом, структура Льюиса O = O со всеми электронами в парах не точно отражает природу связи в молекулярном кислороде. Однако альтернативная структура • O – O • также неадекватна, поскольку подразумевает характер одинарной связи, в то время как экспериментально определенная длина связи 121 пм [6] намного короче, чем одинарная связь в перекиси водорода (HO-OH), которая имеет длиной 147,5 м. [7]Это указывает на то, что триплетный кислород имеет более высокий порядок связи. Чтобы правильно объяснить наблюдаемый парамагнетизм и короткую длину связи одновременно, необходимо использовать теорию молекулярных орбиталей . В рамках теории молекулярных орбиталей связь кислород-кислород в триплетном дикислороде лучше описывать как одну полную σ-связь плюс две π-полусвязи, причем каждая полусвязь объясняется двухцентровой трехэлектронной (2c-3e) связью , чтобы получить чистый порядок облигаций, равный двум (1 + 2 ×1/2) с учетом спинового состояния ( S = 1). В случае триплетного дикислорода каждая связь 2c-3e состоит из двух электронов на связывающей орбитали π u и одного электрона на антисвязывающей орбитали π g, что дает чистый вклад порядка связи в1/2.
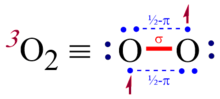
Обычные правила построения структур Льюиса должны быть изменены, чтобы приспособить молекулы, такие как триплетный дикислород или оксид азота, которые содержат связи 2c-3e. По этому поводу нет единого мнения; Полинг предложил использовать три близко расположенных коллинеарных точки, чтобы обозначить трехэлектронную связь (см. Иллюстрацию). [8]
Наблюдение в жидком состоянии [ править ]
Обычный экспериментальный способ наблюдать парамагнетизм дикислорода - охладить его до жидкой фазы. Если налить жидкий кислород между полюсами сильных магнитов, которые расположены близко друг к другу, он может быть взвешен. Или магнит может тянуть струю жидкого кислорода, когда он льется. Теория молекулярных орбиталей дает объяснение этим наблюдениям.
Реакция [ править ]
Необычная электронная конфигурация препятствует прямому взаимодействию молекулярного кислорода со многими другими молекулами, которые часто находятся в синглетном состоянии . Однако триплетный кислород будет легко реагировать с молекулами в дублетном состоянии с образованием нового радикала.
Для сохранения спинового квантового числа потребуется триплетное переходное состояние в реакции триплетного кислорода с замкнутой оболочкой (молекула в синглетном состоянии). Требуемой дополнительной энергии достаточно для предотвращения прямой реакции при температуре окружающей среды со всеми субстратами, кроме наиболее реактивных, например, с белым фосфором . При более высоких температурах или в присутствии подходящих катализаторов реакция протекает легче. Например, большинство легковоспламеняющихся веществ характеризуются температурой самовоспламенения, при которой они будут гореть на воздухе без внешнего пламени или искры.
Ссылки [ править ]
- ^ a b «Триплетный диоксид кислорода (CHEBI: 27140)» . Химические объекты, представляющие биологический интерес (ChEBI) . Великобритания: Европейский институт биоинформатики.
- ^ Борден, Уэстон Тэтчер; Хоффманн, Роальд; Stuyver, Thijs; Чен, Бо (2017). «Диоксид кислорода: что делает этот триплетный бирадикал кинетически устойчивым?» . Журнал Американского химического общества . 139 (26): 9010–9018. DOI : 10.1021 / jacs.7b04232 . PMID 28613073 .
- ^ Аткинс, Питер; Де Паула, Хулио; Фридман, Рональд (2009) Quanta, Matter, and Change: A Molecular Approach to Physical Chemistry, pp. 341–342, Oxford: Oxford University Press, ISBN 0199206066 , см. [1] . по состоянию на 11 августа 2015 г.
- ^ Wulfsberg, Гэри (2000). Неорганическая химия . Саусалито, Калифорния: University Science Press. п. 879. ISBN 9781891389016.
- ^ Массачусетский технологический институт (2014). «Состояния кислорода» (PDF) . Принципы неорганической химии I .
- ^ Housecroft, Екатерина Е .; Шарп, Алан Г. (2005). Неорганическая химия (2-е изд.). Пирсон Прентис-Холл. п. 438. ISBN 978-0130-39913-7.
- ^ Housecroft и Шарп p.443
- ^ Maksic, ZB; Орвилл-Томас, WJ (1999). Наследие Полинга: современное моделирование химической связи . Амстердам: Эльзевир. п. 455. ISBN 978-0444825087.
Дальнейшее чтение [ править ]
- ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Онлайн-исправленная версия: (2006–) « синглетный молекулярный кислород (синглетный молекулярный дикислород) ». DOI : 10,1351 / goldbook.S05695
Внешние источники [ править ]
- http://meta-synthesis.com/webbook/16_diradical/diradical.html [ необходим лучший источник ]
