 | |
 | |
| Клинические данные | |
|---|---|
| Пути администрирования | Оральный , испарившийся , интраназально , Инъецированный |
| Правовой статус | |
| Правовой статус |
|
| Фармакокинетические данные | |
| Биодоступность | 62% орально; 79% назальный; 91 - 93,5% копченых; 100% IV |
| Метаболизм | Печеночный |
| Ликвидация Период полураспада | 10-19 часов |
| Экскреция | Почечный |
| Идентификаторы | |
| |
| Количество CAS |
|
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII |
|
| Химические и физические данные | |
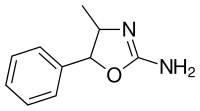
| Формула | C 10 H 12 N 2 O |
| Молярная масса | 176,21 г · моль -1 |
| 3D модель ( JSmol ) | |
| Хиральность | Рацемическая смесь |
| |
| |
| | |
4-метиламинорекс ( 4-МАР , 4-MAX ) является стимулятором препарат из 2- амино -5- aryloxazoline класса , который был впервые синтезирован в 1960 году McNeil Laboratories. [1] Он также известен под названиями улиц « U4Euh » (« Эйфория ») и « Лед ». Он запрещен во многих странах как стимулятор .
4-Метиламинорекс имеет эффекты, сравнимые с метамфетамином, но с большей продолжительностью.
Результаты экспериментов на животных, проведенных с этим наркотиком, позволяют предположить, что он имеет склонность к злоупотреблению, аналогичную кокаину и амфетамину. Одно исследование показало, что «стимулирующие свойства рацемического цис-, рацемического транс-и всех четырех отдельных оптических изомеров 4-метиламинорекса были изучены на крысах, обученных отличать 1 мг / кг S (+) сульфата амфетамина от физиологического раствора. ) стимул амфетамина, распространенный на всех исследованных агентов ». [2] Второе исследование, в котором крысы обучались отличать 0,75 мг / кг S (+) - амфетамина или 1,5 мг / кг фенфлурамина от физиологического раствора, распространенного на аминорекс в качестве стимулятора амфетамина, но не на фенфлурамин. [3]Крысы обучены отличать 8 мг / кг кокаина от общего 4-метиламинорекса солевого раствора и кокаинового раздражителя. [4] Усиливающие эффекты цис-4-метиламинорекса были определены на двух моделях внутривенного введения лекарств приматам. Дозы носителя или 4-метиламинорекса были заменены на кокаин. Одна из двух различных доз 4-метиламинорекса поддерживала поведение при самостоятельном введении выше контрольных уровней носителя. [5]
Химия [ править ]
4-Метиламинорекс существует в виде четырех стереоизомеров : (±) - цис и (±) - транс . (±) - цис- изомеры - форма, используемая в рекреационных целях . (±) - цис- изомеры [рацемат (смесь 1: 1) (4 R , 5 S ) -изомера и энантиомерный (4 S , 5 R ) -изомер], как правило, синтезируются из dl-фенилпропаноламина в одну стадию путем циклизации с цианогенбромидом (иногда готовят на месте путем реакции цианида натрия с бромом). Альтернативные пути синтеза обычно включают больше стадий, таких как замена цианогенбромида цианатом натрия или калия с образованием промежуточного продукта, а затем его взаимодействие с концентрированной соляной кислотой . Метод, описанный в микрограммах, заменил необходимость отдельного добавления соляной кислоты , начав с гидрохлоридной соли dl-фенилпропаноламина, но были отмечены побочные продукты. (±) - транс- изомеры [рацемат (смесь 1: 1) (4 S , 5 S ) -изомера и энантиомерный (4 R , 5 R ) -изомер] синтезируются таким же образом, как указано выше, но dl- норэфедринвместо этого используется в качестве исходного материала. Реакция с цианатом протекает иначе, чем с цианогенбромидом, и вместо этого превращает норэфедрин в транс-4-метиламинорекс, как отмечено на микрофотографии DEA. Цианогенбромид, для сравнения, преобразовал норэфедрин в цис-изомер и норпсевдоэфедрин в транс-изомеры конечного продукта.
Дозировка [ править ]
4-метиламинорекс можно курить, вдыхать или принимать внутрь.
В качестве Анорексического , то ED50 составляет 8,8 мг / кг у крыс для (±) - цис - изомеров. (±) - транс- изомеры несколько более эффективны при концентрации 7,0 мг / кг. В качестве рекреационного препарата эффективная дозировка составляет от 5 до 25 мг. [6]
В 1970-х McNeil Laboratories , Inc. пыталась вывести 4-метиламинорекс на рынок лекарств в качестве симпатомиметика (наиболее часто используемого в качестве лекарств от астмы), название исследования было McN-822, они упоминали, что доза для человека была бы 0,25 мг / кг. веса тела. Они также упоминают LD50: 17 мг / кг перорально для мышей [7]
Существует патент на использование 4-метиламинорекса «в качестве назального противозастойного средства, которое при пероральном введении не оказывает неблагоприятного стимулирующего действия на центральную нервную систему, как это происходит с другими противоотечными средствами и анорексантами». Указанная доза составляет 0,25 мг / кг массы тела. [8]
Эффекты [ править ]
Он оказывает продолжительное действие, обычно до 16 часов при пероральном приеме и до 12 часов при курении или инсуффляции . По некоторым данным, большие дозы могут длиться до 36 часов. Эффекты носят стимулирующий характер, вызывают эйфорию , повышенное внимание и познавательные способности . Как ни странно, было сообщено, что он производит эффекты, аналогичные ноотропам . Однако нет исследований, подтверждающих утверждение о том, что он отличается от других психостимуляторов или более эффективен в этом отношении. Более того, 4-метиламинорекс не имеет установленного профиля безопасности широко используемых клинических психостимуляторов, таких как метилфенидат и декстроамфетамин..
| Время (ч) | Концентрация 4-метиламинорекса в моче (мкг / мл) |
|---|---|
| 0-6 | 45 |
| 6-24 | 1.0 |
| 24–36 | 0,1 |
| 36-48 | не обнаружен |
Сообщается об одной смерти из-за 4-метиламинорекса и диазепама. Концентрации 4-метиламинорекса составляли: в крови 21,3 мг / л; в моче 12,3 мг / л. Концентрация диазепама в крови составляла 0,8 мг / л. [9] В одном эксперименте на крысах изучалось выделение 4-метиламинорекса с мочой: «Концентрация транс-4-метиламинорекса в моче крысы после четырех инъекций транс-4S, 5S-изомера по 5 мг / кг внутрибрюшинно с интервалами 12 ч за 2 дня, согласно количественному измерению с помощью ГХ / МС ». [10]
Другое исследование было сосредоточено на фармакокинетике и тканевом распределении стереоизомеров 4-метиламинорекса у крыс. [11]
«Легочная гипертензия была связана с приемом подавляющего аппетит средства аминорекс. Подобное соединение, 4-метиламинорекс, было обнаружено у трех человек с диагнозом легочная гипертензия». [12]
Исследования нейротоксичности [ править ]
Было проведено три исследования, изучающих возможную нейротоксичность 4-метиламинорекса. Первое исследование [13] с использованием довольно высоких доз (самая высокая доза вызвала клонические судороги, и некоторые крысы умерли) на крысах и изучение краткосрочных эффектов (крысы были умерщвлены от 30 минут до 18 часов после инъекции 5, 10 или 20 мг / кг рацемата. цис-4-метиламинорекс) предположил снижение активности триптофангидроксилазы (TPH) (возможный маркер нейротоксичности серотонина), но со ссылкой на исследование: «Через 30 минут после инъекции изменений в активности TPH не наблюдалось; через 8 часов активность этого фермента, по-видимому, снизилась. выздоравливает ". и «этот агент значительно менее нейротоксичен, чем метамфетамин или МДМА ».
В исследовании [14], опубликованном на 2 года позже первого, также предполагалось снижение активности триптофангидроксилазы, они также использовали довольно высокие дозы (10 мг / кг цис-4-метиламинорекса) и изучали также долгосрочные эффекты (крысы были убиты 3 ч, 18 ч или 7 дней после инъекции), они обнаружили снижение активности триптофангидроксилазы (ТПГ) на 20-40% и «восстановление активности ТПГ произошло через 18 ч после лечения, но снова значительно снизилось к 7 дню». но «Примечательно, что, в отличие от других аналогов, уровни 5-HT в полосатом теле не снижались с активностью TPH после многократного лечения 4-метиламинорексом»
В последнем исследовании [15] (с использованием мышей) не было обнаружено каких-либо долгосрочных эффектов, предполагающих нейротоксичность, и вместо этого было обнаружено повышение уровня серотонина, они также использовали высокие дозы (15 мг / кг каждого изученного изомера). в настоящих экспериментах примерно в 6-10 раз превышают эффективные дозы аминорекса и стереоизомеров при ингибировании приема пищи ». Дозы повторяли 3 раза в день, и мышей умерщвляли через 7 дней после последней дозы. «Поскольку длительное истощение дофамина или 5-HT, по-видимому, является хорошим предиктором нейротоксичности дофамина или 5-HT (Wagner et al. 1980; Ricaurte et al. 1985), результаты показывают, что соединения аминорекса, за исключением 4S, 5S-диметиламинорекс , в отличие от МДМА илифенфлурамин не токсичен ни для дофамина, ни для систем нейротрансмиттеров 5-HT у мышей CBA . Сообщалось, что, хотя многократные дозы 4-метиламинорекса вызывали долгосрочное (7 дней) снижение активности триптофангидроксилазы в полосатом теле у крыс SD, не было обнаружено никаких изменений в уровнях 5-HT и 5-HIAA (Hanson et al. 1992). [12]
Это первое исследование [11] также предполагало снижение уровня дофамина (DA) (возможный маркер нейротоксичности дофамина), но со ссылкой на исследование: «Однако через 8 часов после введения лекарства не было обнаружено отличий от контрольных значений в уровнях DA , DOPAC или HVA . " и снова более поздние исследования [12-13] не обнаружили какого-либо долгосрочного снижения.
Правовой статус [ править ]
Австралия [ править ]
В Австралии 4-метиламинорекс внесен в Список 9, что делает его разрешенным только для научных и медицинских исследований. [16]
Канада [ править ]
В Канаде 4-метиламинорекс внесен в Список III. [17]
Нидерланды [ править ]
В Нидерландах аминорекс (4-метиламинорекс - дизайнерский препарат 2014 г.) включен в Список I Закона об опиуме . [18] Он не одобрен CBG, и поэтому признан непригодным для использования в медицинских целях.
Соединенное Королевство [ править ]
В Соединенном Королевстве 4-метиламинорекс указан как класс А. [19]
Соединенные Штаты [ править ]
В Соединенных Штатах (±) - цис- 4-метиламинорекс был помещен в Список I Закона о контролируемых веществах вскоре после его появления в качестве рекреационного наркотика в середине 1980-х годов. [20] Производство транс- изомера требовало процесса, отличного от тех, которые использовались при первом включении вещества, и считалось менее эффективным, чем цис- изомер, с гораздо более низким потенциалом злоупотребления. Тем не менее, исследования, раскрывающие потенциал злоупотребления «транс» изомером, [ необходима ссылка ] в сочетании с разработкой новых подпольных методов синтеза, которые могли бы производить транс [ необходима ссылка ]создали потенциальную лазейку в законе, которая охватывает только цис-изомер. Чтобы прояснить ситуацию, Управление по борьбе с наркотиками США опубликовало в своем DEA Microgram Journal статью , касающуюся интерпретации соответствующего статутного закона в части статуса транс- 4-метиламинорекса. Таким образом, в соответствии с этим решением, не имеющим обязательной юридической силы, транс- 4-метиламинорекс в настоящее время не является контролируемым веществом, а является его потенциальным аналогом. Фактически, в отчете прямо говорится:
[Управление по борьбе с наркотиками] США придерживается следующего мнения о законности позиционного изомера «транс» -4-метиламинорекс, который, в отличие от его «цис-изомера», никогда не включался в какой-либо перечень в соответствии с Законом о контролируемых веществах .
Однако в заключении говорится, что агентство считает вещество потенциальным аналогом контролируемого вещества , что делает это вещество идентичным веществу Списка I, если оно предназначено для потребления человеком, в соответствии с Федеральным законом об аналогах . В отчете содержится отчет об успешном осуждении в соответствии с Федеральным законом об аналогах за преступление, связанное с транс- изомером. [21]
Флорида [ править ]
«2-амино-4-метил-5-фенил-2-оксазолин (4-метиламинорекс)» и «любой материал, соединение, смесь или препарат, которые содержат любое количество« этого »или которые содержат любую из [его] солей , изомеры, включая оптические, позиционные или геометрические изомеры, и соли изомеров, если существование таких солей, изомеров и солей изомеров возможно », является контролируемым веществом Списка I в штате Флорида, что делает его незаконным приобретение, продавать или владеть во Флориде. [22]
См. Также [ править ]
- Список аналогов аминорекса
- 4,4'-диметиламинорекс
- Аминорекс
- Кломинорекс
- Циклазодон
- Фенозолон
- Флуминорекс
- Пемолин
- Тозалинон
Ссылки [ править ]
- ^ US 3278382 , « Композиции 2-амино-5-арилоксазолина и способы их использования»
- ^ Гленнон RA, Misenheimer B (март 1990). «Стимулирующие свойства нового дизайнерского препарата: 4-метиламинорекс (« U4Euh »)». Фармакология, биохимия и поведение . 35 (3): 517–21. DOI : 10.1016 / 0091-3057 (90) 90282-M . PMID 1971111 . S2CID 10464868 .
- Перейти ↑ Young R (май 1992 г.). «Аминорекс оказывает стимулирующее действие, подобное амфетамину, но в отличие от фенфлурамина». Фармакология, биохимия и поведение . 42 (1): 175–8. DOI : 10.1016 / 0091-3057 (92) 90462-O . PMID 1356272 . S2CID 31002190 .
- ^ Young R, Гленнон RA (май 1993). «Обобщение кокаинового стимула на два новых дизайнерских наркотика: меткатинон и 4-метиламинорекс». Фармакология, биохимия и поведение . 45 (1): 229–31. DOI : 10.1016 / 0091-3057 (93) 90110-F . PMID 8516363 . S2CID 7648152 .
- ^ Mansbach RS, Sannerud CA, Гриффитс RR, RL Balster, Harris LS (октябрь 1990). «Внутривенное самостоятельное введение 4-метиламинорекса приматам». Наркотическая и алкогольная зависимость . 26 (2): 137–44. DOI : 10.1016 / 0376-8716 (90) 90120-4 . PMID 2242714 .
- ^ «Эровид 4-метиламинорекс Хранилище: Дозировка» .
- ^ "Время ожидания системы истекло (онлайн-каталог Библиотеки Конгресса)" .
- ^ "Метод снятия заложенности носа ... - Патенты Google" .
- Перейти ↑ Davis FT, Brewster ME (март 1988). «Погиб с участием U4Euh, циклического производного фенилпропаноламина». Журнал судебной медицины . 33 (2): 549–53. DOI : 10,1520 / JFS11971J . PMID 3373171 .
- ^ Канкаанпяя А, Meririnne Е, Ellermaa S, Ariniemi К, Сеппала Т (сентябрь 2001 г.). «Обнаружение и анализ цис- и транс-изомеров 4-метиламинорекса в образцах мочи, плазмы и тканей». Международная криминалистическая экспертиза . 121 (1–2): 57–64. DOI : 10.1016 / S0379-0738 (01) 00453-4 . PMID 11516888 .
- ^ Meririnne Е, Ellermaa S, Канкаанпяя А, барды А, Сеппала Т (июнь 2004 г.). «Фармакокинетика и тканевое распределение стереоизомеров 4-метиламинорекса у крыс». Журнал фармакологии и экспериментальной терапии . 309 (3): 1198–205. DOI : 10,1124 / jpet.103.060053 . PMID 14742748 . S2CID 28124406 .
- ^ а б Гейн С.П., Рубин Л.Дж., Кметцо Дж.Дж., Палевский Х.И., Трэйл Т.А. (ноябрь 2000 г.). «Рекреационное применение аминорекса и легочной гипертензии» . Сундук . 118 (5): 1496–7. DOI : 10,1378 / chest.118.5.1496 . PMID 11083709 . Архивировано из оригинала на 2013-01-12.
- ^ Бункер CF, Джонсон М, Гибб JW, Буш LG, Hanson GR (май 1990). «Нейрохимические эффекты острого лечения 4-метиламинорексом: новый стимулятор злоупотребления». Европейский журнал фармакологии . 180 (1): 103–11. DOI : 10.1016 / 0014-2999 (90) 90597-Y . PMID 1973111 .
- ^ Hanson GR, Бункер CF, Johnson M, L Bush, Гибб JW (август 1992). «Ответ моноаминергической и нейропептидной систем на 4-метиламинорекс: новый стимулятор злоупотребления». Европейский журнал фармакологии . 218 (2–3): 287–93. DOI : 10.1016 / 0014-2999 (92) 90181-3 . PMID 1358636 .
- Перейти ↑ Zheng Y, Russell B, Schmierer D, Lavernity R (январь 1997 г.). «Влияние аминорекса и родственных соединений на моноамины и метаболиты мозга мышей CBA». Журнал фармации и фармакологии . 49 (1): 89–96. DOI : 10.1111 / j.2042-7158.1997.tb06758.x . PMID 9120777 . S2CID 20224300 .
- ^ "Стандарт ядов 2009" . Проверено 2 сентября 2009 .
- ^ "Закон о контролируемых наркотиках и веществах" . Проверено 2 сентября 2009 .
- ^ "Bijlage 1 Lijst I Opiumwetmiddelen" . Архивировано из оригинала на 2009-06-25 . Проверено 2 сентября 2009 .
- ^ «СПИСОК ЛЕКАРСТВЕННЫХ СРЕДСТВ, КОНТРОЛИРУЕМЫХ В НАСТОЯЩЕЕ ВРЕМЯ КЛАССА А» (PDF) . Проверено 2 сентября 2009 .
- ^ «Раздел 1308.11 Приложение I» . Архивировано 27 августа 2009 года . Проверено 2 сентября 2009 .
- ^ Синтез транс-4-метиламинорекса из норэфедрина и цианата калия (DEA Microgram Journal). Архивировано 30 сентября 2007 г. на Wayback Machine.
- ↑ Законодательство Флориды - Глава 893 - ПРОФИЛАКТИКА И КОНТРОЛЬ ЗЛОУПОТРЕБЛЕНИЯ НАРКОТИКАМИ
Внешние ссылки [ править ]
- Хранилище 4-метиламинорексов Эровида