Аммиак - одно из самых производимых неорганических химикатов. Существуют многочисленные крупные производства аммиака заводы по всему миру, производя в общей сложности 144 миллионов тонн азота ( что эквивалентно 175 млн т аммиака) в 2016 году [1] Китай произвел 31,9% мирового производства, а затем России с 8,7% , Индия - 7,5% и США - 7,1%. 80% или более производимого аммиака используется для удобрения сельскохозяйственных культур. Аммиак также используется для производства пластмасс, волокон, взрывчатых веществ, азотной кислоты (посредством процесса Оствальда ) и промежуточных продуктов для красителей и фармацевтических препаратов.
История [ править ]
Перед началом Первой мировой войны большая часть аммиака была получена путем сухой перегонки азотистых продуктов растительного и животного происхождения; восстановление азотистой кислоты и нитритов с водородом ; а также разложением солей аммония щелочными гидроксидами или негашеной известью , наиболее часто используемой солью является хлорид ( сали-аммиак ).
Сегодня большая часть аммиака производится в больших масштабах по технологии Хабера с производительностью до 3300 тонн в день. В этом процессе газы N 2 и H 2 могут реагировать при давлении 200 бар.
Современные заводы по производству аммиака [ править ]
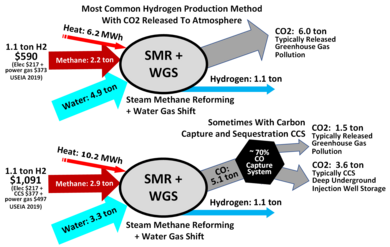
Типичная современная установка по производству аммиака сначала преобразует природный газ , сжиженный нефтяной газ или нефтяную нафту в газообразный водород . Способ получения водорода из углеводородов известен как паровой риформинг . [2] Затем водород объединяется с азотом для получения аммиака с помощью процесса Габера-Боша .
Начиная с исходного природного газа, для производства водорода используются следующие процессы:
- Первым этапом процесса является удаление соединений серы из сырья, поскольку сера дезактивирует катализаторы, используемые на последующих этапах. Удаление серы требует каталитического гидрирования для превращения соединений серы в исходном сырье в газообразный сероводород :
- H 2 + RSH → RH + H 2 S (газ)
- Затем газообразный сероводород адсорбируется и удаляется, пропуская его через слои оксида цинка, где он превращается в твердый сульфид цинка :
- Н 2 S + ZnO → ZnS + H 2 O
- Затем используется каталитический паровой риформинг сырья, не содержащего серы, для образования водорода плюс монооксида углерода :
- СН 4 + Н 2 О → СО + 3Н 2
- На следующем этапе используется преобразование каталитического сдвига для преобразования моноксида углерода в диоксид углерода и больше водорода:
- СО + Н 2 О → СО 2 + Н 2
- Затем диоксид углерода удаляют либо абсорбцией водными растворами этаноламина, либо адсорбцией в адсорберах с переменным давлением (PSA) с использованием запатентованных твердых адсорбционных сред.
- Последним шагом в производстве водорода является использование каталитического метанирования для удаления любых небольших остаточных количеств монооксида углерода или диоксида углерода из водорода:
- CO + 3H 2 → CH 4 + H 2 O
- СО 2 + 4Н 2 → СН 4 + 2Н 2 О
Для получения желаемого конечного продукта аммиака водород затем каталитически реагирует с азотом (полученным из технологического воздуха) с образованием безводного жидкого аммиака. Этот этап известен как цикл синтеза аммиака (также называемый процессом Габера-Боша ):
- 3Н 2 + N 2 → 2NH 3
Из-за природы катализатора (обычно с множественным промотированием магнетита), используемого в реакции синтеза аммиака, при синтезе могут быть допустимы только очень низкие уровни кислородсодержащих (особенно CO, CO 2 и H 2 O) соединений (водород и азотная смесь) газ. Относительно чистый азот можно получить путем разделения воздуха , но может потребоваться дополнительное удаление кислорода.
Из-за относительно низких степеней конверсии за один проход (обычно менее 20%) требуется большой поток рециркуляции. Это может привести к накоплению инертных газов в петлевом газе.
Каждая из стадий парового риформинга, сдвигового преобразования, удаления диоксида углерода и метанирования работает при абсолютном давлении примерно от 25 до 35 бар, а контур синтеза аммиака работает при абсолютном давлении в диапазоне от 60 до 180 бар в зависимости от используемой запатентованной конструкции. Есть много инженерных и строительных компаний, которые предлагают собственные разработки для установок синтеза аммиака. Хальдор Топсе из Дании, Thyssenkrupp Industrial Solutions GmbH из Германии, Ammonia Casale из Швейцарии и Kellogg Brown & Root из США являются одними из наиболее опытных компаний в этой области.
Устойчивое производство аммиака [ править ]
Производство аммиака зависит от обильных запасов энергии , в основном природного газа . Из-за критической роли аммиака в интенсивном сельском хозяйстве и других процессах желательно устойчивое производство. Это возможно за счет экологически чистого пиролиза метана или получения водорода путем электролиза воды (или пара) с использованием электроэнергии с нулевым выбросом углерода из возобновляемых источников энергии или ядерной энергетики .
Это было бы просто в водородной экономике, если бы часть производства водорода была переключена с топлива на использование сырья. Например, в 2002 году Исландия произвела 2 000 тонн газообразного водорода путем электролиза , используя избыточное производство электроэнергии на своих гидроэлектростанциях , в первую очередь для производства аммиака для удобрений. [3] Веморк ГЭС в Норвегии использовал его излишки выработки электроэнергии для генерации возобновляемой азотной кислоты с 1911 по 1971, [4] требует 15 МВт · ч / т азотной кислоты. Та же реакция осуществляется молнией, обеспечивая естественный источник для преобразования атмосферного азота в растворимые нитраты. [5]На практике природный газ останется основным источником водорода для производства аммиака до тех пор, пока он будет самым дешевым .
Сточные воды часто содержат много аммиака. Поскольку сброс воды, содержащей аммиак, в окружающую среду, даже на очистных сооружениях, может вызвать проблемы, нитрификация часто необходима для удаления аммиака. [6] Это может стать потенциально устойчивым источником аммиака в будущем из-за его большого количества и необходимости в любом случае удалять его из воды . [7] В качестве альтернативы аммиак из сточных вод направляют в электролизер аммиака (электролиз аммиака), работающий с возобновляемыми источниками энергии (солнечные фотоэлектрические и ветряные турбины) для производства водорода и чистой очищенной воды. [8] Электролиз аммиака может потребовать гораздо меньше термодинамической энергии, чем электролиз воды (всего 0,06 В в щелочной среде).[9]
Другим вариантом извлечения аммиака из сточных вод является использование механизма цикла термической абсорбции аммиак-вода. [10] [11] Используя этот вариант, аммиак может быть извлечен в виде жидкости или гидроксида аммония. Преимущество первого состоит в том, что с ним намного легче обращаться и транспортировать, тогда как последний также имеет коммерческую ценность, когда производится 30-процентная концентрация гидроксида аммония в растворе.
Побочные продукты [ править ]
Одним из основных промышленных побочных продуктов производства аммиака является CO 2 . В 2018 году высокие цены на нефть привели к длительной летней остановке европейских заводов по производству аммиака, что привело к коммерческой нехватке CO 2 , что ограничило производство газированных напитков, таких как пиво и газированные безалкогольные напитки. [12]
См. Также [ править ]
- Очистка аминового газа
- Процесс Габера
- Водородная экономика
- Пиролиз метана
Ссылки [ править ]
- ^ Публикация Геологической службы США
- ^ Твигг, Мартин В. (1989). Справочник по катализаторам (2-е изд.). Издательство Оксфордского университета. ISBN 978-1-874545-36-1.
- ^ «Исландия запускает энергетическую революцию» . Новости BBC. 2001-12-24. Архивировано из оригинального 7 -го апреля 2008 года . Проверено 23 марта 2008 .
- ^ Брэдли, Дэвид (2004-02-06). «Великий потенциал: Великие озера как региональный возобновляемый источник энергии» (PDF) . Архивировано из оригинального (PDF) 29 октября 2008 года . Проверено 4 октября 2008 .
- ^ Карл Фишер; Уильям Э. Ньютон (2002). Дж. Дж. Ли (ред.). Фиксация азота в тысячелетии . Эльзевир. стр. 2 -3. ISBN 978-0-444-50965-9.
- ^ http://www.waterworld.com/articles/print/volume-26/issue-3/editorial-features/addressing-the-challenge.html
- ^ Хуанг, Цзяньинь; Канканамге, Надика Ратнаяке; Чоу, Кристофер; Валлийский, Дэвид Т .; Ли, Тяньлинь; Тисдейл, Питер Р. (январь 2018 г.). «Удаление аммония из воды и сточных вод с помощью экономичных адсорбентов: обзор». Журнал наук об окружающей среде . 63 : 174–197. DOI : 10.1016 / j.jes.2017.09.009 . PMID 29406102 .
- ^ Мутувел, Мадхиванан; Ботте, Жерардин G (2009). «Тенденции электролиза аммиака». Современные аспекты электрохимии, № 45 . Современные аспекты электрохимии. 45 . С. 207–245. DOI : 10.1007 / 978-1-4419-0655-7_4 . ISBN 978-1-4419-0654-0.
- ^ Gwak, Jieun; Чоун, Мёнхун; Ли, Джэён (февраль 2016 г.). «Электролиз щелочного аммиака на электроосажденной платине для контролируемого производства водорода». ChemSusChem . 9 (4): 403–408. DOI : 10.1002 / cssc.201501046 . PMID 26530809 .
- ^ Лин, П .; Wang, RZ; Ся, ZZ; Ма, К. (июнь 2011 г.). «Аммиачно-водопоглощающий цикл: перспективный способ транспортировки низкопотенциальной тепловой энергии на большие расстояния» . Международный журнал низкоуглеродных технологий . 6 (2): 125–133. DOI : 10,1093 / ijlct / ctq053 .
- ^ Шокати, Насер; Ханахмадзаде, Салах (август 2018 г.). «Влияние различных комбинаций аммиачно-водяных циклов Ренкина и абсорбционных холодильных циклов на эксергоэкономические характеристики когенерационного цикла». Прикладная теплотехника . 141 : 1141–1160. DOI : 10.1016 / j.applthermaleng.2018.06.052 .
- ^ «Именно поэтому у нас заканчивается CO2 для производства пива и мяса» . iNews . 2018-06-28.
Внешние ссылки [ править ]
- Современная промышленность по производству водорода
- Энергопотребление и энергоемкость химической промышленности США , отчет LBNL-44314, Национальная лаборатория Лоуренса Беркли (прокрутите вниз до страницы 39 из 40 страниц PDF, чтобы просмотреть список заводов по производству аммиака в Соединенных Штатах)
- Аммиак: следующий шаг включает подробную схему технологического процесса .
- Краткая технологическая схема завода по производству аммиака с тремя элементами управления.