Участие соседних групп ( NGP ) (также известное как анхимерная помощь ) в органической химии было определено IUPAC как взаимодействие реакционного центра с неподеленной парой электронов в атоме или электронами, присутствующими в сигма-связи или пи-связи, содержащейся внутри родительская молекула, но не конъюгированная с реакционным центром. [1] [1] [2] [3] Когда NGP работает, скорость реакции увеличивается. Также возможно для стереохимииреакции быть ненормальной (или неожиданной) по сравнению с нормальной реакцией. Хотя соседние группы могут влиять на многие реакции в органической химии ( например, реакция диена, такого как 1,3-циклогексадиен, с малеиновым ангидридом, обычно дает эндо-изомер из-за вторичного эффекта {перекрытие π-орбиталей карбонильной группы с переходное состояние в реакции Дильса-Альдера }) эта страница ограничена эффектами соседних групп, наблюдаемыми с карбокатионами и реакциями S N 2.
NGP по одиночным парам гетероатомов [ править ]
Классическим примером NGP является реакция иприта серы или азота с нуклеофилом , скорость реакции намного выше для иприта серы и нуклеофила, чем для первичного хлористого алкила без гетероатома .
Ph-S-CH 2 -CH 2 -Cl реагирует с водой в 600 раз быстрее, чем CH 3 -CH 2 -CH 2 -Cl.
NGP от алкена [ править ]
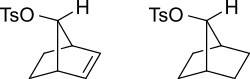
Π-орбитали алкена могут стабилизировать переходное состояние , помогая делокализовать положительный заряд карбокатиона . Например, ненасыщенный тозилат будет реагировать быстрее (в 10–11 раз быстрее для водного сольволиза) с нуклеофилом, чем насыщенный тозилат.
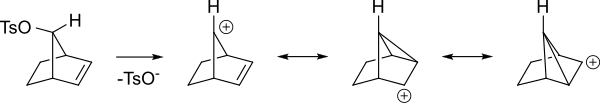
Карбокатионный промежуточный продукт будет стабилизирован резонансом, когда положительный заряд распространяется на несколько атомов. На схеме ниже это показано.
Вот другой взгляд на те же промежуточные звенья.
Даже если алкен находится дальше от реакционного центра, алкен все равно может действовать таким образом. Например, в следующем алкилбензолсульфонате алкен способен делокализовать карбокатион.
Кроме того , увеличение скорости от S Н реакции 2 из аллилового метила с нуклеофилом по сравнению с реакцией бромида н-пропил происходит потому , что орбитали перекрывания π связи с тем , из переходного состояния . В аллильной системе алкеновые орбитали перекрываются с орбиталями переходного состояния S N 2.
NGP циклопропаном, циклобутаном или гомоаллильной группой [ править ]
Если циклопропилметилхлорид взаимодействует с этанолом и водой, то получается смесь 48% циклопропилметилового спирта, 47% циклобутанола и 5% гомоаллилового спирта ( бут -3-енола). Это связано с тем, что карбокатионный промежуточный продукт делокализован на многих различных атомах углерода через обратимое отверстие в кольце.
NGP по ароматическому кольцу [ править ]
В случае бензилгалогенида реакционная способность выше, потому что переходное состояние S N 2 имеет эффект перекрытия, аналогичный таковому в аллильной системе.
Ароматическое кольцо может помочь в формировании карбокатионного промежуточного называется ион phenonium от делокализующих положительного заряда.
Когда следующий тозилат реагирует с уксусной кислотой при сольволизе, а не в простой реакции S N 2 с образованием B, была получена смесь A, B (которые являются энантиомерами) и C + D в соотношении 48: 48: 4 [2] [3] .
Механизм, образующий A и B, показан ниже.
NGP алифатическими CC или CH связями [ править ]
Алифатические связи CC или CH могут привести к делокализации заряда, если эти связи близки и антиперипланарны по отношению к уходящей группе. Соответствующие промежуточные соединения относятся к неклассическим ионам , причем наиболее известным случаем является 2-норборнильная система.
Внешние ссылки [ править ]
- Определение ИЮПАК
Ссылки [ править ]
- ^ де Rooij, JF; Wille-Hazeleger, G .; Бургерс, PM; ван Бум, Дж. Х. (1979). «Участие соседних групп в разблокировке фосфотриэфиров нуклеиновых кислот» . Исследования нуклеиновых кислот . 6 (6): 2237–2259. DOI : 10.1093 / NAR / 6.6.2237 . PMC 327848 . PMID 461188 .
- ^ Stalford, Susanne A .; Килнер, Колин А .; Лич, Эндрю Дж .; Тернбулл, В. Брюс (07.12.2009). «Участие соседних групп против добавления к ионам оксакарбения: исследования синтеза микобактериальных олигосахаридов». Органическая и биомолекулярная химия . Королевское химическое общество . 7 (23): 4842–4852. DOI : 10.1039 / B914417J . PMID 19907773 .
- ^ Боуден, Keith (1993-01-01). Бетелл, Д. (ред.). «Участие соседних групп карбонильных групп в гидролизе сложного эфира» . Academic Press, ScienceDirect . С. 171–206 . Проверено 17 декабря 2019 .
- ^ Продвинутая органическая химия, стр. 314, Джерри Марч (4-е изд.), Wiley-Interscience.
- ^ Исследования по стереохимии . И. Стереоспецифическое Вагнер-Меервейна Перегруппировка из изомеров 3-фенил-2-бутанол Donald J. Cram J. Am. Chem. Soc. ; 1949; 71 (12); 3863-3870. Абстрактный
- ^ Исследования по стереохимии. V. Ионные пары сульфоната фенония как промежуточные соединения во внутримолекулярных перегруппировках и реакциях сольволиза, которые происходят в системе 3-фенил-2-бутанола Donald J. Cram J. Am. Chem. Soc. ; 1952; 74 (9); 2129-2137Аннотация.