 | |
| Имена | |
|---|---|
| Название ИЮПАК дикадмий (2+) бис (тетрахоридоалюминат (1-)) | |
| Идентификаторы | |
| |
3D модель ( JSmol ) | |
| |
| |
| Характеристики | |
| Cd 2 [AlCl 4 ] 2 | |
| Молярная масса | 562,4123 г / моль |
| Появление | белый кристалл |
| Температура плавления | 227 ° (разл.) |
| Опасности | |
| NIOSH (пределы воздействия на здоровье в США): | |
PEL (Допустимо) | [1910.1027] TWA 0,005 мг / м 3 (как Cd) [1] |
REL (рекомендуется) | Ca [1] |
IDLH (Непосредственная опасность) | Ca [9 мг / м 3 (в виде Cd)] [1] |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
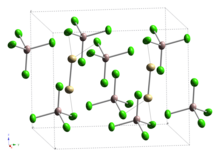
Кадмий (I) , тетрахлоралюминат представляет собой неорганическое соединение с формулой Cd 2 (AlCl 4 ) 2 , A тетрахлоралюминат из кадмия (I) . Это было первое сообщенное соединение (1961), которое содержало кадмий в степени окисления +1 и имеет связь кадмий-кадмий.
Подготовка и свойства [ править ]
Cd 2 (AlCl 4 ) 2 первоначально получали растворением металлического Cd в расплавленном CdCl 2 с последующим добавлением AlCl 3 . [2]
- CdCl 2 + Cd → Cd 2 Cl 2
- Cd 2 Cl 2 + 2 AlCl 3 → Cd 2 (AlCl 4 ) 2
Последующие исследования спектра комбинационных колебаний показали наличие связи кадмий – кадмий [3], что было подтверждено двумя отдельными рентгеноструктурными исследованиями монокристаллов. [4] [5] Таким образом, данное соединение можно сравнить с соединениями ртути (I) (ртутью) (такими как хлорид ртути (I) ), которые содержат Hg.2+
2. Связи Cd-Cd являются частью этана -кака Cd 2 Cl 6 единиц , разделяющих вершины с AlCl 4 единиц, с длиной Cd-Cd связей представлены как 257,6 м [4] или 256.1pm. [5]
Cd 2 (AlCl 4 ) 2 диамагнитен. Он не содержит неспаренных электронов и легко реагирует с водой, диспропорционируя с образованием металлического Cd и Cd 2+ .

Ссылки [ править ]
- ^ a b c Карманный справочник NIOSH по химической опасности. «# 0087» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Корбетт, JD; Буркхард, WJ; Друдинг, Л. Ф. (январь 1961 г.). «Стабилизация состояния окисления кадмия (I). Система Cd-Cd.1
2(AlCl
4)
2-CD2
(AlCl
4)
2». Журнал Американского химического общества . 83 (1):. 76-80 DOI : 10.1021 / ja01462a016 . - ↑ Corbett, JD (август 1962 г.). "Кадмий (I) Ион Cd2+
2. Рамановский спектр и связь с Hg2+
2». Неорганическая химия . 1 (3):. 700-703 DOI : 10.1021 / ic50003a051 . - ^ a b Faggiani, R .; Рональд Дж. Гиллеспи; Джон Э. Векрис (1986). «Ион кадмия (I), Cd2+
2; Рентгеновская кристаллическая структура Cd
2(AlCl
4)
2». Журнал химического общества, Chemical Communications . 1986 (7): 517-518. DOI : 10.1039 / C39860000517 . - ^ a b Staffel, T .; Доктор Герд Мейер (1987). «Синтез и кристаллические структуры Cd [AlCl
4]
2и Cd
2[AlCl
4]
2». Zeitschrift für anorganische унд Allgemeine Хеми . 548 (5):. 45-54 DOI : 10.1002 / zaac.19875480505 .