Молекулы, выделяющие монооксид углерода ( CORM ), представляют собой химические соединения, предназначенные для высвобождения контролируемых количеств монооксида углерода (CO). CORM разрабатываются как потенциальные терапевтические агенты для локальной доставки CO к клеткам и тканям, таким образом преодолевая ограничения протоколов ингаляции CO. [1]
CO наиболее известен своей токсичностью при отравлении оксидом углерода в высоких дозах. Однако СО входит в число эндогенных газообразных сигнальных молекул, и низкие дозы СО связаны с терапевтическими преимуществами. Доклинические исследования были сосредоточены на противовоспалительной активности CO со значительным применением при сердечно-сосудистых заболеваниях, онкологии, хирургии трансплантата и нейропротекции. [2]
Большая часть CO, продуцируемого у млекопитающих, возникает в результате разложения гема тремя изоформами гемоксигеназы , при этом HO-1 индуцируется окислительным стрессом , CO и множеством ксенобиотиков . [3] HO-2 и HO-3 являются составными. Другие эндогенные источники могут включать перекисное окисление липидов [4].
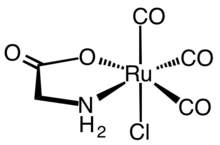
Ферментативная реакция гемоксигеназы вдохновила на разработку синтетических CORM. Первые синтетические CORM обычно представляли собой карбонильные комплексы металлов . Типичным CORM, который был широко охарактеризован как с биохимической, так и с фармакологической точки зрения, является комплекс рутения (II) Ru ( глицинат ) Cl (CO) 3 , широко известный как CORM-3.
Классификации CORM [ править ]
Самый простой источник CO - это реакция горения через источники горения, такие как ископаемое топливо или дрова . Источники, выделяющие CO при термическом разложении или сгорании, обычно не считаются CORM.
CORM с переходным металлом [ править ]
Большинство терапевтически значимых CORM представляют собой комплексы переходных металлов, в основном на основе железа , молибдена , рутения , марганца , кобальта и рения.
PhotoCORMs [ править ]
Высвобождение CO из агентов-носителей можно вызвать фотохимически. Эти носители называются фотоCORM и включают как комплексы металлов, так и не содержащие металлов ( органические ) соединения различных структурных мотивов, которые можно рассматривать как особый тип фотолабильной защитной группы .
ET-CORM [ править ]
CORM, запускаемые ферментами (ET-CORM), были разработаны для улучшения селективной локальной доставки CO. Некоторые пролекарства ET-CORM активируются ферментами эстеразы для сайт-специфического высвобождения CO. [5]
Органические CORM [ править ]
Органические небольшие молекулы разрабатываются для преодоления ограничений токсичности неорганических CORM. На основании предыдущих сообщений об образовании карбоксигемоглобина посредством метаболизма, метиленхлорид был первым органическим CORM, вводимым перорально . Второй органический CORM, CORM-A1 (боранокарбонат натрия), был разработан на основе отчета 1960-х годов о выделении CO из боранокарбоната калия.
В 2003 году циклические оксоуглероды были предложены в качестве источника терапевтического CO, включая дельтовую кислоту , квадратную кислоту , кроконовую кислоту и родизоновую кислоту и их соли.
Органические пролекарства CO [ править ]
В последние годы наблюдается рост интереса к органическим пролекарствам CO из-за необходимости учитывать вопросы разработки лекарственных средств при разработке терапевтических средств на основе CO (Ji, X; Damera, K .; Zheng, Y .; Yu, B .; Otterbein, LE; и Ван Б. «К терапевтическим средствам на основе окиси углерода: важнейшие вопросы доставки лекарств и разработки» J. Pharm. Sci. 2016, 105, 406-416. PMID: 26869408). Эти пролекарства CO имеют регулируемую скорость высвобождения, триггерное высвобождение и способность высвобождать более одной полезной нагрузки из одного пролекарства (Ji. X .; Wang, B. "Стратегии в отношении пролекарств органического окиси углерода" Acc. Chem. Res. 2018, 51, 1377-85. PMID: 29762011).
Ферментные гибриды [ править ]
На основе синергизма системы гемоксигеназы и доставки CO возник новый класс молекулярных гибридных CORM (HYCO), состоящий из соединенного индуктора HO-1 и частиц CORM. Один из таких HYCO включает диметилфумаратный фрагмент, который активирует NRF2, чтобы тем самым индуцировать HO-1, в то время как CORM-фрагмент также высвобождает CO.
Материалы, выделяющие окись углерода [ править ]
Материалы, выделяющие монооксид углерода (CORMA), представляют собой по существу новые лекарственные формы и платформы доставки лекарств, которые появились для преодоления фармацевтических ограничений большинства видов CORM. [6] Типичный CORMA, разработанный Hubbell, состоит из состава мицелл, полученных из триблок- сополимеров с CORM-структурой, высвобождение которой запускается добавлением цистеина . Другие CO-рилизинг каркасы включают в себя полимеры , пептиды , диоксид кремния наночастицы , наноалмаза , магнитные наночастицы , наноматериал гель, металло дендримеров, и конъюгаты CORM-белок (макромолекула). [7] [8]
Инфузия карбоксигемоглобина [ править ]
Карбоксигемоглобин может быть введен для доставки CO. Наиболее распространенные подходы основаны на использовании бычьего карбоксигемоглобина, связанного с полиэтиленгликолем (ПЭГ), и карбоксигемоглобина человека, конъюгированного с малеимидом и ПЭГ.
Порфирины [ править ]
Порфириновые структуры, такие как гем , гемин и аналоги металлического протопорфирина IX (PPIX) (такие как PPIX кобальта), используются для индукции гемоксигеназы и впоследствии подвергаются биотрансформации с высвобождением CO, неорганического иона и биливердина / билирубина . [9] Некоторые аналоги PPIX, такие как PPIX олова, мезопорфирин олова и PPIX цинка , являются ингибиторами гемоксигеназы .
Эндогенный CO [ править ]
В конце 1960-х Тенхунен продемонстрировал ферментативную реакцию катаболизма гема [10], тем самым идентифицировав фермент гемоксигеназу (HO). HO является основным источником эндогенного образования CO, хотя в последние годы были выявлены и другие второстепенные источники. CO образуется в организме человека со скоростью 16,4 мкмоль / час, ~ 86% происходит из гема через гемоксигеназу и ~ 14% из негемовых источников, включая фотоокисление, перекисное окисление липидов и ксенобиотики. [11] Средний уровень карбоксигемоглобина (CO-Hb) у некурящих составляет от 0,2% до 0,85% CO-Hb (тогда как у курильщика может быть от 4% до 10% CO-Hb), [12] хотя географическое положение , род занятий, здоровье и поведение являются дополнительными переменными.
Ферменты [ править ]
Гемоксигеназа [ править ]
Гемоксигеназа (HO) - гемосодержащий член семейства белков теплового шока (HSP), идентифицированный как HSP32 . На сегодняшний день идентифицированы три изоформы HO, включая индуцированный стрессом HO-1 и конститутивные HO-2 и HO-3. НО-1 считается белком, спасающим клетки, который индуцируется в ответ на окислительный стресс и многочисленные болезненные состояния. Кроме того, HO-1 индуцируется бесчисленным количеством молекул, включая статины , гемин и натуральные продукты . [13]
НО катализирует разложение гема до биливердина / билирубина , иона двухвалентного железа и CO. Хотя H2O присутствует во всем организме, он обладает значительной активностью в селезенке по деградации гемоглобина во время рециркуляции эритроцитов (0,8% пула эритроцитов в день), что на него приходится ~ 80% эндогенного производства CO, происходящего из гема. Большая часть оставшихся 20% продукции CO, производного от гема, связана с печеночным катаболизмом гемопротеинов ( миоглобина , цитохромов , каталазы , пероксидазы , растворимой гуанилатциклазы , синтазы оксида азота.) и неэффективный эритропоэз в костном мозге . [14] [15]
Перекисное окисление липидов [ править ]
Об образовании CO в результате перекисного окисления липидов впервые сообщили в конце 1960-х годов, и он считается второстепенным фактором эндогенного образования CO. [16] [17]
Фармакология CO [ править ]
Окись углерода является одной из трех газообразных сигнальных молекул наряду с оксидом азота и сероводородом . Эти газы в совокупности называются газопередатчиками .
Сигнализация [ править ]
Первое свидетельство CO в качестве сигнальной молекулы происходит при наблюдении СО стимулирующего растворимую гуанилатциклазу и последующего циклического гуанозинмонофосфата производства (цГМФ) , чтобы служить в качестве сосудорасширяющего в сосудистых гладкомышечных клеток . [18] В противовоспалительные эффекты СО приписаны к активации р38 митоген-активируемой протеинкиназы (МАРК) пути. Хотя CO обычно взаимодействует с атомом железа гема в гемопротеине , было продемонстрировано, что CO активирует кальций-зависимые калиевые каналы, вступая в водородные связи с поверхностными остатками гистидина.
CO оказывает ингибирующее действие на многие белки, включая цитохром P450 [19] и цитохром с оксидазу.
CO является модулятором ионных каналов, оказывая как возбуждающее, так и ингибирующее действие на многие классы ионных каналов, таких как потенциалзависимые кальциевые каналы .
Распространение [ править ]
CO имеет примерно в 210 раз большее сродство к гемоглобину, чем кислород . [20] Константа равновесной диссоциации реакции Hb-CO ⇌ Hb + CO сильно благоприятствует комплексу CO, поэтому высвобождение CO для легочной экскреции занимает некоторое время.
Основываясь на этой аффинности связывания, кровь по существу является необратимым стоком CO и представляет собой терапевтическую проблему для доставки CO к клеткам и тканям.
Метаболизм [ править ]
CO считается инертным в организме и в первую очередь выводится из легких и окисляется менее чем на 10%. [21]
Ссылки [ править ]
- ^ Motterlini R, Otterbein LE (сентябрь 2010). «Лечебный потенциал окиси углерода». обзорная статья. Обзоры природы. Открытие наркотиков . 9 (9): 728–43. DOI : 10.1038 / nrd3228 . PMID 20811383 .
- ↑ Махан В.Л. (декабрь 2012 г.). «Нейропротекторные, нейротерапевтические и нейрометаболические эффекты окиси углерода» . обзорная статья. Медицинские газовые исследования . 2 (1): 32. DOI : 10,1186 / 2045-9912-2-32 . PMC 3599315 . PMID 23270619 .
- ^ Ferrándiz ML, Девеса I (2008). «Индукторы гемоксигеназы-1». обзорная статья. Текущий фармацевтический дизайн . 14 (5): 473–86. DOI : 10,2174 / 138161208783597399 . PMID 18289074 .
- ^ Уилкинсон WJ, Кемп PJ (июль 2011). «Окись углерода: новый регулятор ионных каналов» . обзорная статья. Журнал физиологии . 589 (Pt 13): 3055–62. DOI : 10.1113 / jphysiol.2011.206706 . PMC 3145923 . PMID 21521759 .
- ^ Различная конструкция молекул, выделяющих CO (ET-CORM), запускаемых ферментами, выявляет количественные различия в биологической активности с точки зрения токсичности и воспаления. Stamellou E, Storz D, Botov S, Ntasis E, Wedel J, Sollazzo S, Krämer BK, van Son W., Seelen M, Schmalz HG, Schmidt A, Hafner M, Yard BA, Redox Biol. 2014 5 июня; 2: 739-48. DOI: 10.1016 / j.redox.2014.06.002. Электронная коллекция 2014 г.
- ^ Heinemann SH, Хоши Т, Вестерхаузен М, Шиллер А (апрель 2014). «Окись углерода - физиология, обнаружение и контролируемое высвобождение» . обзорная статья. Chemical Communications (Кембридж, Англия) . 50 (28): 3644–60. DOI : 10.1039 / c3cc49196j . PMC 4072318 . PMID 24556640 .
- ↑ Nguyen D, Boyer C (сентябрь 2015 г.). «Каркасы из макромолекулярных и неорганических наноматериалов для доставки монооксида углерода: последние разработки и будущие тенденции». обзорная статья. ACS Biomaterials Science & Engineering . 1 (10): 895–913. DOI : 10.1021 / acsbiomaterials.5b00230 .
- ^ Kautz AC, Кунц PC, Janiak C (ноябрь 2016). «Системы конъюгатов CO-высвобождающей молекулы (CORM)» . обзорная статья. Сделки Дальтона . 45 (45): 18045–18063. DOI : 10.1039 / c6dt03515a . PMID 27808304 .
- ^ Maines MD (июль 1988). «Гемоксигеназа: функция, множественность, регуляторные механизмы и клиническое применение». обзорная статья. Журнал FASEB . 2 (10): 2557–68. DOI : 10.1096 / fasebj.2.10.3290025 . PMID 3290025 . S2CID 22652094 .
- ^ Tenhunen R, Marver HS, Schmid R (декабрь 1969). «Микросомальная гемоксигеназа. Характеристика фермента». основная статья. Журнал биологической химии . 244 (23): 6388–94. PMID 4390967 .
- ^ Ван Р, изд. (2001). Окись углерода и сердечно-сосудистые функции . обзорная статья (первое изд.). CRC Press. п. 5. ISBN 978-1-4200-4101-9.
- Перейти ↑ Thom SR (2008). «Глава 15: Патофизиология и лечение угарного газа». В Neuman TS, Thom SR (ред.). Физиология и медицина гипербарической оксигенотерапии . обзорная статья. С. 321–347. DOI : 10.1016 / B978-1-4160-3406-3.50020-2 . ISBN 978-1-4160-3406-3.
- ^ Correa-Costa M, Otterbein LE (2014). «Ешьте, чтобы лечить: естественные индукторы системы гемоксигеназы-1». В Folkerts G, Garssen J (ред.). Фарма-Питание . обзорная статья. Успехи AAPS в серии фармацевтических наук. 12 . Спрингер, Чам. С. 243–256. DOI : 10.1007 / 978-3-319-06151-1_12 . ISBN 978-3-319-06150-4.
- ^ Lundh B, Johansson MB, Mercke C, Cavallin-Stahl E (декабрь 1972). «Повышение катаболизма гема за счет ограничения калорийности у человека». основная статья. Скандинавский журнал клинических и лабораторных исследований . 30 (4): 421–7. DOI : 10.3109 / 00365517209080280 . PMID 4639647 .
- ^ Breman HJ, Вонг RJ, Stevenson DK (30 октября 2001). «Глава 15: Источники, приемники и измерение окиси углерода». В Ван Р (ред.). Окись углерода и сердечно-сосудистые функции . обзорная статья (2-е изд.). CRC Press. ISBN 978-0-8493-1041-6.
- Перейти ↑ Wolff DG (декабрь 1976 г.). «Образование окиси углерода при перекисном окислении микросомальных липидов». основная статья. Сообщения о биохимических и биофизических исследованиях . 73 (4): 850–7. DOI : 10.1016 / 0006-291X (76) 90199-6 . PMID 15625852 .
- ^ Nishibayashi Н, Omma Т, Сато R, Эстабрук RW, Okunuki К, Камень MD, Sekuzu I, ред. (1968). Строение и функция цитохромов . обзорная статья. University Park Press. С. 658–665.
- ^ Ким HP, Ryter SW, Choi AM (2006). «СО как клеточная сигнальная молекула». обзорная статья. Ежегодный обзор фармакологии и токсикологии . 46 : 411–49. DOI : 10.1146 / annurev.pharmtox.46.120604.141053 . PMID 16402911 .
- Перейти ↑ Correia MA, Ortiz de Montellano PR (2005). «Ингибирование ферментов цитохрома Р450». Цитохром P450 . обзорная статья. Бостон, Массачусетс: Спрингер. С. 247–322. DOI : 10.1007 / 0-387-27447-2_7 . ISBN 978-0-306-48324-0.
- ↑ Блюменталь I (июнь 2001 г.). «Отравление угарным газом» . обзорная статья. Журнал Королевского медицинского общества . 94 (6): 270–2. DOI : 10.1177 / 014107680109400604 . PMC 1281520 . PMID 11387414 .
- ^ Уилбур S, M Williams, Williams R, Scinicariello F, Klotzbach JM, Diamond GL, Цитра M (2012). «Воздействие на здоровье» . Токсикологический профиль окиси углерода . обзорная статья. Министерство здравоохранения и социальных служб США, Служба общественного здравоохранения, Агентство регистрации токсичных веществ и заболеваний. PMID 23946966 .
Дальнейшее чтение [ править ]
- Ким ХХ, Чой С. (август 2018). «Терапевтические аспекты окиси углерода при сердечно-сосудистых заболеваниях» . обзорная статья. Международный журнал молекулярных наук . 19 (8): 2381. DOI : 10,3390 / ijms19082381 . PMC 6121498 . PMID 30104479 .
- Исмаилова А, Кутер Д., Боле Д.С., Батлер И.С. (2018). «Обзор потенциальных терапевтических применений молекул, высвобождающих CO» . обзорная статья. Биоинорганическая химия и приложения . 2018 : 8547364. дои : 10,1155 / 2018/8547364 . PMC 6109489 . PMID 30158958 .
- Abeyrathna N, Washington K, Bashur C, Liao Y (октябрь 2017 г.). «Неметаллические молекулы, выделяющие монооксид углерода (CORM)». обзорная статья. Органическая и биомолекулярная химия . 15 (41): 8692–8699. DOI : 10.1039 / c7ob01674c . PMID 28948260 .
- Хоппер К., Уоллборн Дж. (Август 2019 г.). «Доставка окиси углерода с помощью анестетиков на основе галогенированного эфира». обзорная статья. Оксид азота . 89 : 93–95. DOI : 10.1016 / j.niox.2019.05.006 . PMID 31125687 .
- Уилсон Дж. Л., Джесси Х. Э., Пул Р. К., Дэвидж К. С. (май 2012 г.). «Антибактериальные эффекты окиси углерода». обзорная статья. Текущая фармацевтическая биотехнология . 13 (6): 760–8. DOI : 10.2174 / 138920112800399329 . PMID 22201612 .
- Сланина Т., Себей П. (май 2018 г.). «PhotoCORMs, активируемые видимым светом: рациональная конструкция высвобождающих CO органических молекул, абсорбирующихся в прозрачном для тканей окне» . обзорная статья. Фотохимические и фотобиологические науки . 17 (6): 692–710. DOI : 10.1039 / C8PP00096D . PMID 29796556 .