Хлоралкиловые эфиры представляют собой класс органических соединений с общей структурой RO- (CH 2 ) n -Cl, характеризующийся как простой эфир, связанный с хлорметильной группой через алкановую цепь.
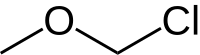
Хлорметилметиловый эфир (CMME) представляет собой простой эфир формулы C H 3 O C H 2 Cl . Он используется в качестве алкилирующего агента и промышленного растворителя для производства додецилбензилхлорида , гидрофобизаторов , ионообменных смол , полимеров и в качестве реагента хлорметилирования . Это известный канцероген для человека . [1] В органическом синтезе соединение используется для введения метоксиметильной (MOM) защитной группы .
Близкородственными соединениями, имеющими промышленное значение, являются бис (хлорметиловый) эфир (BCME) (близкий к химическому оружию серный иприт ) [2] и бензилхлорметиловый эфир (BOMCl).
| Хлорметиловый эфир | р | Молярная масса | Количество CAS | Температура кипения ° C | |
| Бензил хлорметиловый эфир | Бензил | 156,61 | 3587-60-8 | 102 ° C при 14 мм рт. Ст. (1,9 кПа) | |
| Хлорметилметиловый эфир | Метил |  | 80,51 | 107-30-2 | 55-57 |
| Бис (хлорметиловый) эфир | 114,96 | 542-88-1 | 106 | ||
| трет-бутилхлорметиловый эфир | Бутил |  | 124,5 | ||
| Метоксиэтилхлорметиловый эфир | 124,57 | 3970-21-6 | 50-52 ° C при 13 мм рт. Ст. (1,7 кПа) | ||
| Дихлорметилметиловый эфир |  | 114,96 | 4885-02-3 | 82 - 85,5 ° С | |
| Типичные хлоралкиловые эфиры [3] | |||||
Защита от алкоголя [ править ]
2-Метоксиэтоксиметильная (MEM) группа обычно используется в органическом синтезе в качестве защитной группы для спиртов .
Наиболее распространенные методы защиты [ править ]
- Обработка спирта основаниями, такими как гидрид натрия или гидрид калия и 2-метоксиэтоксиметилхлорид в тетрагидрофуране (ТГФ) при 0 ° C [4]
- Группа MEM также может быть установлена при температуре окружающей среды с помощью 2-метоксиэтоксиметилхлорида и мягкого основания, такого как N, N-диизопропилэтиламин (DIPEA) в дихлорметане [5]
Наиболее распространенные методы снятия защиты [ править ]
2-метоксиэтоксиметильная защитная группа может быть отщеплена рядом кислот Льюиса, включая, но не ограничиваясь ими:
- TiCl 4 или ZnBr 2 в дихлорметане при температуре от 0 ° C до температуры окружающей среды
- Если выбранный растворитель представляет собой протонный растворитель, такой как метанол , муравьиная кислота может использоваться для расщепления группы MEM при повышенных температурах.
_____________________________
Метоксиметил (MOM) используется в качестве защитной группы для спиртов в органическом синтезе .
Наиболее распространенные методы защиты [ править ]
- Обработка спирта N, N-диизопропилэтиламином (DIPEA) и метоксиметилхлоридом ( хлорид MOM ) в дихлорметане при 0 ° C [6]
[7]
- Для реакций, проводимых в более полярных растворителях, таких как тетрагидрофуран (ТГФ) или N, N-диметилформамид (ДМФ), защиту спирта можно проводить с помощью гидрида натрия при температуре от 0 ° C до температуры окружающей среды.
Наиболее распространенные методы снятия защиты [ править ]
Группа MOM может быть отщеплена кислотой, обычно используемые условия для снятия защиты со спиртов MOM включают: [6]
- Концентрированная соляная кислота в метаноле или воде
- Трифторуксусная кислота (TFA) в дихлорметане
- Ацетилхлорид в метаноле при 0 ° C
[8]
Ссылки [ править ]
- ^ Бис (хлорметил) эфир и технический хлорметилметиловый эфир CAS Nos. 542-88-1 и 107-30-2 , Отчет о канцерогенных веществах , одиннадцатое издание
- ^ Паспорт безопасности бис (хлорметил) эфира , Отдел охраны труда и техники безопасности, Национальные институты здравоохранения США.
- ^ «Сигма-Олдрич: аналитические, биологические, химические и материаловедческие продукты и услуги» .
- ^ Кори, EJ; Гра, Жан-Луи; Ульрих, Питер (1976-03-01). «Новый общий метод защиты гидроксильной функции». Буквы тетраэдра . 17 (11): 809–812. DOI : 10.1016 / S0040-4039 (00) 92890-9 .
- ^ Ли, Хон Мён; Ньето-Оберхубер, Кристина; Шаир, Мэтью Д. (17 декабря 2008 г.). «Энантиоселективный синтез (+) - кортистатина А, мощного и селективного ингибитора пролиферации эндотелиальных клеток». Журнал Американского химического общества . 130 (50): 16864–16866. DOI : 10.1021 / ja8071918 . ISSN 0002-7863 . PMID 19053422 .
- ^ a b Wuts, Питер GM; Грин, Теодора В. (2006). Защитные группы Грина в органическом синтезе, четвертое издание - Wuts - онлайн-библиотека Wiley . DOI : 10.1002 / 0470053488 . ISBN 9780470053485.
- ^ Эндерс, Дитер; Гейбель, Гюнтер; Осборн, Саймон (2000-04-17). «Диастерео- и энантиоселективный тотальный синтез стигмателлина А». Химия - европейский журнал . 6 (8): 1302–1309. DOI : 10.1002 / (SICI) 1521-3765 (20000417) 6: 8 <1302 :: AID-CHEM1302> 3.0.CO; 2-J .
- ^ Амано, Сэйдзи; Такемура, Нориаки; Оцука, Масами; Огава, Сейитиро; Чида, Норитака (26 марта 1999 г.). «Полный синтез паникулида А из d-глюкозы». Тетраэдр . 55 (13): 3855–3870. DOI : 10.1016 / S0040-4020 (99) 00096-4 .