В кристаллографии , кристаллическая структура представляет собой описание упорядоченного расположения атомов , ионов или молекул в кристаллическом материале . [1] Упорядоченные структуры возникают из внутренней природы составляющих частиц и образуют симметричные узоры, которые повторяются в основных направлениях трехмерного пространства в материи.
Наименьшая группа частиц в материале, составляющая этот повторяющийся узор, - это элементарная ячейка структуры. Элементарная ячейка полностью отражает симметрию и структуру всего кристалла, который построен до повторяющегося перевода элементарной ячейки вдоль его главных осей. Векторы трансляции определяют узлы решетки Браве .
Длины главных осей или краев элементарной ячейки и углы между ними являются постоянными решетки , также называемыми параметрами решетки или параметрами ячейки . В симметрии свойство кристалла описывается концепцией пространственных групп . [1] Все возможные симметричные расположения частиц в трехмерном пространстве могут быть описаны 230 пространственными группами .
Кристаллическая структура и симметрия играют решающую роль в определении многих физических свойств, таких как спайность , электронная зонная структура и оптическая прозрачность .
Элементарная ячейка [ править ]
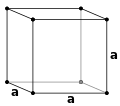
Кристаллическая структура описывается с точки зрения геометрии расположения частиц в элементарной ячейке. Элементарная ячейка определяется как наименьшая повторяющаяся единица, имеющая полную симметрию кристаллической структуры. [2] Геометрия элементарной ячейки определяется как параллелепипед , обеспечивающий шесть параметров решетки, взятых как длины краев ячейки ( a , b , c ) и углы между ними (α, β, γ). Положение частиц внутри элементарной ячейки описывается дробными координатами ( x i , y i , z i) по краям ячейки, отсчитываемой от контрольной точки. Необходимо указать только координаты наименьшего асимметричного подмножества частиц. Эта группа частиц может быть выбрана так, чтобы она занимала наименьшее физическое пространство, а это означает, что не все частицы должны физически находиться внутри границ, задаваемых параметрами решетки. Все остальные частицы элементарной ячейки генерируются операциями симметрии, которые характеризуют симметрию элементарной ячейки. Совокупность операций симметрии элементарной ячейки формально выражается как пространственная группа кристаллической структуры. [3]
Гранецентрированный кубический (F)
Индексы Миллера [ править ]
Векторы и плоскости в кристаллической решетке описываются трехзначным индексом Миллера . Этот синтаксис использует индексы ℓ , m и n в качестве параметров направления. [4]
По определению, синтаксис ( ℓmn ) обозначает плоскость, которая пересекает три точки a 1 / ℓ , a 2 / m и a 3 / n или некоторые из них. То есть индексы Миллера пропорциональны обратным точкам пересечений плоскости с элементарной ячейкой (в базисе векторов решетки). Если один или несколько индексов равны нулю, это означает, что плоскости не пересекают эту ось (т. Е. Точка пересечения находится «на бесконечности»). Плоскость, содержащая координатную ось, перемещается так, что она больше не содержит эту ось до определения ее индексов Миллера. Индексы Миллера для плоскости - целые числабез общих факторов. Отрицательные показатели обозначаются горизонтальными полосами, как в (1 2 3). В ортогональной системе координат для кубической ячейки индексы Миллера плоскости являются декартовыми компонентами вектора, нормального к плоскости.
Если рассматривать только ( ℓmn ) плоскости, пересекающие одну или несколько точек решетки ( плоскости решетки ), расстояние d между соседними плоскостями решетки связано с (кратчайшим) вектором обратной решетки, ортогональным плоскостям, по формуле
Самолеты и направления [ править ]
Кристаллографические направления - это геометрические линии, соединяющие узлы ( атомы , ионы или молекулы ) кристалла. Точно так же кристаллографические плоскости представляют собой геометрические плоскости, соединяющие узлы. Некоторые направления и плоскости имеют более высокую плотность узлов. Эти плоскости с высокой плотностью влияют на поведение кристалла следующим образом: [1]
- Оптические свойства : показатель преломления напрямую связан с плотностью (или периодическими колебаниями плотности).
- Адсорбция и реакционная способность : физическая адсорбция и химические реакции происходят на или вблизи поверхностных атомов или молекул. Таким образом, эти явления чувствительны к плотности узлов.
- Поверхностное натяжение : конденсация материала означает, что атомы, ионы или молекулы более стабильны, если они окружены другими подобными частицами. Таким образом, поверхностное натяжение границы раздела зависит от плотности на поверхности.
- Микроструктурные дефекты : поры и кристаллиты обычно имеют прямые границы зерен, следующие за плоскостями с более высокой плотностью.
- Расщепление : обычно происходит параллельно плоскостям с более высокой плотностью.
- Пластическая деформация : скольжение дислокаций происходит преимущественно параллельно плоскостям с более высокой плотностью. Возмущение, переносимое дислокацией ( вектор Бюргерса ), идет в плотном направлении. Смещение одного узла в более плотном направлении требует меньшего искажения кристаллической решетки.
Некоторые направления и плоскости определяются симметрией кристаллической системы. В моноклинной, ромбоэдрической, тетрагональной и тригонально-гексагональной системах есть одна уникальная ось (иногда называемая главной осью ), которая имеет более высокую вращательную симметрию, чем две другие оси. Базисная плоскость является плоскостью , перпендикулярной главной оси в этих кристаллических системах. Для триклинных, орторомбических и кубических кристаллических систем обозначение оси произвольное, главная ось отсутствует.
Кубические структуры [ править ]
В частном случае простых кубических кристаллов векторы решетки ортогональны и имеют одинаковую длину (обычно обозначаются a ); аналогично для обратной решетки. Таким образом, в этом общем случае индексы Миллера ( ℓmn ) и [ ℓmn ] просто обозначают нормали / направления в декартовых координатах . Для кубических кристаллов с постоянной решетки a расстояние d между соседними (ℓmn) плоскостями решетки равно (сверху):
Из-за симметрии кубических кристаллов можно менять место и знак целых чисел и иметь эквивалентные направления и плоскости:
- Координаты в угловых скобках, такие как «100», обозначают семейство направлений, эквивалентных из-за операций симметрии, таких как [100], [010], [001] или отрицательного значения любого из этих направлений.
- Координаты в фигурных скобках или скобки , такие как {100} обозначим семейство плоских нормалей, которые эквивалентны за счет операций симметрии, то , как много угловые скобки обозначают семейство направлений.
Для гранецентрированной кубической (ГЦК) и объемноцентрированной кубической (ОЦК) решеток векторы примитивной решетки не ортогональны. Однако в этих случаях индексы Миллера обычно определяются относительно векторов решетки кубической сверхъячейки и, следовательно, снова являются просто декартовыми направлениями .
Межплоскостное расстояние [ править ]
Расстояние d между соседними ( hkℓ ) плоскостями решетки определяется выражением [5] [6]
- Кубический:
- Тетрагональный:
- Шестиугольник:
- Ромбоэдрический:
- Орторомбический:
- Моноклиника:
- Триклиник:
Классификация по симметрии [ править ]
Определяющим свойством кристалла является присущая ему симметрия. Выполнение определенных операций симметрии с кристаллической решеткой не меняет ее. Все кристаллы обладают трансляционной симметрией в трех направлениях, но некоторые имеют и другие элементы симметрии. Например, поворот кристалла на 180 ° вокруг определенной оси может привести к атомной конфигурации, идентичной исходной конфигурации; кристалл имеет двойную вращательную симметрию относительно этой оси. В дополнение к вращательной симметрии кристалл может иметь симметрию в виде зеркальных плоскостей, а также так называемые составные симметрии, которые представляют собой комбинацию трансляционной и вращательной или зеркальной симметрии. Полная классификация кристалла достигается, когда идентифицированы все присущие кристаллу симметрии. [7]
Решетчатые системы [ править ]
Решеточные системы представляют собой группу кристаллических структур в соответствии с осевой системой, используемой для описания их решетки. Каждая решетчатая система состоит из трех осей с определенным геометрическим расположением. Все кристаллы попадают в одну из семи систем решеток. Они похожи, но не совсем такие же, как семь кристаллических систем .
| Кристальная семья | Решетчатая система | Schönflies | 14 решеток Браве | |||
|---|---|---|---|---|---|---|
| Примитивный | По центру основания | По центру тела | По центру лица | |||
| триклинический | C i | |||||
| моноклинический | C 2 ч | |||||
| ромбический | Д 2ч | |||||
| четырехугольный | Д 4ч | |||||
| шестиугольный | ромбоэдрический | D 3d | ||||
| шестиугольный | Д 6ч | |||||
| кубический | О ч | |||||
Самая простая и наиболее симметричная, кубическая или изометрическая система, имеет симметрию куба , то есть имеет четыре оси вращения третьего порядка , ориентированные под углом 109,5 ° ( тетраэдрический угол ) относительно друг друга. Эти тройные оси лежат по диагоналям тела куба. Остальные шесть решетчатых систем являются гексагональной , тетрагональной , ромбоэдрической (часто путают с тригональной кристаллической системой ), ромбической , моноклинной и триклинной .
Решетки Браве [ править ]
Решетки Браве , также называемые пространственными решетками , описывают геометрическое расположение узлов решетки [4] и, следовательно, трансляционную симметрию кристалла. Три измерения пространства дают 14 различных решеток Браве, описывающих трансляционную симметрию. Все известные сегодня кристаллические материалы, за исключением квазикристаллов , вписываются в одну из этих схем. Четырнадцать трехмерных решеток, классифицированных по системе решеток, показаны выше.
Кристаллическая структура состоит из одной и той же группы атомов, основы , расположенной вокруг каждой точки решетки. Таким образом, эта группа атомов бесконечно повторяется в трех измерениях в соответствии с расположением одной из решеток Браве. Характерное вращение и зеркальная симметрия элементарной ячейки описываются ее кристаллографической точечной группой .
Кристаллические системы [ править ]
Кристаллическая система - это набор точечных групп, в которых сами точечные группы и соответствующие им пространственные группы назначены решеточной системе. Из 32 точечных групп, существующих в трех измерениях, большинство относятся только к одной системе решетки, и в этом случае кристаллическая система и система решетки имеют одно и то же имя. Однако пять точечных групп приписываются двум системам решеток, ромбоэдрической и гексагональной, поскольку обе системы решеток обладают тройной вращательной симметрией. Эти точечные группы относятся к тригональной кристаллической системе.
| Кристальная семья | Кристаллическая система | Группа точек / класс кристалла | Schönflies | Точечная симметрия | Заказ | Абстрактная группа |
|---|---|---|---|---|---|---|
| триклинический | педальный | C 1 | энантиоморфный полярный | 1 | банальный | |
| пинакоидальный | C i (S 2 ) | центросимметричный | 2 | циклический | ||
| моноклинический | клиновидный | C 2 | энантиоморфный полярный | 2 | циклический | |
| домический | C s (C 1h ) | полярный | 2 | циклический | ||
| призматический | C 2 ч | центросимметричный | 4 | Кляйн четыре | ||
| ромбический | ромбико-дисфеноидальный | D 2 (В) | энантиоморфный | 4 | Кляйн четыре | |
| ромбовидно- пирамидальный | C 2v | полярный | 4 | Кляйн четыре | ||
| ромбовидно- дипирамидальный | Д 2 ч (В ч ) | центросимметричный | 8 | |||
| четырехугольный | тетрагонально-пирамидальный | C 4 | энантиоморфный полярный | 4 | циклический | |
| тетрагонально-дисфеноидальный | S 4 | нецентросимметричный | 4 | циклический | ||
| тетрагонально-дипирамидальный | C 4ч | центросимметричный | 8 | |||
| тетрагонально-трапециевидный | D 4 | энантиоморфный | 8 | двугранный | ||
| дитетрагонально-пирамидальный | C 4v | полярный | 8 | двугранный | ||
| тетрагонально-чешуйчатый | D 2d (V d ) | нецентросимметричный | 8 | двугранный | ||
| дитетрагонально-дипирамидальный | Д 4ч | центросимметричный | 16 | |||
| шестиугольный | тригональный | тригонально-пирамидальный | C 3 | энантиоморфный полярный | 3 | циклический |
| ромбоэдрический | C 3i (S 6 ) | центросимметричный | 6 | циклический | ||
| тригонально-трапецоэдрический | D 3 | энантиоморфный | 6 | двугранный | ||
| дитригонально-пирамидальный | C 3v | полярный | 6 | двугранный | ||
| дитригонально-чешуйчатый | D 3d | центросимметричный | 12 | двугранный | ||
| шестиугольный | гексагонально-пирамидальный | С 6 | энантиоморфный полярный | 6 | циклический | |
| тригонально-дипирамидальный | C 3ч | нецентросимметричный | 6 | циклический | ||
| гексагонально-дипирамидальный | C 6h | центросимметричный | 12 | |||
| гексагонально-трапециевидный | D 6 | энантиоморфный | 12 | двугранный | ||
| дигексагонально-пирамидальный | C 6v | полярный | 12 | двугранный | ||
| дитригонально-дипирамидный | Д 3ч | нецентросимметричный | 12 | двугранный | ||
| дигексагонально-дипирамидальный | Д 6ч | центросимметричный | 24 | |||
| кубический | тетартоидный | Т | энантиоморфный | 12 | чередование | |
| диплоидный | Т ч | центросимметричный | 24 | |||
| гироидный | О | энантиоморфный | 24 | симметричный | ||
| шестигранник | Т д | нецентросимметричный | 24 | симметричный | ||
| гексоктаэдрический | О ч | центросимметричный | 48 | |||
Всего существует семь кристаллических систем: триклинная, моноклинная, ромбическая, тетрагональная, тригональная, гексагональная и кубическая.
Группы точек [ править ]
Кристаллографические точечная группа или кристаллический класс представляет собой математическую группу , включающую операции симметрии , которые оставляют по меньшей мере , одну точку неподвижным , и что оставить внешний вид кристаллической структуры без изменений. Эти операции симметрии включают
- Отражение , которое отражает структуру в плоскости отражения.
- Вращение , при котором конструкция поворачивается на заданную часть круга вокруг оси вращения.
- Инверсия , которая меняет знак координаты каждой точки относительно центра симметрии или точки инверсии.
- Неправильное вращение , которое состоит из вращения вокруг оси с последующим инверсией.
Оси вращения (собственные и несобственные), плоскости отражения и центры симметрии вместе называются элементами симметрии . Всего существует 32 возможных класса кристаллов. Каждую из них можно отнести к одной из семи кристаллических систем.
Космические группы [ править ]
Помимо операций точечной группы, пространственная группа кристаллической структуры содержит операции трансляционной симметрии. К ним относятся:
- Чистые переводы , которые перемещают точку по вектору
- Винтовые оси , которые вращают точку вокруг оси, перемещаясь параллельно оси. [8]
- Плоскости скольжения , которые отражают точку через плоскость, переводя ее параллельно плоскости. [8]
Есть 230 различных космических групп.
Атомная координация [ править ]
Рассматривая расположение атомов относительно друг друга, их координационные числа (или количество ближайших соседей), межатомные расстояния, типы связей и т. Д., Можно сформировать общее представление о структурах и альтернативных способах их визуализации. [9]
Тесная упаковка [ править ]
Используемые принципы можно понять, рассмотрев наиболее эффективный способ упаковки сфер одинакового размера и укладки плотно упакованных атомных плоскостей в трех измерениях. Например, если плоскость A лежит ниже плоскости B, есть два возможных способа размещения дополнительного атома поверх слоя B. Если дополнительный слой был помещен непосредственно над плоскостью A, это привело бы к следующей серии:
- ... АБАБАБАБ ...
Такое расположение атомов в кристаллической структуре известно как гексагональная плотная упаковка (ГПУ) .
Если, однако, все три плоскости расположены в шахматном порядке относительно друг друга и последовательность повторяется только после того, как четвертый слой будет расположен непосредственно над плоскостью A, тогда возникает следующая последовательность:
- ... ABCABCABC ...
Этот тип структурного устройства известен как кубическая плотная упаковка (ccp) .
Элементарной ячейкой ccp-расположения атомов является гранецентрированная кубическая (ГЦК) элементарная ячейка. Это не сразу очевидно, поскольку плотно упакованные слои параллельны плоскостям {111} элементарной ячейки ГЦК. Есть четыре различных ориентации плотноупакованных слоев.
Эффективность упаковки может быть разработана путем расчета общего объема сфер и деления на объеме ячейки следующим образом :
Эффективность упаковки 74% - это максимальная плотность, возможная для элементарных ячеек, построенных из сфер только одного размера. Большинство кристаллических форм металлических элементов - это ГПУ, ГЦК или ОЦК (объемно-центрированная кубическая). Координационное число атомов в ГПУ и ГЦК структуры 12 и ее атомный фактор упаковки (ПФ) это число упоминалось выше, 0,74. Это можно сравнить с APF ОЦК-структуры, равным 0,68.
Границы зерна [ править ]
Границы зерен - это границы раздела кристаллов разной ориентации. [4] граница зерна представляет собой однофазный интерфейс, с кристаллами на каждой стороне границы являются идентичными , за исключением ориентации. Иногда, хотя и редко, используется термин «граница кристаллита». Области границ зерен содержат те атомы, которые были возмущены из своих исходных узлов решетки, дислокации и примеси, которые мигрировали к границе зерен с более низкой энергией.
Рассматривая границу зерна геометрически как границу раздела монокристалла, разрезанного на две части, одна из которых вращается, мы видим, что для определения границы зерна требуется пять переменных. Первые два числа берутся из единичного вектора, определяющего ось вращения. Третье число обозначает угол поворота зерна. Последние два числа определяют плоскость границы зерна (или единичный вектор, перпендикулярный этой плоскости). [9]
Границы зерен нарушают движение дислокаций в материале, поэтому уменьшение размера кристаллитов является обычным способом повышения прочности, как описано соотношением Холла – Петча . Поскольку границы зерен являются дефектами кристаллической структуры, они имеют тенденцию уменьшать электрическую и теплопроводность материала. Высокая межфазная энергия и относительно слабая связь в большинстве границ зерен часто делают их предпочтительными участками для начала коррозии и выделения новых фаз из твердого тела. Они также важны для многих механизмов ползучести . [9]
Границы зерен обычно имеют ширину всего несколько нанометров. В обычных материалах кристаллиты достаточно велики, чтобы границы зерен составляли небольшую часть материала. Однако достижимы очень маленькие размеры зерен. В нанокристаллических твердых телах границы зерен составляют значительную объемную долю материала, что оказывает сильное влияние на такие свойства, как диффузия и пластичность . В пределе мелких кристаллитов, когда объемная доля границ зерен приближается к 100%, материал перестает иметь какой-либо кристаллический характер и, таким образом, становится аморфным твердым телом . [9]
Дефекты и примеси [ править ]
Реальные кристаллы имеют дефекты или неровности в идеальном устройстве, описанном выше, и именно эти дефекты критически определяют многие электрические и механические свойства реальных материалов. Когда один атом замещает один из основных атомных компонентов в кристаллической структуре, могут произойти изменения электрических и тепловых свойств материала. [10] Примеси могут также проявляться как примеси электронного спина в некоторых материалах. Исследования магнитных примесей показывают, что на существенное изменение определенных свойств, таких как удельная теплоемкость, могут влиять небольшие концентрации примесей, например, примесей в полупроводниковых ферромагнитных сплавах.может привести к другим свойствам, как впервые было предсказано в конце 1960-х годов. [11] [12] Дислокации в кристаллической решетке допускают сдвиг при меньшем напряжении, чем это необходимо для идеальной кристаллической структуры. [13]
Прогнозирование структуры [ править ]
Сложность предсказания стабильных кристаллических структур на основе знания только химического состава долгое время была камнем преткновения на пути к полностью вычислительному дизайну материалов. Теперь, благодаря более мощным алгоритмам и высокопроизводительным вычислениям, структуры средней сложности могут быть предсказаны с использованием таких подходов, как эволюционные алгоритмы , случайная выборка или метадинамика.
Кристаллические структуры простых ионных твердых веществ (например, NaCl или поваренная соль) уже давно рационализированы в терминах правил Полинга , впервые изложенных в 1929 году Линусом Полингом , которого многие с тех пор называют «отцом химической связи». [14]Полинг также рассмотрел природу межатомных сил в металлах и пришел к выводу, что около половины из пяти d-орбиталей в переходных металлах участвуют в связывании, а оставшиеся несвязывающие d-орбитали ответственны за магнитные свойства. Таким образом, он смог соотнести количество d-орбиталей в образовании связи с длиной связи, а также со многими физическими свойствами вещества. Впоследствии он ввел металлическую орбиталь, дополнительную орбиталь, необходимую для разрешения беспрепятственного резонанса валентных связей между различными электронными структурами. [15]
В теории резонансной валентной связи факторы, определяющие выбор одной из альтернативных кристаллических структур металла или интерметаллического соединения, вращаются вокруг энергии резонанса связей между межатомными положениями. Ясно, что некоторые режимы резонанса будут давать больший вклад (будут более механически устойчивыми, чем другие), и что, в частности, простое соотношение количества связей к количеству позиций будет исключительным. В результате чего принцип заключается в том, что специальная стабильность связана с простейшими соотношениями или "чисел облигаций": 1 / 2 , 1 / 3 , 2 / 3 , 1 / 4 , 3⁄ 4 и т. Д. Выбор структуры и значение осевого отношения (которое определяет относительную длину связи), таким образом, является результатом попытки атома использовать свою валентность для образования стабильных связей с простыми дробными числами связей. [16] [17]
Постулируя прямую корреляцию между концентрацией электронов и кристаллической структурой в сплавах с бета-фазой, Хьюм-Ротери проанализировал тенденции изменения точек плавления, сжимаемости и длин связей в зависимости от номера группы в периодической таблице, чтобы установить систему валентностей переходные элементы в металлическом состоянии. Таким образом, эта обработка подчеркнула увеличение прочности сцепления в зависимости от номера группы. [18]Действие направленных сил было подчеркнуто в одной статье о связи между гибридами связей и металлическими структурами. Результирующая корреляция между электронными и кристаллическими структурами резюмируется одним параметром, весом d-электронов на гибридизованную металлическую орбиталь. «D-вес» составляет 0,5, 0,7 и 0,9 для структур ГЦК, ГПУ и ОЦК соответственно. Таким образом, становится очевидной связь между d-электронами и кристаллической структурой. [19]
При прогнозировании / моделировании кристаллической структуры обычно применяется периодичность, поскольку система представляется неограниченно большой во всех направлениях. Начиная с триклинной структуры без дополнительных предполагаемых свойств симметрии, систему можно заставить показать некоторые дополнительные свойства симметрии, применив Второй закон Ньютона к частицам в элементарной ячейке и недавно разработанное динамическое уравнение для векторов периодов системы [20] (решетка параметры, включая углы), даже если система подвергается внешним нагрузкам.
Полиморфизм [ править ]
Полиморфизм - это появление нескольких кристаллических форм материала. Он содержится во многих кристаллических материалах, включая полимеры , минералы и металлы . Согласно правилам фазового равновесия Гиббса, эти уникальные кристаллические фазы зависят от интенсивных переменных, таких как давление и температура. Полиморфизм связан с аллотропией , которая относится к элементарным твердым телам . Полная морфология материала описывается полиморфизмом и другими переменными, такими как габитус кристалла , аморфная фракция или кристаллографические дефекты.. Полиморфы обладают разной стабильностью и могут спонтанно и необратимо превращаться из метастабильной формы (или термодинамически нестабильной формы) в стабильную форму при определенной температуре. [21] Они также имеют разные температуры плавления , растворимость и дифрактограммы рентгеновских лучей .
Хорошим примером этого является кварцевая форма диоксида кремния или SiO 2 . В подавляющем большинстве силикатов атом Si имеет тетраэдрическую координацию по 4 атомам кислорода. Все кристаллические формы, кроме одной, содержат тетраэдрические {SiO 4} блоки, соединенные вместе общими вершинами в разном порядке. В разных минералах тетраэдры демонстрируют разную степень сетки и полимеризации. Например, они встречаются поодиночке, соединены вместе попарно, в более крупные конечные кластеры, включая кольца, цепочки, двойные цепи, листы и трехмерные каркасы. Минералы классифицируются на группы на основе этих структур. В каждой из 7 термодинамически стабильных кристаллических форм или полиморфов кристаллического кварца только 2 из 4 ребер тетраэдров {SiO 4 } являются общими с другими, что дает чистую химическую формулу кремнезема: SiO 2 .
Другой пример - элементарное олово (Sn), которое является пластичным при температурах окружающей среды, но хрупким при охлаждении. Это изменение механических свойств связано с существованием двух его основных аллотропов , α- и β-олова. Два аллотропа , встречающиеся при нормальном давлении и температуре, α-олово и β-олово, более известны как серое олово и белое олово соответственно. Еще два аллотропа, γ и σ, существуют при температурах выше 161 ° C и давлениях выше нескольких ГПа. [22] Белое олово является металлическим и является стабильной кристаллической формой при комнатной температуре или выше. Ниже 13,2 ° C олово существует в серой форме, которая имеет кубическую форму алмаза.кристаллическая структура, подобная алмазу , кремнию или германию . Серое олово вообще не имеет металлических свойств, представляет собой тускло-серый порошкообразный материал и имеет несколько применений, кроме нескольких специализированных полупроводниковых применений. [23] Хотя температура α – β превращения олова номинально составляет 13,2 ° C, примеси (например, Al, Zn и т. Д.) Понижают температуру перехода значительно ниже 0 ° C, и при добавлении Sb или Bi превращение может не происходить. вообще. [24]
Физические свойства [ править ]
Двадцать из 32 классов кристаллов являются пьезоэлектрическими , и кристаллы, принадлежащие к одному из этих классов (точечных групп), проявляют пьезоэлектричество . Все классы пьезоэлектрических элементов не обладают инверсионной симметрией . Любой материал развивает диэлектрическую поляризацию при приложении электрического поля, но вещество, которое имеет такое естественное разделение зарядов даже в отсутствие поля, называется полярным материалом. Полярность материала определяется исключительно его кристаллической структурой. Только 10 из 32 точечных групп полярны . Все полярные кристаллы являются пироэлектрическими , поэтому 10 классов полярных кристаллов иногда называют пироэлектрическими классами.
Есть несколько кристаллических структур, особенно структура перовскита , которые демонстрируют сегнетоэлектрические свойства. Это аналогично ферромагнетизму в том смысле , что в отсутствие электрического поля во время производства сегнетоэлектрический кристалл не проявляет поляризации. При приложении электрического поля достаточной величины кристалл становится постоянно поляризованным. Эта поляризация может быть обращена достаточно большим противодействием, точно так же, как ферромагнетик может быть обращен. Однако, хотя они и называются сегнетоэлектриками, эффект обусловлен кристаллической структурой (а не наличием черного металла).
См. Также [ править ]
- Зона Бриллюэна - примитивная ячейка в решетке обратного пространства кристаллов
- Кристалл инженерия
- Рост кристаллов - после первого зародышеобразования наступает второй этап кристаллизации, заключающийся в регулярной аккреции атомов или ионов на поверхности кристалла.
- Кристаллографическая база данных
- Дробные координаты
- Фазы Франка – Каспера
- Обозначение Германа – Могена - Обозначение для представления симметрии в точечных группах, плоских группах и пространственных группах
- Рост пьедестала с лазерным нагревом
- Жидкий кристалл - состояние вещества со свойствами как обычных жидкостей, так и кристаллов.
- Функция Паттерсона
- Периодическая таблица (кристаллическая структура)
- Примитивная ячейка - ячейка минимального объема (элементарная ячейка), соответствующая одной точке решетки структуры с дискретной трансляционной симметрией.
- Семенной кристалл
- Ячейка Вигнера – Зейтца - примитивная ячейка кристаллических решеток с применением разложения Вороного
Ссылки [ править ]
- ^ a b c Крюк, младший; Холл, HE (2010). Физика твердого тела . Манчестерская серия физики (2-е изд.). Джон Вили и сыновья. ISBN 9780471928041.
- ^ Уэст, Энтони Р. (1999). Основы химии твердого тела (2-е изд.). Вайли. п. 1. ISBN 978-0-471-98756-7.
- ^ Международные таблицы для кристаллографии (2006). Том A, Пространственно-групповая симметрия.
- ^ a b c Энциклопедия физики (2-е издание), RG Lerner, GL Trigg, VHC publishers, 1991, ISBN (Verlagsgesellschaft) 3-527-26954-1, ISBN (VHC Inc.) 0-89573-752-3
- ^ «4. Прямая и обратная решетки» . CSIC Dept de Cristalografia y Biologia Estructural . 6 апреля 2017 . Дата обращения 18 мая 2017 .
- ^ Эдингтон, JW (1975). Электронная дифракция в электронном микроскопе . DOI : 10.1007 / 978-1-349-02595-4 . ISBN 978-0-333-18292-5.
- ^ Эшкрофт, Н .; Мермин, Д. (1976). «Глава 7». Физика твердого тела . Брукс / Коул (Thomson Learning, Inc.). ISBN 978-0030493461.
- ^ a b Дональд Э. Сэндс (1994). «§4-2 Винтовые оси и §4-3 плоскости скольжения» . Введение в кристаллографию (Перепечатка WA Benjamin, исправленное изд. 1975 г.). Курьер-Дувр. С. 70–71. ISBN 978-0486678399.
- ^ a b c d Паркер, CB, изд. (1994). Энциклопедия физики Макгроу Хилла (2-е изд.). ISBN 978-0070514003.
- ^ Каллай, Никола (2000). Межфазная динамика . CRC Press. ISBN 978-0824700065.
- ^ Хоган, CM (1969). «Плотность состояний изолирующего ферромагнитного сплава». Физический обзор . 188 (2): 870–874. Bibcode : 1969PhRv..188..870H . DOI : 10.1103 / PhysRev.188.870 .
- ^ Чжан, XY; Зуль, Х (1985). «Спиново-волновые удвоения периода и хаос при поперечной накачке». Physical Review . 32 (4): 2530–2533. Bibcode : 1985PhRvA..32.2530Z . DOI : 10.1103 / PhysRevA.32.2530 . PMID 9896377 .
- ^ Кортни, Томас (2000). Механическое поведение материалов . Лонг-Гроув, Иллинойс: Waveland Press. п. 85. ISBN 978-1-57766-425-3.
- ^ Л. Полинг (1929). «Принципы, определяющие структуру сложных ионных кристаллов». Варенье. Chem. Soc. 51 (4): 1010–1026. DOI : 10.1021 / ja01379a006 .
- ^ Полинг, Линус (1938). «Природа межатомных сил в металлах». Физический обзор . 54 (11): 899–904. Полномочный код : 1938PhRv ... 54..899P . DOI : 10.1103 / PhysRev.54.899 .
- ^ Полинг, Линус (1947). «Атомные радиусы и межатомные расстояния в металлах». Журнал Американского химического общества . 69 (3): 542–553. DOI : 10.1021 / ja01195a024 .
- ^ Полинг, Л. (1949). "Теория резонансных валентных связей металлов и интерметаллических соединений" . Труды Королевского общества А . 196 (1046): 343–362. Bibcode : 1949RSPSA.196..343P . DOI : 10,1098 / rspa.1949.0032 .
- ^ Hume-rothery, W .; Ирвинг, HM; Уильямс, RJP (1951). «Валентности переходных элементов в металлическом состоянии». Труды Королевского общества А . 208 (1095): 431. Bibcode : 1951RSPSA.208..431H . DOI : 10.1098 / rspa.1951.0172 . S2CID 95981632 .
- ^ Альтманн, SL; Колсон, Калифорния; Хьюм-Розери, У. (1957). «О связи между гибридами облигаций и металлическими структурами». Труды Королевского общества А . 240 (1221): 145. Bibcode : 1957RSPSA.240..145A . DOI : 10.1098 / rspa.1957.0073 . S2CID 94113118 .
- Перейти ↑ Liu, Gang (2015). «Динамические уравнения для векторов периодов в периодической системе при постоянном внешнем напряжении». Может. J. Phys. 93 (9): 974–978. arXiv : cond-mat / 0209372 . Bibcode : 2015CaJPh..93..974L . DOI : 10,1139 / CJP-2014-0518 . S2CID 54966950 .
- ^ Anatase to Rutile Transition ART, в J. Mat. Sci.
- ^ Молодец, AM; Набатов, С.С. (2000). «Термодинамические потенциалы, диаграмма состояния и фазовые переходы олова при ударном сжатии». Высокая температура . 38 (5): 715–721. DOI : 10.1007 / BF02755923 . S2CID 120417927 .
- ^ Холлеман, Арнольд Ф .; Виберг, Эгон; Виберг, Нильс (1985). "Банка". Lehrbuch der Anorganischen Chemie (на немецком языке) (91–100 изд.). Вальтер де Грюйтер. С. 793–800. ISBN 978-3-11-007511-3.
- ^ Шварц, Мел (2002). «Олово и сплавы, свойства». Энциклопедия материалов, деталей и отделок (2-е изд.). CRC Press. ISBN 978-1-56676-661-6.
Внешние ссылки [ править ]
СМИ, связанные с кристаллическими структурами на Викискладе?
- Внутреннее строение кристаллов ... Кристаллография для начинающих.
- Различные типы кристаллической структуры
- Приложение A из руководства для Atoms, программное обеспечение для XAFS
- Введение в минералы: класс и система кристаллов
- Введение в кристаллографию и системы минеральных кристаллов
- Хрустальные плоскости и индексы Миллера
- Интерактивные 3D-модели кристаллов
- Конкретные модели Crystal 3D
- Открытая база данных кристаллографии (с более чем 140000 кристаллических структур)