 | |
| Имена | |
|---|---|
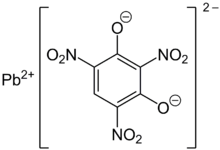
| Предпочтительное название IUPAC Свинец (II) 2,4,6-тринитробензол-1,3-бис (олат) | |
| Другие имена Свинец 2,4,6-тринитробензол-1,3-diolate свинца 2,4,6-тринитро- м -phenylene диоксида 1,3-бензолдиол, 2,4,6-тринитро-, свинец (2+) соли (1 : 1) Трицинат свинца Тринитрорезорцинат свинца Трицинат [1] | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.035.703 |
| Номер ЕС |
|
PubChem CID | |
| UNII |
|
| Номер ООН | 01:30 |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| C 6 HN 3 O 8 Pb | |
| Молярная масса | 450,288 г / моль |
| Плотность | От 3,06 до 3,1 г см −3 |
| Взрывоопасные данные | |
| Чувствительность к ударам | Высоко |
| Чувствительность к трению | Высоко |
| Скорость детонации | 5200 м / с |
| Опасности | |
| Паспорт безопасности | Оксфордский паспорт безопасности материалов |
Классификация ЕС (DSD) (устарела) | Вредно (X), Опасно для окружающей среды (N), Взрывоопасно (E) |
| NFPA 704 (огненный алмаз) | |
| 330 ° С (626 ° F, 603 К) | |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Стифнат свинца (2,4,6- тринитрорезорцинат свинца , C 6 HN 3 O 8 Pb), название которого происходит от стифиновой кислоты , представляет собой взрывчатое вещество, используемое в качестве компонента смесей капсюля и детонатора для менее чувствительных вторичных взрывчатых веществ . Стифнат свинца плохо растворяется в воде и метаноле . [2]Образцы стифната свинца различаются по цвету от желтого до золотого, оранжевого, красновато-коричневого, до коричневого. Стифнат свинца известен в виде различных полиморфов, гидратов и основных солей. Существуют нормальный моногидрат стифната свинца, одноосновный стифнат свинца, трехосновный дигидрат стифната свинца и пятиосновный дигидрат стифната свинца, а также α, β-полиморфы стифната свинца.
Стифнат свинца образует шестигранные кристаллы моногидрата и небольшие прямоугольные кристаллы. Стифнат свинца особенно чувствителен к возгоранию и разряду статического электричества . Особенно чувствительны длинные тонкие кристаллы. Стифнат свинца не реагирует с другими металлами и менее чувствителен к ударам и трению, чем фульминат ртути или азид свинца . Он стабилен при хранении даже при повышенных температурах. Как и с другими свинцовыми соединениями отработанный, стифнат свинца является токсичным в силу тяжелых металлов отравления.
Подготовка [ править ]
Хотя это и не подтверждено, стифнат свинца, возможно, был открыт Питером Гриссом (известный по тестам Грисса ) в 1874 году. В 1919 году Эдмунд Герц впервые создал препарат безводного нормального стифната свинца путем реакции стифната магния с ацетатом свинца в присутствии азотной кислоты. кислота. [3] [4]
- {C 6 N 3 O 8 } MgH 2 O + Pb (CH 3 CO 2 ) 2 → {C 6 N 3 O 8 } PbH 2 O + Mg (CH 3 CO 2 ) 2
Структура [ править ]
Нормальный стифнат свинца существует в виде α- и β-полиморфов, причем оба являются моноклинными кристаллами. Центры свинца семикоординатны и соединены кислородными мостиками. Молекула воды скоординирована с металлом, а также связана водородными связями с анионом. Многие расстояния Pb-O короткие, что указывает на некоторую степень ковалентности. Ионы стифната лежат примерно в параллельных плоскостях, связанных атомами Pb. [5] [6]
Свойства [ править ]
Теплота образования стифната свинца составляет -835 кДж моль -1 . Потеря воды приводит к образованию чувствительного безводного материала с плотностью 2,9 г см -3 . Разница в цветах остается невыясненной. [7] Стифнат свинца имеет скорость детонации 5,2 км / с и температуру взрыва 265–280 ° C через пять секунд. [8]
Приложения [ править ]
Стифнат свинца в основном используется в боеприпасах для стрелкового оружия военного и коммерческого назначения. Он служит в качестве основного взрывчатого вещества с метательным взрывчатым веществом , которое не загорается при простом ударе. [9] Стифнат свинца также используется в качестве грунтовки в микродвигателях для небольших спутниковых станций. [10]
Ссылки [ править ]
- ^ ECHA, Европейское химическое агентство "Архивная копия" (PDF) . Архивировано из оригинального (PDF) 22 октября 2014 года . Проверено 17 октября 2014 .CS1 maint: заархивированная копия как заголовок ( ссылка )
- ^ Жак Буало, Клод Фокиньон, Бернар Хюбер и Ханс Х. Мейер (2009). «Взрывчатка». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a10_143.pub2 .CS1 maint: несколько имен: список авторов ( ссылка )
- ^ JR Payne (1994). «Термохимия стифната свинца». Thermochimica Acta . 242 : 13–21. DOI : 10.1016 / 0040-6031 (94) 85003-8 .
- ^ Жак Буало; Клод Фокиньон; Бернар Хюбер; Ханс Х. Мейер (2009). Взрывчатка . Энциклопедия промышленной химии Ульмана . DOI : 10.1002 / 14356007.a10_143.pub2 . ISBN 978-3527306732.
- Перейти ↑ Pierce-Butler, MA (1984). «Структура свинцовой соли моногидрата 2,4,6-тринитро-1,3-бензолдиола (альфа-полиморф)». Acta Crystallogr . 40 : 63–65. DOI : 10.1107 / S0108270184003036 .
- Перейти ↑ Pierce-Butler, MA (1982). «Структуры бариевой соли моногидрата 2,4,6-тринитро-1,3-бензолдиола и изоморфной соли свинца (бета-полиморф)». Acta Crystallogr . 38 (12): 3100–3104. DOI : 10.1107 / S0567740882010966 .
- ^ Роберт Матяш; Джи Пачман (2013). Первичные взрывчатые вещества . Springer Science & Business Media. DOI : 10.1007 / 978-3-642-28436-6 . ISBN 978-3-642-28435-9. S2CID 199492549 .
- ^ Хайман Хенкин; Рассел МакГилл (1952). «Скорость взрывного разложения взрывчатых веществ. Экспериментальные и теоретические кинетические исследования в зависимости от температуры». Ind. Eng. Chem . 44 (6): 1391–1395. DOI : 10.1021 / ie50510a054 .
- ^ Грей, Теодор (2009). «Flash Bang» . Популярная наука .
- ^ Дэниел В. Янгнер; и другие. (2000). "Мегапиксельные массивы микродвигателей MEMS для малых спутниковых станций" . 14-я ежегодная конференция Honeywell Technology / USU по малым спутникам .
Внешние ссылки [ править ]
- Национальный реестр загрязнителей - Свинец и сведения о свинцовых соединениях
