 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Медрол, Депо-Медрол (в виде ацетата ), Солю-Медрол (в виде сукцината ), другие |
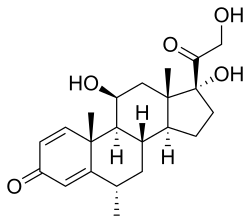
| Другие имена | 6α-метилпреднизолон; 11β, 17,21-тригидрокси-6α-метил-δ 1- прогестерон; 11β, 17,21-тригидрокси-6α-метилпрегна-1,4-диен-3,20-дион |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a682795 |
| Данные лицензии |
|
Категория беременности |
|
| Пути администрирования | По рот , И. М. (как ацетат ), И.А. (как ацетат ), IV (как сукцинат , suleptanate ) |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетические данные | |
| Связывание с белками | 78% |
| Метаболизм | В первую очередь печень , почки , ткани ; CYP3A4 |
| Ликвидация Период полураспада | 18–26 часов |
| Экскреция | Моча |
| Идентификаторы | |
Название ИЮПАК
| |
| Количество CAS |
|
| PubChem CID |
|
| IUPHAR / BPS |
|
| DrugBank |
|
| ChemSpider |
|
| UNII |
|
| КЕГГ |
|
| ЧЭБИ |
|
| ЧЭМБЛ |
|
| CompTox Dashboard ( EPA ) |
|
| ECHA InfoCard | 100,001,343 |
| Химические и физические данные | |
| Формула | С 22 Н 30 О 5 |
| Молярная масса | 374,477 г · моль -1 |
| 3D модель ( JSmol ) |
|
| Температура плавления | От 228 до 237 ° C (от 442 до 459 ° F) |
| Растворимость в воде | 1,20х10 + 2 мг / мл (20 ° С) |
Улыбки
| |
ИнЧИ
| |
| (проверять) | |
Метилпреднизолон (Депо-Медрол, Медрол, Солю-Медрол) - синтетический глюкокортикоид , который в первую очередь назначают из-за его противовоспалительного и иммунодепрессивного действия. [2] [3] [4] Он используется либо в низких дозах при хронических заболеваниях, либо одновременно в высоких дозах во время обострений. Метилпреднизолон и его производные можно вводить перорально или парентерально. [5]
Независимо от пути введения, метилпреднизолон системно интегрируется, о чем свидетельствует его эффективность для быстрого уменьшения воспаления во время обострений. [6] Это связано со многими побочными реакциями, которые требуют отмены препарата, как только болезнь окажется под контролем. [7] Серьезные побочные эффекты включают ятрогенный синдром Кушинга, гипертонию, остеопороз, диабет, инфекции и атрофию кожи. [7]
По химическому составу метилпреднизолон представляет собой синтетический стероидный гормон прегнана, полученный из гидрокортизона и преднизолона . Он принадлежит к классу синтетических глюкокортикоидов и, в более общем плане, кортикостероидов . Он действует как агонист рецепторов минералокортикоидов и глюкокортикоидов. По сравнению с другими экзогенными глюкокортикоидами, метилпреднизолон имеет более высокое сродство к рецепторам глюкокортикоидов, чем к рецепторам минералокортикоидов.
Название глюкокортикоидов было получено после открытия их участия в регуляции углеводного обмена. [7] В настоящее время считается, что клеточные функции глюкокортикоидов, таких как метилпреднизолон, регулируют гомеостаз, метаболизм, развитие, познание и воспаление. [7] Они играют решающую роль в адаптации и реагировании на окружающий, физический и эмоциональный стресс. [7]
Метилпреднизолон был впервые синтезирован и произведен компанией Upjohn Company (ныне Pfizer) и одобрен FDA в США 2 октября 1957 г. [8] Срок действия патента истек, и теперь доступны генерики. В 2021 году он занимает 153-е место среди наиболее часто назначаемых лекарств в Соединенных Штатах, на него выписано более четырех миллионов рецептов. [9] По сравнению с 2017 годом, он поднялся на четыре позиции в рейтинге. Метилпреднизолон был назначен в качестве лечения во время пандемии COVID-19 . [10] [11]
Фармакодинамика [ править ]
Метилпреднизолон - это синтетический глюкокортикоид (ГК), который оказывает плейотропное действие на различные физиологические механизмы. [3] Тем не менее, они были назначены широко из-за их воздействия на воспаление и иммунитет. [4] Действие синтетических глюкокортикоидов, таких как метилпреднизолон, зависит от его связи с внутриклеточными рецепторами глюкокортикоидов (GR) и, в меньшей степени, с рецепторами минералокортикоидов (MR). GR широко распространены в отличие от MR, которые показывают ограниченное распределение в тканях. [7] По этому механизму рецептор, связанный с лигандом, перемещается в ядро и модулирует экспрессию генов. [4]
Преобразование сигнала [ править ]
В отсутствие эндогенных или синтетических GC, мономерные GR расположены в цитоплазме и образуют мультибелковые комплексы с белками теплового шока (HSP), иммунофилинами и другими шаперонами, такими как src и p23. [2] GR действует лиганд-зависимым образом, при этом комплекс удерживает GR в неактивной форме с высокой специфичностью для лиганда. [4] Когда метилпреднизолон из плазмы или интерстициальной жидкости пассивно диффундирует через клеточную мембрану, он связывается с GR, вызывая конформационные изменения и димеризацию GC-GR. Ранее считалось, что это конформационное изменение было необходимо для диссоциации мультибелкового комплекса, чтобы позволить связанному с лигандом рецептору перемещаться в ядро. [2] [3]Однако недавние исследования показали, что шапероны играют роль в ядерном импорте. [12] Активный в настоящее время комплекс метилпреднизолон-GR может либо трансдуктировать негеномные изменения в цитоплазме, либо перемещаться в ядро и регулировать транскрипционную активность генов-мишеней с помощью прямых, связывающих или сложных механизмов. [3]
Геномная сигнализация [ править ]
Геномные механизмы, независимо от типа, вызывают ответы с медленным началом и медленным рассеянием. [13] Это связано с продолжительностью транскрипции и трансляции мРНК. [13] Глюкокортикоиды обладают способностью регулировать примерно от 100 до 1000 генов со специфичностью к типу клеток. [13]
Три основных механизма описали, как комплекс MP-GR изменяет экспрессию генов путем связывания с ДНК или модуляторов транскрипции. [3] Один из механизмов геномной передачи сигналов происходит, когда комплекс MP-GR напрямую связывается с последовательностями ДНК, называемыми элементами глюкокортикоидного ответа (GRE). [3] GRE расположены в регуляторных областях генов-мишеней и опосредуют их трансактивацию или трансрепрессию. [4] Например, активация липокортина 1 (ANAX1) отрицательно влияет на выработку простагландинов и лейкотриенов , известных провоспалительных сигналов. Точно так же отрицательные GRE (nGRE) ответственны за репрессию генов, участвующих в активации иммунных клеток.[3]
Пост-транскрипционные модификации [ править ]
Посттрансляционные модификации (PTM) также вносят вклад в передачу сигналов метилпреднизолона и могут вызывать геномные и негеномные эффекты. [12] GR содержит несколько сайтов для фосфорилирования, сумоилирования, убиквитинирования и ацетилирования, которое в первую очередь происходит после связывания внутриклеточного метилпреднизолона с GR. [4] [14] PTM модулируют многие функции, включая ядерную транслокацию, силу и продолжительность передачи сигналов рецепторами и взаимодействие кофакторов. [12] Конкретным примером является деацетилирование гистондеацетилазой 2 (HDACe), необходимое для трансрепрессии NF-κB. [4] [14]
Негеномная передача сигналов [ править ]
Механизмы негеномной передачи сигналов отличаются от геномной передачи сигналов, но опосредуют сходные пути и обеспечивают терапевтическое значение. [15] [16] Эти механизмы характеризуются быстрым началом (менее 15 минут), поскольку они не зависят от длительной транскрипции или трансляции и не изменяются ингибиторами транскрипции. [13]
Негеномная передача сигналов, индуцированная метилпреднизолоном, классифицируется по трем механизмам: (1) негеномные эффекты, опосредованные цитоплазматическим рецептором глюкокортикоидов (cGR), (2) негеномные эффекты мембраносвязанного рецептора глюкокортикоидов (mGR) и (3) физиохимические взаимодействия с клеточными мембранами (неспецифические негеномные эффекты). [13] [15]
Белки, которые диссоциируют от активированного комплекса GC-cGR, запускают механизмы, не зависящие от внутриклеточной транскрипции. [17] [18] Это свидетельствует о том, что диссоциированный SRC отвечает за ингибирование высвобождения арахидоновой кислоты (АК) из фосфолипидов клеточной мембраны. [15] АК требуется для синтеза медиаторов воспаления (простагландинов и лейкотриенов), и, таким образом, ингибирование АК опосредует несколько важных путей, таких как рост клеток, метаболизм и воспаление. [17] [18]
Предыдущие исследования идентифицировали mGR в клетках лимфомы, но только в 2004 году mGR были идентифицированы в периферических мононуклеарных клетках человека. [15] Распространенность mGR варьируется в зависимости от типа клеток, с самой высокой концентрацией в В-лимфоцитах до 12,3%, до 9,2% в моноцитах и отсутствием в Т-лимфоцитах. [15] Исследования показали положительную корреляцию между mGR-положительными клетками и активностью, связанной с заболеванием. [15] В настоящее время нет доказанных сигнальных путей, связанных с mGR. Некоторые исследователи предполагают, что высокая активность заболевания активирует экспрессию mGR и при введении метилпреднизолона создает петлю отрицательной обратной связи, вызывая апоптоз. [15]
Высокие концентрации интеркалата метилпреднизолона в плазме и митохондриальных клеточных мембранах. Эта ассоциация изменяет физико-химические свойства мембраны; активируя мембранные белки, изменяя клеточные функции и в конечном итоге влияя на транспорт катионов через плазматическую мембрану и стимулируя утечку протонов через внутреннюю митохондриальную мембрану. [13] [15] Затрудненное окислительное фосфорилирование ставит под угрозу производство АТФ, основного источника энергии для клеточного энергетического метаболизма и иммунной функции. Исследования in vivo стимулированных Con-A тимоцитов (у крыс) и иммунных клеток человека, которым вводили высокие дозы метилпреднизолона, показали, что они ингибируют дыхание дозозависимым образом, ингибируют поглощение кальция и натрия в плазме и повышают концентрацию кальция в цитоплазме. [15]Суммирующий процесс выглядит следующим образом: метилпреднизолон интеркалирует в плазматическую мембрану, вызывает физико-химические изменения, активирует мембранные белки, которые ингибируют поглощение кальция и натрия в плазме (имитируя состояние дефицита энергии). Снижается потребление АТФ (это напоминает угнетенное дыхание), что приводит к проницаемости белка на внутренней митохондриальной мембране и разобщению окислительного фосфорилирования. Примечательно, что синтез ДНК / РНК не был затруднен. [15] Зависимость клеток домашнего хозяйства и иммунных клеток от АТФ приводит к иммуносупрессии во время дефицита АТФ. Специфические иммунные функции, на которые влияет этот процесс, включают цитокинез, миграцию, фагоцитоз, процессинг и представление антигена, синтез антител, цитотоксичность и регуляцию. [15]
Ось HPA [ править ]
Активация гипоталамо-гипофизарной оси (ось HPA) стимулирует выработку эндогенных глюкокортикоидов в коре надпочечников. [12] Ось HPA интерпретирует стимулы (стресс, воспаление и циркадные сигналы) и преобразует соответствующий физико-химический ответ. [4] Глюкокортикоиды, высвобождаемые в кровь, служат посредником, связываясь с рецепторами глюкокортикоидов, широко распространенными по всему телу, включая саму ось HPA. [12] Таким образом, физиологический диапазон GC контролируется петлей отрицательной обратной связи GC, воздействующей на любую часть оси HPA. [4] Метилпреднизолон структурно и функционально имитирует эндогенные кортикоиды и действует аналогичным образом на ось HPA.
Фармакокинетика [ править ]
Метилпреднизолон разрешен для перорального и родительского применения. Метилпреднизолон (Медрол) для перорального применения доступен в форме таблеток с дозировкой 2 мг, 4 мг, 8 мг, 16 мг или 32 мг. [19] И метилпреднизолона ацетат (Depo-Medrol), и метилпреднизолона сукцинат (Solu-Medrol) одобрены для внутримышечной инъекции. [20] [21] Депо-Медрол дополнительно одобрен для инъекций в очаг поражения, внутрисуставных и мягких тканей. Депо-Медрол доступен в виде стерильного водного раствора с концентрацией 20 мг / мл, 40 мг / мл или 80 мг / мл. [20]Solu-Medrol - единственное производное метилпреднизолона, одобренное для внутривенного вливания, поскольку стерильный порошок растворим в воде и может быть смешан с разбавителем. Сила варьируется от 40 мг до 2 г. [21]
Синтетические глюкокортикоиды сходны с эндогенными стероидами в метаболизме, но различаются по сродству к глюкокортикоидным и минералокортикоидным рецепторам, сродству к связыванию с белками, скорости выведения и продуктам метаболизма. [2]
При пероральном приеме метилпреднизолон легко всасывается из желудочно-кишечного тракта с биодоступностью 89,9%. [22] В отличие от эндогенных ГК, метилпреднизолон не связывается с гликопротеином транскортином (кортикостероидсвязывающим глобулином, CBG), но имеет умеренное связывание белка с альбумином. [13] Таким образом, фармакокинетика метилпреднизолона линейна и не зависит от дозы. [13] Пациенты с низкой концентрацией альбумина подвергаются риску побочных эффектов при терапии глюкокортикоидами. [13] Оральный метилпреднизолон имеет умеренное распределение в тканях в концентрации 1,38 л / кг. [23]
Метилпреднизолон в первую очередь выводится метаболизмом в печени и почечной экскрецией метаболитов; с почечной экскрецией неизмененного метилпреднизолона всего 1,3–9,2%. [23] Метилпреднизолон может взаимно превращаться с метилпреднизоном. [13] Печеночный метаболизм опосредуется 11 бета-гидроксистероиддегидрогеназами (11β-HSD) и 20-кетостероидредуктазами. [23] Метилпреднизолон подвергается почечной экскреции гидрофильных неактивных метаболитов, включая 20-карбоксиметилпреднизолон и 6β-гидрокси-20α-гидроксиметилпреднизолон. [13]
| Синтетический глюкокортикоид | Эквивалентная доза (мг) | Противовоспалительная активность 1 | Минералокортикоидная активность 1 | Биологический период полураспада (часы) | Рекомендации |
|---|---|---|---|---|---|
| Глюкокортикоиды короткого и среднего действия | |||||
| Гидрокортизон | 20 | 1 | 1 | 8–12 | [2] [7] |
| Кортизон | 25 | 0,8 | 0,8 | 8–12 | [2] [7] |
| Преднизон | 5 | 4 | 0,3 | 12–36 | [2] [7] |
| Преднизолон | 5 | 4–5 | 0,3 | 12–36 | [2] [7] |
| Метилпреднизолон | 4 | 5 | 0,25-0,5 | 12–36 | [2] [7] |
| Мепреднизон | 4 | 5 | 0 | [2] | |
| Глюкокортикоиды средней продолжительности действия | |||||
| Триамцинолон | 4 | 5 | 0 | 12–36 | [2] [7] |
| Параметазон | 2 | 10 | 0 | Нет данных | [2] [7] |
| Флупреднизолон | 1.5 | 15 | 0 | [2] | |
| Глюкокортикоиды длительного действия | |||||
| Бетаметазон | 0,6 | 25-40 | 0 | 36-72 | [2] [7] [24] |
| Дексаметазон | 0,75 | 30 | 0 | 36-72 | [2] [7] |
| Минералокортикоиды | |||||
| Флудрокортизон | 2 | 10 | 250 | 18–36 | [2] [7] |
| Дезоксикортикостерона ацетат | 0 | 20 | |||
Медицинское использование [ править ]
Как указывалось ранее, основное применение метилпреднизолона - подавление воспалительных и иммунных реакций. Метилпреднизолон достигает этого, прежде всего, регулируя количество и функцию лейкоцитов, цитокинов и хемокинов. [2] Его широко распространенный контроль воспаления способствует применению при множественных заболеваниях независимо от патологии. [2] Метилпреднизолон обычно назначают в качестве краткосрочной терапии острых обострений, как при остром подагрическом артрите. Его можно назначать во время продолжающейся терапии в более низких дозах при условии наблюдения за побочными эффектами. [3] Дозировка и состав оптимизированы для медицинского применения. [4]
Астма [ править ]
В 2001–2002 гг. 11,4% пациентов с диагнозом астма, осмотренных на амбулаторном лечении, получали пероральные кортикостероиды в качестве долгосрочной контрольной терапии. [25] Национальная программа обучения и профилактики астмы (NAEPP) указывает, что системный метилпреднизолон как в краткосрочной, так и в долгосрочной терапии позволяет быстро контролировать и подавлять стойкую астму, соответственно. [26] При обострениях, которые приводят к обращению в отделение неотложной помощи (ED), пероральный метилпреднизолон предпочтительнее внутривенного введения, если нет проблем с соблюдением режима лечения или рвотой. [26] [27] Пероральный метилпреднизолон менее инвазивен, и исследования показали, что его эффективность эквивалентна эффективности метилпреднизолона внутривенно. [26] [27] Дозировка выше 60–80 мг / день или 2 мг / кг / день не рекомендуется, поскольку не было показано, что она влияет на легочную функцию, частоту госпитализаций или продолжительность пребывания в больнице по сравнению с более низкими дозами. [27] После выписки из ЭД рекомендуется назначить пятидневный курс метилпреднизолона, чтобы снизить вероятность рецидива или абстинентного синдрома. [26] [27]
Ревматические заболевания [ править ]
Метилпреднизолон используется для лечения нескольких ревматических заболеваний, таких как системная красная волчанка (СКВ) и ревматоидный артрит (РА). Дозировка и введение метилпреднизолона при этих заболеваниях сильно различаются из-за различной патофизиологии между заболеваниями и пациентами, у которых диагностировано данное заболевание. [28] [29] При волчаночном нефрите, частом проявлении СКВ, пациентам часто назначают метилпреднизолон одновременно с иммунодепрессантами. Тяжелые проявления часто лечат циклофосфамидом или ритуксимабом и тремя дозами метилпреднизолона внутривенно пульс (в соответствии с рекомендациями ACR) до перехода на пероральный преднизолон и азатиоприн для поддерживающей терапии. [28] [29]
Внутрисуставные инъекции кортикостероидов (IACI) - это терапия второй линии для облегчения боли в суставах, вызванной ревматоидным артритом. [30] Чаще всего вводят в коленные и плечевые суставы. [30] Хотя инъекции являются местными, исследования показали системное всасывание, что подтверждается благотворным воздействием на отдаленные суставы. [30] В попытке свести к минимуму подавление HPA руководство FDA ограничило IACI до трех в год с минимальным интервалом 30 дней между инъекциями. [31]
Первичная или вторичная недостаточность коры надпочечников [ править ]
Метилпреднизолон обычно не рекомендуется при первичной или вторичной недостаточности коры надпочечников по сравнению с другими кортикостероидами, которые обладают более высоким сродством к рецепторам минералокортикоидов и удерживают соли. [2]
Маркированные показания [ править ]
Указанные ниже показания сгруппированы по способу введения, а затем по медицинской дисциплине.
Пероральный метилпреднизолон [ править ]
- Аллергия и иммунология: ангионевротический отек , [26] астма , крапивница , сезонный или постоянный аллергический ринит, реакции гиперчувствительности к лекарствам и сывороточная болезнь . [19]
- Дерматология: токсический эпидермальный некролиз [26], атопический дерматит , контактный дерматит , пузырчатка , мультиформная эритема , синдром Стивена-Джонсона , герпетиформный буллезный дерматит, тяжелый себорейный дерматит , эксфолиативный дерматит, грибовидный микоз и тяжелый псориаз . [19]
- Эндокринология: врожденная гиперплазия надпочечников , гиперкальциемия, связанная с раком , негнойный тиреоидит, а также первичная или вторичная недостаточность коры надпочечников . [19]
- Гастроэнтерология: воспалительные заболевания кишечника и язвенный колит . [19]
- Гематология: приобретенная (аутоиммунная) гемолитическая анемия , идиопатическая тромбоцитопеническая пурпура , вторичная тромбоцитопения, эритробластопения, лейкемия , лимфома и врожденная (эритроидная) гипопластическая анемия. [19]
- Легочные: аспирационный пневмонит , хроническая бериллиевая болезнь , эозинофильная пневмония , симптоматический саркоидоз и туберкулез легких в сочетании с противотуберкулезной химиотерапией. [19]
- Нефрология: нефротический синдром идиопатического типа или вторичный по отношению к волчаночному нефриту . [19]
- Неврология: рассеянный склероз . [19]
- Офтальмология: склерит , васкулит сетчатки , [26] увеит , хориоидит, ирит, иридоциклит, кератит , неврит зрительного нерва , аллергический конъюнктивит , аллергические язвы на краях роговицы, опоясывающий герпес офтальмоза , симпатический офтальмия и хориоретинит. [19]
- Ревматология: ревматоидный артрит , ревмокардит , острый подагрический артрит , анкилозирующий спондилоартрит , дерматомиозит и полимиозит , псориатический артрит , системная красная волчанка , острый и подострый бурсит , синовит остеоартрит, посттравматический остеоартрит, и эпикондилит . [19]
- Прочее: трихинеллез с неврологическим поражением или поражением миокарда. [19]
Парентеральный метилпреднизолон [ править ]
- Внутрисуставные инъекции или инъекции мягких тканей: острый подагрический артрит, острый и подострый бурсит, острый теносиновит, эпикондилит и синовит остеоартрита. [29]
- Intralesional инъекции: алопеция , дискоидная красная волчанка , келоиды , гранулема кольцевидная , красный плоский лишай , простой лишай Chronicus , псориазе, некробиоз липоидный diabeticorum . [29]
- Внутримышечные инъекции назначают для лечения многих из тех же состояний, которые указаны для перорального приема. Внутримышечные инъекции применяются как альтернатива пероральной терапии. [29]
Показания вне лейбла [ править ]
Некоторые из показаний к применению метилпреднизолона не по прямому назначению включают острое повреждение спинного мозга , острый респираторный дистресс-синдром , алкогольный гепатит , гормональную реанимацию при восстановлении трупных органов и хроническую обструктивную болезнь легких . [26]
Доступные формы [ править ]
| Активный компонент | Имя бренда | ROA | Форма | Сила 1 | Неактивные Ингридиенты |
|---|---|---|---|---|---|
| метилпреднизолон | Медрол | Устный | планшет | 2, 4, 8, 16, 32 мг | стеарат кальция, кукурузный крахмал, лактоза, минеральное масло, сорбиновая кислота, сахароза и эритрозин натрия (только 2 мг), желтый FD&C № 6 (только 8 и 32 мг) |
| метилпреднизолон | Медрол | Устный | планшет | 4 мг; 21 таблетка (доза-упаковка) | стеарат кальция, кукурузный крахмал, лактоза, сахароза |
| метилпреднизолона ацетат | Депо-Медрол | Парентерально: внутрисуставные или мягкие ткани, внутриочаговые или внутримышечные | приостановка | 20, 40, 80 мг / мл | Полиэтиленгликоль 3350, полисорбат 80, одноосновный фосфат натрия, двухосновный фосфат натрия USP, бензиловый спирт 2 добавлены в качестве консерванта. |
| метилпреднизолона ацетат 3 | Депо-Медрол | Парентерально: внутрисуставные или мягкие ткани, внутриочаговые или внутримышечные | приостановка | 40 или 80 мг / мл (флакон с однократной дозой) | Полиэтиленгликоль 3350 Миристил-гамма-пиколиния хлорид |
| метилпреднизолона сукцинат | Солю-Медрол | Парентерально: внутривенно или внутримышечно | раствор, восстановленный | 500, 1000, 2000 мг / флакон, 2000 мг с разбавителем (многодозовый флакон) | безводный одноосновный фосфат натрия, высушенный двухосновный фосфат натрия и водная лактоза. Бактериостатическая вода добавлена в качестве разбавителя с добавлением бензилового спирта 2 в качестве консерванта. |
| метилпреднизолона сукцинат 3 | Солю-Медрол | Парентерально: внутривенно или внутримышечно | раствор, восстановленный | 40, 125, 500, 1000 мг / флакон (флакон для разовой дозы) | безводный одноосновный фосфат натрия, высушенный двухосновный фосфат натрия и водная лактоза. |
Сноски:
1 Означает различную силу доступных форм. Не является показателем частоты или суточной кумулятивной дозы; варьируется в зависимости от пациента и состояния.
2 Бензиловый спирт не следует использовать новорожденным
3 Состав без консервантов
Противопоказания [ править ]
Метилпреднизолон не следует принимать перорально людям с системными грибковыми инфекциями, за исключением Депо-Медрола, который вводится в виде внутрисуставной инъекции при локализованных состояниях суставов. [20] Метилпреднизолон противопоказан людям с известной гиперчувствительностью к метилпреднизолону или его компонентам. [19] Стероиды следует применять с осторожностью у пациентов с язвенным колитом, сердечными заболеваниями или гипертонией, язвенной болезнью, почечной недостаточностью, остеопорозом, миастенией, глаукомой и сахарный диабет. [2] [19]При приеме метилпреднизолона могут появиться психические проявления, от эйфории, бессонницы, изменений личности до депрессии. С осторожностью следует относиться к пациентам с предрасположенными психозами, так как при приеме кортикостероидов психотические тенденции могут усиливаться. [19]
Дозировка Solu-Medrol 40 мг содержит моногидрат лактозы, произведенный из коровьего молока; Его не следует принимать лицам с известной гиперчувствительностью к молочным продуктам или их компонентам. [21] Тяжелые медицинские события были связаны с эпидуральным введением Solu-Medrol и Depo-Medrol, включая инфаркт спинного мозга, параплегию, квадриплегию, корковую слепоту и инсульт. Внутримышечные инъекции не следует вводить пациентам с идиопатической тромбоцитопенической пурпурой. Составы Solu-Medrol и Depo-Medrol, содержащие бензиловый спирт, противопоказаны для использования у недоношенных детей. [21] Воздействие чрезмерного количества бензилового спирта на нервную ткань было связано с токсичностью и в редких случаях приводило к смерти. [20]
Побочные реакции [ править ]
Побочные реакции могут затмевать терапевтические эффекты метилпреднизолона. [7]
Центральная нервная система [ править ]
Существует минимальный клинический диагностический критерий для определения психических побочных эффектов (PAE), связанных с использованием метилпреднизолона у пациентов с системной красной волчанкой (SLE). [24] Распространенность колеблется от 1,3 до 62% среди взрослых пациентов, получавших лечение. [24] Тип и тяжесть психоневрологических симптомов также значительно различаются между пациентами: 33% пациентов сообщают о ЛАЭ от легкой до умеренной, а 5-10% - о тяжелой. [24] Доза и продолжительность приема метилпреднизолона влияют на развитие ПАЭ. 20 мг / день преднизона (16 мг / день метилпреднизолона) - это пороговая доза для развития ПАЭ, согласованная во многих исследованиях. [24]Краткосрочная пульс-внутривенная терапия в высоких дозах связана с быстрым началом маниакальных и гипоманиакальных симптомов, тогда как длительная терапия вызывает депрессивные симптомы (попытки суицида случаются нечасто). [24] PAE обратимы при сокращении или прекращении лечения. [24]
Метаболические и эндокринные [ править ]
Ятрогенный синдром Кушинга является прямым осложнением терапии глюкокортикоидами и наиболее частой причиной экзогенного синдрома Кушинга. [32] Клинические признаки синдрома Кушинга включают множество побочных эффектов при терапии глюкокортикоидами. [32] Традиционные симптомы включают прибавку в весе, миопатию, остеопороз, повышенный риск инфекции, гипертонию и психологический эффект. Отложение жира происходит централизованно на туловище, между плечами («буйволиный горб») и на лице («лунное лицо»). [32] Обучение пациентов и наблюдение за медицинским работником - первый шаг в распознавании и диагностике ятрогенного синдрома Кушинга. Экзогенные глюкокортикоиды подавляют адренокортикотропный гормон(ATCH), что может быть подтверждено биохимическим анализом AM. [32] Начало побочных эффектов варьируется; нейропсихиатрические симптомы могут возникнуть в течение нескольких часов, тогда как остеопороз может развиться через несколько месяцев. [32]
Метаболические эффекты от приема метилпреднизолона включают непрерывное расщепление белков для глюконеогенеза, увеличение потребности в инсулине. Это приводит к гиперлипидемии, увеличению веса, миопатии, что может побудить пациента обратиться за лечением. [2]
Инфекции [ править ]
- См .: Глюкокортикоиды § Иммунодефицит.
В разделе «Иммунодефицит» перечислены известные патогены, вызывающие обеспокоенность при иммунодефиците, вызванном глюкокортикоидами.
Скелетно-мышечный [ править ]
Остеопороз - это тип заболевания костей, характеризующийся потерей плотности, массы и архитектуры костей, что делает пациента уязвимым к переломам. [33] Всемирная организация здравоохранения (ВОЗ) определяет остеопороз у кавказских женщин в постменопаузе как минеральную плотность костной ткани (МПК) и Т-балл -2,5 или меньше. [18] [34] Распространенность остеопороза у пациентов с СКВ варьируется по географическому признаку, и некоторые связывают это с диагностической целесообразностью МПК и Т-показателя. [18] Британцы 10,3%, китайцы 21,7% Канадские клинические практические рекомендации и Американский колледж ревматологии перешли на использование Z-балла в качестве диагностического маркера остеопороза, но не смогли определить порог клинической диагностики. [18]Кроме того, исследование в Великобритании показало, что МПК может не соответствовать пациенту с СКВ, поскольку его риск переломов на 22% выше, чем у здорового человека. [18]
Экзогенные кортикостероиды вызывают остеопороз, увеличивая резорбцию кости и уменьшая образование костной ткани. [18] Потеря костной массы может быть выражена в течение первых нескольких месяцев после начала приема метилпреднизолона с устойчивым снижением при постоянном применении. Потеря трабекулярной кости в поясничном отделе позвоночника предшествует потере кортикальной кости в шейке бедра. [18]
Исчерпывающий список [ править ]
Аллергические: аллергические реакции или реакции гиперчувствительности, анафилактоидные реакции, анафилаксия и крапивница. [19]
Сердечно-сосудистые: гипертензия, застойная сердечная недостаточность у восприимчивых пациентов [19], преждевременное атеросклеротическое заболевание, аритмии и возможная гиперлипидемия. [32]
Дерматологические: нарушение заживления ран, петехии и экхимозы, истончение кожи, эритема лица и повышенное потоотделение. [19]
Эндокринные: кушингоидные особенности, подавление роста у детей, вторичная адренокортикальная и гипофизарная невосприимчивость, нарушения менструального цикла, пониженная непереносимость углеводов и латентный сахарный диабет. У пациентов с сахарным диабетом повышенная потребность в инсулине или пероральных гипогликемических средствах. [19]
Нарушения жидкости и электролитов: задержка натрия, задержка жидкости, потеря калия, гипокалиемический алкалоз или застойная сердечная недостаточность у восприимчивых пациентов. [19]
Со стороны желудочно-кишечного тракта: язвенная болезнь, панкреатит, вздутие живота и язвенный эзофагит. [19]
Метаболический: катаболизм белков, вызывающий отрицательный азотистый баланс. [19]
Со стороны скелетно-мышечной системы: мышечная слабость, потеря мышечной массы, стероидная миопатия, остеопороз, разрыв сухожилий (особенно ахиллова), компрессионные переломы позвонков, асептический некроз головки бедренной и плечевой кости и патологический перелом длинных костей. [19]
Неврологические: повышение внутричерепного давления с отеком диска зрительного нерва, судороги, головокружение и головная боль. [19]
Офтальмологические: задняя субкапсулярная катаракта, повышение внутриглазного давления, глаукома и экзофтальм. [19]
Снятие [ править ]
Обратная связь экзогенных глюкокортикоидов по оси гипоталамус-гипофиз-надпочечники (HPA) подавляет секрецию кортикотропин-рилизинг-гормона (CRH) и адренокортикотропного гормона (ATCH) в гипоталамусе и гипофизе соответственно. [35] Длительное подавление приводит к неадекватной реакции на физические и эмоциональные стрессы, такие как болезни и травмы. [35] Подавление ATCH может привести к гипоплазии надпочечников или вторичной атрофии надпочечников в течение 6 недель терапии метилпреднизолоном, подвергая пациента риску развития угрожающего жизни криза надпочечниковой недостаточности. [7] [35]Факторы, которые влияют на степень подавления оси HPA, включают активность стероидных гормонов (тип соединения и способ введения), кумулятивную дозу, продолжительность лечения и сопутствующее применение лекарств. [7] Любой человек, принимавший стероидные гормоны в течение 2+ недель, подвержен риску развития подавления оси HPA. [35] • Системный риск применения метилпреднизолона был отмечен как умеренный в классе синтетических глюкокортикоидов. [35]
Перед прекращением приема метилпреднизолона по любой причине проконсультируйтесь с врачом. [36] Резкое прекращение приема препарата обычно вызывает преходящие неспецифические симптомы, такие как потеря аппетита, расстройство желудка, рвота, сонливость, спутанность сознания, головная боль, жар, боли в суставах и мышцах, шелушение кожи и потеря веса. [35] [36] Эти симптомы могут быть связаны с синдромом отмены стероидов, надпочечниковой недостаточностью или рецидивом заболевания. [35] Тем, кто принимал метилпреднизолон в качестве длительного лечения, можно постепенно снизить дозу, чтобы минимизировать симптомы отмены и вероятность рецидива. [36] [35] При обострении симптомов временное повышение дозировки метилпреднизолона показало клиническую значимость.[35] Исследования, в которых проводилось повторное тестирование пациентов после отмены метилпреднизолона, показали стойкую надпочечниковую недостаточность, при этом одно исследование показало 15% через 3 года. [7] [37] Тем не менее, наблюдался широкий диапазон распространенности и отсутствие единообразия в сроках наблюдения. [37]
Взаимодействие с лекарствами [ править ]
Следует соблюдать осторожность при одновременном приеме метилпреднизолона с лекарствами, описанными ниже.
Индукторы ферментов
Все препараты, относящиеся к классу индукторов ферментов, увеличивают клиренс и уменьшают период полувыведения метилпреднизолона при совместном применении. [13] Фенобарбитал , фенитоин , рифампицин , карбамазепин и барбитураты увеличивают печеночные ферменты и скорость их выведения, тем самым снижая иммуносупрессивный эффект метилпреднизолона. [13] Для достижения желаемого эффекта метилпреднизолона могут потребоваться повышенные дозировки. [13]
Ингибиторы цитохрома P450 (CYP) 3A4
Тролеандомицин , кетоконазол и кларитромицин подавляют метаболизм; и может снизить скорость выведения и увеличить период полувыведения метилпреднизолона. [19] [13] Дозировки следует соответственно уменьшить, чтобы избежать побочных эффектов. Другой ингибитор CYP 3A4, грейпфрутовый сок, продлевает период полувыведения перорального метилпреднизолона. [13]
Оральные контрацептивы
Оральные контрацептивы подавляют окислительные процессы, о чем свидетельствует их способность уменьшать клиренс метилпреднизолона. [13]
Ингибиторы Р-гликопротеина
Показано, что метилпреднизолон является субстратом Р-гликопротеина; Считается, что его ингибирование увеличивает всасывание и распределение метилпреднизона. Никакой клинической значимости не установлено. [13]
Циклоспорин, такролимус, сиролимус (рапамицин)
Метилпреднизолон и циклоспорин подавляют метаболизм и, следовательно, повышают вероятность возникновения побочных эффектов, связанных с любым из отдельных препаратов. Помимо известных индивидуальных побочных эффектов сообщалось о судорогах. [19]
Ингибиторы ЦОГ1
Метилпреднизолон может увеличивать скорость выведения при хроническом приеме высоких доз аспирина . Пациенты подвержены повышенному уровню салицилата в сыворотке крови или токсичности салицилата после прекращения приема метилпреднизолона. Следует соблюдать особую осторожность при назначении метилпреднизолона и аспирина пациентам с гипопротромбинемией . [19]
Антикоагулянты
Антикоагулянты проявляют различные взаимодействия; Для достижения желаемого эффекта рекомендуется мониторинг показателей коагуляции. [19]
Физические свойства [ править ]
Пероральный метилпреднизолон (Медрол) и его производные представляют собой белый кристаллический порошок без запаха. Его растворимость варьируется от практически нерастворимого в воде, очень мало растворимого в эфире, хорошо растворимого в ацетоне и хлороформе до умеренно растворимого в спирте, диоксане и метаноле. [38] Суспензия метилпреднизолона ацетата (Depo-Medrol) представляет собой 6-метилпроизводное преднизолона, которое плавится при 215 градусах Цельсия с некоторым разложением. [20] Метилпреднизолон натрия сукцинат (Solu-Medrol) представляет собой натрийсукцинатный эфир метилпреднизолона. В отличие от растворимости, указанной выше, сукцинат метилпреднизолона натрия растворим в воде и спирте, слабо растворим в ацетоне и нерастворим в хлороформе [21].
Химические свойства [ править ]
Метилпреднизолон, или 6α-метилпреднизолон, также известный как 11 & beta, 17,21-тригидрокси-6α-метилпрегна-1,4-диен-3,20-дион, является синтетическим прегнан стероидом и производный от гидрокортизона (11 & beta ; , 17 & alpha ; , 21 -тригидроксипрегн-4-ен-3,20-дион) и преднизолон (11β, 17α, 21-тригидроксипрегн-1,4-диен-3,20-дион). [39] [40] Существует множество сложных эфиров метилпреднизолона с различными характеристиками, которые продаются для медицинского использования. [39] [40] Они включают метилпреднизолона ацепонат (Адвантан), метилпреднизолона ацетат (Депо-Медрол),метилпреднизолона сукцинат (Solu-Medrol) и сулептанат метилпреднизолона (Medrosol, Promedrol). [39] [40]
Синтез [ править ]
Синтетические стероиды синтезируются из холевой кислоты и сапогенинов, полученных от крупного рогатого скота и растений соответственно. [2]
История, общество и культура [ править ]
Метилпреднизолон был впервые синтезирован и произведен компанией Upjohn (ныне Pfizer) и Управлением по контролю за продуктами и лекарствами (FDA), одобренным в США 2 октября 1957 г. [8] Срок действия патента истек, и теперь доступны генерики. В 2021 году он занимает 153-е место среди наиболее часто назначаемых лекарств в Соединенных Штатах, на него выписано более четырех миллионов рецептов. [41] По сравнению с 2017 годом, он поднялся на четыре позиции в рейтинге. Метилпреднизолон назначали в качестве лекарственного средства во время пандемии COVID-19 [42] [43]
Ссылки [ править ]
- ^ a b «Использование метилпреднизолона во время беременности» . Drugs.com . 20 августа 2019 . Проверено 20 февраля 2020 года .
- ^ Б с д е е г ч я J к л м п о р д т ы т у V Katzung BG, Masters SB, Тревор AJ (2012). Фундаментальная и клиническая фармакология (12-е изд.). Нью-Йорк: McGraw-Hill Medical. ISBN 978-0-07-176401-8. OCLC 761378641 .
- ^ Б с д е е г ч Timmermans S, Souffriau J, Libert C (2019). «Общее введение в биологию глюкокортикоидов» . Границы иммунологии . 10 : 1545 DOI : 10,3389 / fimmu.2019.01545 . PMC 6621919 . PMID 31333672 .
- ^ a b c d e f g h i j Xavier AM, Anunciato AK, Rosenstock TR, Glezer I (2016). «Контроль экспрессии генов глюкокортикоидными рецепторами во время врожденных иммунных ответов» . Границы эндокринологии . 7 : 31. DOI : 10,3389 / fendo.2016.00031 . PMC 4835445 . PMID 27148162 .
- ^ Ocejo А, Корреа R (2020). «Метилпреднизолон». StatPearls . Остров сокровищ (Флорида): StatPearls Publishing. PMID 31335060 . Проверено 10 ноября 2020 .
- ↑ Хабиб Г.С. (июль 2009 г.). «Системные эффекты внутрисуставных кортикостероидов». Клиническая ревматология . 28 (7): 749–56. DOI : 10.1007 / s10067-009-1135-х . PMID 19252817 . S2CID 5645348 .
- ^ a b c d e f g h i j k l m n o p q r s t Paragliola RM, Papi G, Pontecorvi A, Corsello SM (октябрь 2017 г.). «Лечение синтетическими глюкокортикоидами и оси гипоталамус-гипофиз-надпочечники» . Международный журнал молекулярных наук . 18 (10): 2201. DOI : 10,3390 / ijms18102201 . PMC 5666882 . PMID 29053578 .
- ^ a b «Лекарства @ FDA: лекарства, одобренные FDA» . www.accessdata.fda.gov . Проверено 5 декабря 2020 .
- ^ «Топ 300 2021 года» . Clincalc.com . Проверено 5 декабря 2020 .
- ^ Косака М, Ямадзаки Y, Maruno Т, Сакагучи К, Саваки S (январь 2021 года). «Кортикостероиды в качестве дополнительной терапии при лечении коронавирусной болезни 2019: отчет о двух случаях и обзор литературы» . Журнал инфекций и химиотерапии . 27 (1): 94–98. DOI : 10.1016 / j.jiac.2020.09.007 . PMC 7480527 . PMID 32988730 .
- ^ Yousefifard МЫ, Мохамед Али К, Aghaei А, Зали А, Мадань Neishaboori А, Zarghi А, и др. (Август 2020 г.). «Кортикостероиды в лечении коронавирусной болезни 2019 (COVID-19): системный обзор и метаанализ» . Иранский журнал общественного здравоохранения . 49 (8): 1411–1421. DOI : 10.18502 / ijph.v49i8.3863 . PMC 7554375 . PMID 33083317 .
- ^ a b c d e Cain DW, Cidlowski JA (апрель 2017 г.). «Иммунная регуляция глюкокортикоидами». Обзоры природы. Иммунология . 17 (4): 233–247. DOI : 10.1038 / nri.2017.1 . PMID 28192415 . S2CID 47176122 .
- ^ a b c d e f g h i j k l m n o p q r Czock D, Keller F, Rasche FM, Häussler U (2005). «Фармакокинетика и фармакодинамика глюкокортикоидов, применяемых системно». Клиническая фармакокинетика . 44 (1): 61–98. DOI : 10.2165 / 00003088-200544010-00003 . PMID 15634032 . S2CID 24458998 .
- ^ а б Кино Т., Хрусос Г.П. Опосредованная ацетилированием эпигенетическая регуляция активности глюкокортикоидных рецепторов: связанные с циркадным ритмом изменения действий глюкокортикоидов в тканях-мишенях. Mol Cell Endocrinol . 2011; 336 (1-2): 23-30. DOI: 10.1016 / j.mce.2010.12.001
- ^ a b c d e f g h i j k Song IH, Buttgereit F (февраль 2006 г.). «Негеномные эффекты глюкокортикоидов, чтобы обеспечить основу для новых разработок лекарств». Молекулярная и клеточная эндокринология . 246 (1–2): 142–6. DOI : 10.1016 / j.mce.2005.11.012 . PMID 16388891 . S2CID 40239838 .
- ^ Panettieri Р.А., Schaafsma D, Амраните Y, Koziol-белый С, Острое R, Tliba O (январь 2019). «Негеномные эффекты глюкокортикоидов: обновленный взгляд» . Направления фармакологических наук . 40 (1): 38–49. DOI : 10.1016 / j.tips.2018.11.002 . PMC 7106476 . PMID 30497693 .
- ^ a b Stahn C, Buttgereit F (октябрь 2008 г.). «Геномные и негеномные эффекты глюкокортикоидов». Природа Клиническая практика. Ревматология . 4 (10): 525–33. DOI : 10,1038 / ncprheum0898 . PMID 18762788 . S2CID 22686260 .
- ^ a b c d e f g h Пханг К.Ф., Чо Дж, Ли В., Мак А (2018). «Глюкокортикоид-индуцированный остеопороз при системной красной волчанке» . Ревматологическая практика и исследования . 3 : 205990211880251. DOI : 10,1177 / 2059902118802510 .
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad "Медрол США, выписывающая информацию для врача" . ООО «Компания Пфайзер и Апджон» . 2019-02-01 . Проверено 10 ноября 2020 .
- ^ a b c d e "Многодозовый флакон DEPO-MEDROL, информация о назначении врача в США" . Pfizer. Июль 2018 г.
- ^ a b c d e f "Многодозовый флакон СОЛУ-МЕДРОЛ, прописанный врачом в США" . Pfizer. Сентябрь 2020 г.
- ^ Garg DC, Вагнер JG, Сакмар E, Weidler DJ, Альберт KS (август 1979). «Ректальное и пероральное всасывание метилпреднизолона ацетата». Клиническая фармакология и терапия . 26 (2): 232–9. DOI : 10.1002 / cpt1979262232 . ЛВП : 2027,42 / 117227 . PMID 455892 . S2CID 28001411 .
- ^ a b c Szefler SJ, Ebling WF, Georgitis JW, Jusko WJ (1986). «Метилпреднизолон по сравнению с фармакокинетикой преднизолона в зависимости от дозы для взрослых». Европейский журнал клинической фармакологии . 30 (3): 323–9. DOI : 10.1007 / BF00541537 . PMID 3732369 . S2CID 21550959 .
- ^ Б с д е е г Fietta P, P Fietta, Delsante G (октябрь 2009 г.). «Влияние природных и синтетических глюкокортикоидов на центральную нервную систему» . Психиатрия и клинические неврологии . 63 (5): 613–22. DOI : 10.1111 / j.1440-1819.2009.02005.x . PMID 19788629 . S2CID 28778979 .
- ^ Национальный центр статистики здравоохранения. Здравоохранение, США, 2004 г. С таблицей тенденций в области здоровья американцев. Хяттсвилл, Мэриленд: 2004 г. https://www.cdc.gov/nchs/data/hus/hus04.pdf
- ^ a b c d e f g h Национальная программа обучения и профилактики астмы (ноябрь 2007 г.). «Отчет экспертной комиссии 3 (EPR-3): Руководство по диагностике и лечению астмы - Сводный отчет 2007» (PDF) . Журнал аллергии и клинической иммунологии . 120 (5 Suppl): S94–138. DOI : 10.1016 / j.jaci.2007.09.043 . PMID 17983880 .
- ^ а б в г Алангари AA (июль 2010 г.). «Геномное и негеномное действие глюкокортикоидов при астме» . Анналы торакальной медицины . 5 (3): 133–9. DOI : 10.4103 / 1817-1737.65040 . PMC 2930650 . PMID 20835306 .
- ↑ a b Каул А., Гордон С., Ворон М., Тома З., Уровиц МБ, ван Волленховен Р., Руис-Ирасторза Г., Хьюз Г. (2016). "Системная красная волчанка". Nat Rev Dis Primers . 2 : 16039. дои : 10.1038 / nrdp.2016.39 . PMID 27306639 . S2CID 2628865 .
- ^ Б с д е е Chan ТМ (январь 2015). «Лечение тяжелого волчаночного нефрита: новые горизонты». Обзоры природы. Нефрология . 11 (1): 46–61. DOI : 10.1038 / nrneph.2014.215 . PMID 25421826 . S2CID 19814440 .
- ^ a b c Хабиб, Г.С. Системные эффекты внутрисуставных кортикостероидов. Clin. Ревматол. 2009, 28, 749–756.
- ↑ Johnston PC, Lansang MC, Chatterjee S, Kennedy L (март 2015 г.). «Внутрисуставные инъекции глюкокортикоидов и их влияние на функцию гипоталамо-гипофизарно-надпочечниковой (HPA) оси». Эндокринная . 48 (2): 410–6. DOI : 10.1007 / s12020-014-0409-5 . PMID 25182149 . S2CID 207363039 .
- ^ Б с д е е Hopkins RL, Leinung MC (июнь 2005 г.). «Экзогенный синдром Кушинга и абстиненция глюкокортикоидов». Клиники эндокринологии и метаболизма Северной Америки . Синдром Кушинга. 34 (2): 371–84, ix. DOI : 10.1016 / j.ecl.2005.01.013 . PMID 15850848 .
- ^ "Обзор остеопороза | Национальный ресурсный центр по остеопорозу и родственным костным заболеваниям NIH" . www.bones.nih.gov . Проверено 7 декабря 2020 .
- Перейти ↑ Jeremiah MP, Unwin BK, Greenawald MH, Casiano VE (август 2015). «Диагностика и лечение остеопороза» . Американский семейный врач . 92 (4): 261–8. PMID 26280231 .
- ^ a b c d e f g h i Илиопулу А., Аббас А., Мюррей Р. (май 2013 г.). «Как справиться с отменой глюкокортикоидной терапии». Писатель . 24 (10): 23–9. DOI : 10.1002 / psb.1060 . S2CID 72082017 .
- ^ a b c «Метилпреднизолон» . Информация о лекарствах MedlinePlus . Национальная медицинская библиотека США. Сентябрь 2017 г.
- ^ а б Джозеф Р.М., Хантер А.Л., Рэй Д.В., Диксон В.Г. (август 2016 г.). «Системная глюкокортикоидная терапия и надпочечниковая недостаточность у взрослых: систематический обзор» . Семинары по артриту и ревматизму . 46 (1): 133–41. DOI : 10.1016 / j.semarthrit.2016.03.001 . PMC 4987145 . PMID 27105755 .
- ^ PubChem. «Метилпреднизолон» . pubchem.ncbi.nlm.nih.gov . Проверено 16 ноября 2020 .
- ^ a b c Elks J (14 ноября 2014 г.). Словарь лекарств: химические данные: химические данные, структуры и библиографии . Springer. С. 811–. ISBN 978-1-4757-2085-3.
- ^ a b c Номинальный индекс 2000: Международный справочник лекарств . Тейлор и Фрэнсис. 2000. С. 675–. ISBN 978-3-88763-075-1.
- ^ «Топ 300 2021 года» . Clincalc.com . Проверено 5 декабря 2020 .
- ^ Косака М, Ямадзаки Y, Maruno Т, Сакагучи К, Саваки S (январь 2021 года). «Кортикостероиды в качестве дополнительной терапии при лечении коронавирусной болезни 2019: отчет о двух случаях и обзор литературы» . Журнал инфекций и химиотерапии . 27 (1): 94–98. DOI : 10.1016 / j.jiac.2020.09.007 . PMC 7480527 . PMID 32988730 .
- ^ Yousefifard МЫ, Мохамед Али К, Aghaei А, Зали А, Мадань Neishaboori А, Zarghi А, и др. (Август 2020 г.). «Кортикостероиды в лечении коронавирусной болезни 2019 (COVID-19): системный обзор и метаанализ» . Иранский журнал общественного здравоохранения . 49 (8): 1411–1421. DOI : 10.18502 / ijph.v49i8.3863 . PMC 7554375 . PMID 33083317 .
Внешние ссылки [ править ]
- «Метилпреднизолон» . Информационный портал о наркотиках . Национальная медицинская библиотека США.
- "метилпреднизолон" на medicinenet.com