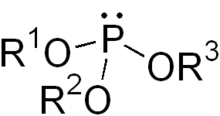
В химии сложный эфир фосфита или органофосфит обычно относится к фосфорорганическому соединению с формулой P (OR) 3 . Их можно рассматривать как сложные эфиры ненаблюдаемой таутомерной фосфористой кислоты , H 3 PO 3 , простейшим примером которой является триметилфосфит , P (OCH 3 ) 3 . Некоторые фосфиты можно рассматривать как сложные эфиры доминирующего таутомера фосфористой кислоты (HP (O) (OH) 2 ). Самый простой представитель - диметилфосфит с формулой HP (O) (OCH 3 ) 2. Оба класса фосфитов обычно представляют собой бесцветные жидкости.
Синтез [ править ]
- Из PCl 3
Сложные эфиры фосфористой кислоты , как правило , получают путем обработки трихлорида фосфора с алкоголем . В зависимости от деталей синтеза этот алкоголиз может давать диорганофосфиты: [1]
- PCl 3 + 3 C 2 H 5 OH → (C 2 H 5 O) 2 P (O) H + 2 HCl + C 2 H 5 Cl
Альтернативно, когда алкоголиз проводят в присутствии акцепторов протонов, получают C 3 -симметричные триалкоксипроизводные: [2]
- PCl 3 + 3 C 2 H 5 OH + 3 R 3 N → (C 2 H 5 O) 3 P + 3 R 3 NHCl
Получены многочисленные производные обоих типов фосфитов.
- Путем переэтерификации
Сложные эфиры фосфита также можно получить переэтерификацией , поскольку они претерпевают спиртовой обмен при нагревании с другими спиртами. [3] Этот процесс обратим и может использоваться для получения смешанных алкилфосфитов. В качестве альтернативы, если используется фосфит летучего спирта, такой как триметилфосфит , то побочный продукт ( метанол ) может быть удален перегонкой, позволяя довести реакцию до завершения.
Реакции и применение трис (органо) фосфитов [ править ]
Реакции [ править ]
 Трис (2,4-ди-трет-бутилфенил) фосфит , широко используемый стабилизатор в полимерах.
Трис (2,4-ди-трет-бутилфенил) фосфит , широко используемый стабилизатор в полимерах.
Фосфиты окисляются до фосфатных эфиров:
- P (ИЛИ) 3 + [O] → OP (ИЛИ) 3
Эта реакция лежит в основе коммерческого использования некоторых сложных эфиров фосфита в качестве стабилизаторов полимеров. [4]
Сложные эфиры алкилфосфита используются в реакции Перкова для образования винилфосфонатов и в реакции Михаэлиса-Арбузова для образования фосфонатов . Эфиры арилфосфита могут не вступать в эти реакции и поэтому обычно используются в качестве стабилизаторов в галогенсодержащих полимерах, таких как ПВХ .
Сложные эфиры фосфита могут использоваться в качестве восстановителей в более специализированных случаях. Например, известно , что триэтилфосфит восстанавливает некоторые гидропероксиды до спиртов, образующихся при автоокислении [5] ( схема ). В этом процессе фосфит превращается в сложный эфир фосфорной кислоты . Этот тип реакции также используется в полном синтезе таксола Вендера .
Гомогенный катализ [ править ]
Сложные эфиры фосфита являются основаниями Льюиса и, следовательно, могут образовывать координационные комплексы с ионами различных металлов. Типичные фосфитные лиганды включают триметилфосфит ((MeO) 3 P), триэтилфосфит ((EtO) 3 P), триметилолпропанфосфит и трифенилфосфит ((PhO) 3 P). Фосфиты демонстрируют меньшие углы конуса лиганда, чем структурно родственное семейство фосфиновых лигандов . Фосфитные лиганды являются компонентами промышленных катализаторов гидроформилирования и гидроцианирования . [6]
Химия HP (O) (OR) 2 [ править ]
- Состав диорганофосфита.
Диорганофосфиты являются производными фосфора (III) и могут рассматриваться как диэфиры фосфористой кислоты . Они демонстрируют таутомерию , однако равновесие в подавляющем большинстве случаев отдает предпочтение правой (фосфонатоподобной) форме: [9]
- (RO) 2 POH ⇌ (RO) 2 P (O) H
Связь PH является участком высокой реакционной способности в этих соединениях (например, в реакции Атертона-Тодда ), тогда как в триорганических фосфитах неподеленная пара на фосфоре является участком высокой реакционной способности. Однако диорганофосфиты подвергаются переэтерификации.
См. Также [ править ]
- Фосфинит P (OR) R 2
- Фосфонит P (OR) 2 R
- Ортоэфир CH (OR) 3
- Сложный эфир бората B (OR) 3
Ссылки [ править ]
- ^ Malowan, Джон Е. (1953). «Диэтилфосфит». Неорганические синтезы . Неорганические синтезы. 4 . С. 58–60. DOI : 10.1002 / 9780470132357.ch19 . ISBN 9780470132357.
- Перейти ↑ AH Ford-Moore & BJ Perry (1963). «Триэтилфосфит» . Органический синтез .; Сборник , 4 , с. 955
- ^ Хоффманн, Фридрих В .; Эсс, Ричард Дж .; Узингеф, Роберт П. (ноябрь 1956 г.). «Переэтерификация триалкилфосфитов алифатическими спиртами». Журнал Американского химического общества . 78 (22): 5817–5821. DOI : 10.1021 / ja01603a026 .
- ↑ Райнер Вольф; Банси Лал Каул (2000). «Пластмассы, добавки». Энциклопедия промышленной химии Ульмана . DOI : 10.1002 / 14356007.a20_459 . ISBN 3527306730.
- ^ Дж. Н. Гарднер; ИП Карлон и О. Гной (1968). «Одностадийная процедура получения третичных α-кетолов из соответствующих кетонов». J. Org. Chem. 33 (8): 3294–3297. DOI : 10.1021 / jo01272a055 . PMID 5742870 .
- ^ Айтор Гуаль; Кирилл Годар; Вероника де ла Фуэнте; Серхио Кастильон (2012). «Дизайн и синтез фосфитных лигандов для гомогенного катализа». У Пола CJ Камера; Пит WNM van Leeuwen (ред.). Лиганды фосфора (III) в гомогенном катализе: дизайн и синтез . Джон Вили и сыновья. С. 81–131. DOI : 10.1002 / 9781118299715.ch3 . ISBN 9781118299715.
- ^ Cuny, Грегори Д .; Бухвальд, Стивен Л. (1993). «Практическое, высокопроизводительное, региоселективное, катализируемое родием гидроформилирование функционализированных α-олефинов». Журнал Американского химического общества . 115 (5): 2066–2068. DOI : 10.1021 / ja00058a079 .
- ^ Ван Рой, Аннемик; Камер, Пол CJ; Ван Левен, Пит WNM; Губиц, Кес; Fraanje, Jan; Вельдман, Нора; Спек, Энтони Л. (1996). "Объемные модифицированные дифосфитом родиевые катализаторы: гидроформилирование и характеристика" . Металлоорганические соединения . 15 (2): 835–847. DOI : 10.1021 / OM950549K .
- ^ Doak, GO; Фридман, Леон Д. (1 февраля 1961 г.). «Структура и свойства диалкилфосфонатов». Химические обзоры . 61 (1): 31–44. DOI : 10.1021 / cr60209a002 .

