| Имена | |||
|---|---|---|---|
| Название ИЮПАК фосфоновая кислота | |||
| Другие имена Оксид дигидроксифосфина Дигидрокси (оксо) - λ 5 -фосфан | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.033.682 | ||
| КЕГГ | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| H 3 PO 3 | |||
| Молярная масса | 81,99 г / моль | ||
| Внешность | белое твердое вещество, расплывающееся | ||
| Плотность | 1,651 г / см 3 (21 ° С) | ||
| Температура плавления | 73,6 ° С (164,5 ° F, 346,8 К) | ||
| Точка кипения | 200 ° С (392 ° F, 473 К) (разлагается) | ||
| 310 г / 100 мл | |||
| Растворимость | растворим в этаноле | ||
| Кислотность (p K a ) | 1.1, 6.7 | ||
| −42,5 · 10 −6 см 3 / моль | |||
| Структура | |||
| псевдотетраэдр | |||
| Опасности | |||
| Основные опасности | раздражитель кожи | ||
| Паспорт безопасности | http://www.sigmaaldrich.com/MSDS/ [1] | ||
| R-фразы (устаревшие) | 22-35 | ||
| S-фразы (устаревшие) | 26-36 / 37 / 39-45 | ||
| NFPA 704 (огненный алмаз) |  3 0 1 | ||
| Родственные соединения | |||
Родственные соединения | H 3 PO 4 (т.е. PO (OH) 3 ) H 3 PO 2 (т.е. H 2 PO (OH)) | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
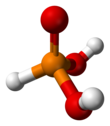
Фосфорная кислота представляет собой соединение, описываемое формулой H 3 PO 3 . Эта кислота является дипротонной (легко ионизирует два протона), а не трипротонной, как можно предположить из этой формулы. Фосфорная кислота является промежуточным продуктом при получении других соединений фосфора. Органические производные фосфористой кислоты, соединения с формулой RPO 3 H 2 , называются фосфоновыми кислотами .
Номенклатура и таутомерия [ править ]
H 3 PO 3 более четко описывается структурной формулой HPO (OH) 2 . В твердом состоянии HP (O) (OH) 2 является тетраэдрическим со связью P – H 1,32 пм, одной более короткой связью P = O 148 пм и двумя более длинными связями P – O (H) 154 пм. Этот вид существует в равновесии с крайне незначительным таутомером P (OH) 3 . ИЮПАК рекомендует называть последнюю фосфористой кислотой, тогда как дигидрокси-форма называется фосфоновой кислотой. [2] Только восстановленные соединения фосфора пишутся с окончанием «ous».
Другие важные оксикислоты из фосфора являются фосфорная кислота (Н 3 РО 4 ) и фосфорноватистая кислоты (Н 3 РО 2 ). Восстановленные фосфорные кислоты подвержены аналогичной таутомерии, включающей сдвиги H между O и P.
Подготовка [ править ]
HPO (OH) 2 является продуктом гидролиза его ангидрида кислоты :
- P 4 O 6 + 6 H 2 O → 4 HPO (OH) 2
(Аналогичное соотношение связывает H 3 PO 4 и P 4 O 10 ).
В промышленном масштабе, кислоту получают путем гидролиза с трихлоридом фосфора с водой или паром: [3]
- PCl 3 + 3 H 2 O → HPO (OH) 2 + 3 HCl
Реакции [ править ]
Кислотно-основные свойства [ править ]
Фосфорная кислота имеет ap K a в диапазоне 1,26–1,3. [4] [5]
- HP (O) (OH) 2 → HP (O) 2 (OH) - + H + p K a = 1,3
Это дипротонная кислота , ион гидрофосфита, HP (O) 2 (OH) - слабая кислота:
- HP (O) 2 (OH) - → HPO2-
3 + H + p K a = 6,7
Основание конъюгата HP (O) 2 (OH) - называется гидрофосфитом, а второе основание конъюгата HPO2-
3, - ион фосфита . [6] (Обратите внимание, что рекомендации IUPAC касаются гидрофосфоната и фосфоната соответственно).
Атом водорода, связанный непосредственно с атомом фосфора, ионизируется с трудом. Экзамены по химии часто проверяют понимание студентами того факта, что не все три атома водорода являются кислыми в водных условиях, в отличие от H 3 PO 4 .
Свойства окислительно-восстановительного потенциала [ править ]
При нагревании до 200 ° C фосфористая кислота диспропорционирует до фосфорной кислоты и фосфина : [7]
- 4 H 3 PO 3 → 3 H 3 PO 4 + PH 3
Эта реакция используется для приготовления PH 3 в лабораторных условиях .
Фосфорная кислота медленно окисляется на воздухе до фосфорной кислоты. [3]
И фосфористая кислота, и ее депротонированные формы являются хорошими восстановителями , хотя и не обязательно быстро реагируют. Они окисляются до фосфорной кислоты или ее солей. Восстанавливает растворы катионов благородных металлов до металлов. При обработке фосфорной кислоты холодным раствором хлорида ртути образуется белый осадок хлорида ртути:
- H 3 PO 3 + 2 HgCl 2 + H 2 O → Hg 2 Cl 2 + H 3 PO 4 + 2 HCl
Хлорид ртути дополнительно восстанавливается фосфористой кислотой до ртути при нагревании или стоянии:
- H 3 PO 3 + Hg 2 Cl 2 + H 2 O → 2 Hg + H 3 PO 4 + 2 HCl
Как лиганд [ править ]
Известно, что при обработке металлами конфигурации d6 фосфористая кислота координируется как редкий в остальном таутомер P (OH) 3 . Примеры включают Mo (CO) 5 (P (OH) 3 ) и [Ru (NH 3 ) 4 (H 2 O) (P (OH) 3 )] 2+ . [8] [9]
Использует [ редактировать ]
Наиболее важным применением фосфористой кислоты (фосфоновой кислоты) является производство основного фосфита свинца , который является стабилизатором ПВХ и связанных с ним хлорированных полимеров. [3]
Он используется в производстве основного стабилизатора ПВХ на основе фосфоната свинца, аминометиленфосфоновой кислоты и гидроксиэтандифосфоновой кислоты. Он также используется в качестве сильного восстановителя и в производстве фосфористой кислоты, синтетических волокон, фосфорорганических пестицидов и высокоэффективного агента для очистки воды ATMP .
Черные металлы, включая сталь, могут быть в некоторой степени защищены путем стимулирования окисления («ржавчины»), а затем преобразования окисления в металлофосфат с использованием фосфорной кислоты и дополнительной защиты с помощью покрытия поверхности. (См .: Пассивация (химия) ).
Органические производные [ править ]
Название ИЮПАК (в основном органическое) - фосфоновая кислота . Эта номенклатура обычно используется для замещенных производных, то есть для органической группы, связанной с фосфором, а не просто для сложного эфира. Так , например, (СН 3 ) РО (ОН) 2 является «метилфосфоновая кислота», которые могут по форме курса «метильную фосфонатные » сложные эфиры .
Ссылки [ править ]
- ^ "Паспорт безопасности данных - 215112" . www.sigmaaldrich.com . Проверено 12 апреля 2018 года .
- ^ Международный союз чистой и прикладной химии (2005). Номенклатура неорганической химии (Рекомендации ИЮПАК 2005 г.). Кембридж (Великобритания): RSC - IUPAC . ISBN 0-85404-438-8 . Электронная версия. .
- ^ a b c Беттерманн, Герхард; Краузе, Вернер; Рис, Герхард; Хофманн, Томас (2000). «Соединения фосфора неорганические». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a19_527 ..
- ^ Ларсон, Джон В .; Пиппин, Маргарет (1989). «Термодинамика ионизации гипофосфористой и фосфористой кислот. Влияние заместителей на оксикислоты второго ряда». Многогранник . 8 (4): 527–530. DOI : 10.1016 / S0277-5387 (00) 80751-2 .
- ^ Справочник CRC по химии и физике (87-е изд.). п. 8–42.
- ^ Новосад, Йозеф (1994). Энциклопедия неорганической химии . Джон Вили и сыновья. ISBN 0-471-93620-0.
- ^ Гохале, SD; Веселый, WL (1967). «Фосфин». Неорганические синтезы . 9 : 56–58. DOI : 10.1002 / 9780470132401.ch17 .
- ^ Sernaglia, RL; Франко, DW (2005). «Рутениевый (II) центр и фосфит-фосфонатное таутомерное равновесие». Неорг. Chem . 28 (18): 3485–3489. DOI : 10.1021 / ic00317a018 .CS1 maint: использует параметр авторов ( ссылка )
- ^ Си, Чанцзюань; Лю, Юйчжоу; Лай, Чунбо; Чжоу, Лишань (2004). «Синтез комплекса молибдена с новым лигандом P (OH) 3 на основе однореакторной реакции Mo (CO) 6 с HP (O) (OEt) 2 и водой». Сообщения неорганической химии . 7 (11): 1202. DOI : 10.1016 / j.inoche.2004.09.012 .
- ^ Си, Чанцзюань; Лю, Юйчжоу; Лай, Чунбо; Чжоу, Лишань (2004). «Синтез комплекса молибдена с новым лигандом P (OH) 3 на основе однореакторной реакции Mo (CO) 6 с HP (O) (OEt) 2 и водой». Сообщения неорганической химии . 7 (11): 1202–1204. DOI : 10.1016 / j.inoche.2004.09.012 .
Дальнейшее чтение [ править ]
- Холлеман, AF; Виберг, Э. (2001). Неорганическая химия . Сан-Диего: Academic Press. ISBN 0-12-352651-5.
- Corbridge., DEC (1995). Фосфор: Очерк его химии, биохимии и технологии (5-е изд.). Амстердам: Эльзевир. ISBN 0-444-89307-5.
- Ли, Джей Ди (3 января 2008 г.). Краткая неорганическая химия . Издательство Оксфордского университета. ISBN 978-81-265-1554-7.