Органическая фотохимия включает в себя органические реакции , вызываемые действием света. [1] [2] Поглощение ультрафиолетового света органическими молекулами часто приводит к реакциям. Раньше использовался солнечный свет, а в наше время используются ультрафиолетовые лампы. Органическая фотохимия оказалась очень полезным синтетическим инструментом. Сложные органические продукты можно получить просто.
История [ править ]
Ранние образцы часто обнаруживались путем наблюдения за осадками или изменениями цвета образцов, подвергавшихся воздействию солнечных лучей. Первый зарегистрированный случай был описан Ciamician, когда солнечный свет преобразовал сантонин в желтый фотопродукт: [3]
Ранний пример осадка был фотодимеризация из антрацена , характеризующаяся Юлий Федорович Фриче и подтверждено СОБ. [4] Подобные наблюдения были сосредоточены на димеризации коричной кислоты до труксилловой кислоты . В настоящее время известно множество фотодимеров, например димер пиримидина , тиофосген , диамантан .
Другой пример был обнаружен Эгбертом Хавингом в 1956 г. [5] . Любопытным результатом была активация при фотолизе мета-нитрогруппой в отличие от обычной активации орто- и пара-группами.
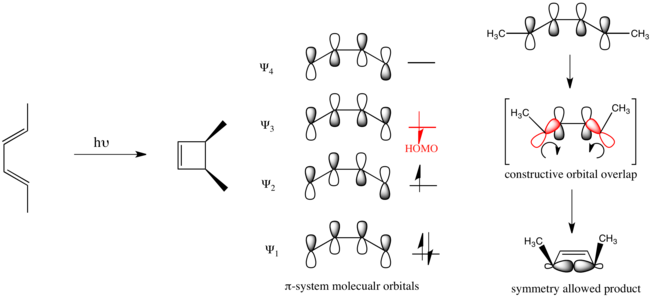
Органическая фотохимия продвинулась вперед с развитием правил Вудворда-Хоффмана . [6] [7] В качестве иллюстрации, эти правила помогают рационализировать электроциклическое замыкание кольца пент-2,4-диена, вызванное фотохимическим воздействием, которое протекает дисротационным образом.
Считается, что органические реакции, подчиняющиеся этим правилам, допускают симметрию. Реакции, протекающие в обратном направлении, запрещены по симметрии и требуют значительно большего количества энергии, если они вообще имеют место.
Ключевые реакции [ править ]
Органические фотохимические реакции объясняются в контексте соответствующих возбужденных состояний . [8] [9]
Параллельно со структурными исследованиями, описанными выше, оценивалась роль спиновой множественности - синглетной или триплетной - на реактивность. Подчеркнута важность триплетно-возбужденных видов. Триплеты, как правило, более долговечны, чем синглеты, и обладают меньшей энергией, чем синглет той же конфигурации. Триплеты могут возникать в результате (A) превращения первоначально образованных синглетов или (B) взаимодействия с триплетом более высокой энергии (сенсибилизация).
Можно гасить триплетные реакции. [10]
Обычные органические фотохимические реакции включают: тип I по Норришу, тип II по Норришу , рацемизацию оптически активных бифенилов, перегруппировку циклогексадиенона типа A, перегруппировку циклогексенона типа B, перегруппировку ди-пи-метана , бицикло [3.1.0 ] перегруппировка гексанона до фенолов, фотохимические электроциклические процессы, перегруппировка эпоксикетонов до бета-дикетонов, раскрытие цикла циклопропилкетонов, гетеролиз 3,5-диметоксилбензильных производных и фотохимическая циклизация диенов.
Практические соображения [ править ]
Реагенты фотореакций могут быть как газообразными, так и жидкими. [11] В общем, необходимо поднести реагенты близко к источнику света, чтобы получить максимально возможную световую отдачу . Для этого реакционную смесь можно облучать либо непосредственно, либо в проточном боковом плече реактора с помощью подходящего источника света. [12]
Недостатком фотохимических процессов является низкая эффективность преобразования электрической энергии в энергию излучения необходимой длины волны . Помимо излучения, источники света выделяют много тепла, что, в свою очередь, требует энергии охлаждения. Кроме того, большинство источников света излучают полихроматический свет, хотя необходим только монохроматический свет . [13] Однако высокий квантовый выход компенсирует эти недостатки.
Работа при низких температурах выгодна, так как избегаются побочные реакции (по мере увеличения селективности) и увеличивается выход (поскольку газообразные реагенты меньше выводятся из растворителя).
Исходные материалы иногда можно охладить перед реакцией до такой степени, что тепло реакции поглощается без дальнейшего охлаждения смеси. В случае газообразных или низкокипящих исходных материалов необходима работа под избыточным давлением. Из-за большого количества возможных исходных материалов было описано большое количество процессов. [14] [15] Крупномасштабные реакции обычно проводят в резервуарном реакторе с мешалкой, реакторе с барботажной колонной или трубчатом реакторе с последующей обработкой в зависимости от целевого продукта. [16]В случае резервуарного реактора с мешалкой лампа (обычно имеющая форму удлиненного цилиндра) снабжена охлаждающей рубашкой и помещена в реакционный раствор. Трубчатые реакторы изготавливаются из кварцевых или стеклянных трубок, которые облучаются снаружи. Преимущество резервуарного реактора с мешалкой заключается в том, что в окружающую среду не теряется свет. Однако интенсивность света быстро падает с расстоянием до источника света из-за адсорбции реагентами. [12]
Влияние излучения на скорость реакции часто может быть представлено степенным законом, основанным на плотности квантового потока, то есть мольном кванте света (ранее измеренном в единицах Эйнштейна ) на площадь и время. Таким образом, одной из целей при проектировании реакторов является определение экономически наиболее выгодных размеров с точки зрения оптимизации квантовой плотности тока. [17]
Тематические исследования [ править ]
[2 + 2] Cycloadditions [ править ]
Олефины димеризуются при УФ-облучении. [18]
Перегруппировка 4,4-дифенилциклогексадиенона [ править ]
Совершенно параллельно с примером сантонина в люмисантонин является перегруппировка 4,4-дифенилциклогексадиенона [9]. Здесь триплетное возбужденное состояние n-pi * претерпевает такое же связывание бета-бета. За этим следует межсистемное пересечение (т.е. ISC) с образованием синглетного основного состояния, которое, как видно, является цвиттер-ионом . Завершающий этап - перегруппировка в бициклический фотопродукт. Реакция называется перегруппировкой циклогексадиенона типа А.
4,4-дифенилциклогексенон [ править ]
Чтобы предоставить дополнительные доказательства механизма диенона, в котором существует связь между двумя двойными связями, здесь представлен случай 4,4-дифенилциклогексенона. Видно, что перестановка совершенно другая; таким образом, для перегруппировки типа А требуются две двойные связи. С одной двойной связью одна из фенильных групп, первоначально в C-4, мигрировала в C-3 (то есть бета-углерод). [19]
Когда одна из арильных групп имеет пара-циано или пара-метоксигруппу, предпочтительнее мигрирует эта замещенная арильная группа. [20] Изучение альтернативных разновидностей фенониевого типа, у которых арильная группа начала мигрировать к бета-углероду, выявляет большую делокализацию электронов с пара-заместителем на мигрирующей арильной группе и, таким образом, более стабильный путь.
π-π * реактивность [ править ]
Еще одним типом фотохимической реакции является перегруппировка дипи-метана . [21] Двумя другими ранними примерами были перегруппировка 1,1,5,5-тетрафенил-3,3-диметил-1,4-пентадиена (молекула «Мариано») [22] и перегруппировка баррелена в полубулвален . [23] Отметим, что, в отличие от реакций циклогексадиенона, в которых используются возбужденные состояния n-π *, перегруппировки ди-π-метана используют возбужденные состояния π-π *.
Связанные темы [ править ]
Фоторедокс-катализ [ править ]
При фоторедокс-катализе фотон поглощается сенсибилизатором (антенной молекулой или ионом), который затем вызывает окислительно-восстановительные реакции на органическом субстрате. Распространенным сенсибилизатором является трис (бипиридин) рутения (II) . Иллюстрацией фотоокислительного катализа являются некоторые реакции аминотрифторметилирования. [24]
Фотохлорирование [ править ]
Фотохлорирование - одно из крупнейших применений фотохимии в органическом синтезе. Однако фотон поглощается не органическим соединением, а хлором . Фотолиз Cl 2 дает атомы хлора, которые отрывают атомы H от углеводородов, что приводит к хлорированию.
Ссылки [ править ]
- ^ П. Клан, Дж. Вирц Фотохимия органических соединений: от концепций к практике . Уайли, Чичестер, 2009 г., ISBN 978-1405190886 .
- ^ NJ Turro, V. Ramamurthy, JC Scaiano Современная молекулярная фотохимия органических молекул . Научные книги университета, Саусалито, 2010, ISBN 978-1891389252 .
- Перейти ↑ Roth, Heinz D. (1989). «Начала органической фотохимии». Angewandte Chemie International Edition на английском языке . 28 (9): 1193–1207. DOI : 10.1002 / anie.198911931 .
- ^ . DOI : 10.1002 / prac.18910440140 . Cite journal requires
|journal=(help); Отсутствует или пусто|title=( справка ) - ^ Имея, E .; Де Йонг, Ро; Дорст, В. (1956). «Фотохимическое ускорение гидролиза нитрофенилфосфатов и нитрофенилсульфатов». Recueil des Travaux Chimiques des Pays-Bas . 75 (4): 378–383. DOI : 10.1002 / recl.19560750403 .
- ^ Вудворд, РБ; Хоффманн, Роальд (1969). «Сохранение орбитальной симметрии». Энгью. Chem. Int. Эд . 8 (11): 781–853. DOI : 10.1002 / anie.196907811 .
- ^ Вудворд, РБ; Хоффманн, Роальд (1971). Сохранение орбитальной симметрии (3-е издание, 1-е изд.). Weinheim, BRD: Verlag Chemie GmbH (BRD) и Academic Press (США). С. 1–178. ISBN 978-1483256153.
- ^ «Фотохимическая перегруппировка 4,4-дифенилциклогексадиенона. Статья I по общей теории фотохимических реакций», Zimmerman, HE; Schuster, DIJ Am. Chem. Soc., 1961, 83, 4486-4487.
- ^ a b Циммерман, Говард Э .; Дэвид И. Шустер (1962). «Новый подход к механической органической фотохимии. IV. Фотохимические перегруппировки 4,4-дифенилциклогексадиенона». Журнал Американского химического общества . ACS 84 (23): 4527–4540. DOI : 10.1021 / ja00882a032 .
- ^ "Теренин, А .; Ермолаев, В. Сенсибилизированная фосфоресценция в органических растворах при низкой температуре; Передача энергии между триплетными состояниями", Пер. Faraday Soc., 1956, 52, 1042–1052.
- ^ Марио Скьявелло (Hrsg.): Фотоэлектрохимия, Фотокатализ и Основы и разработки фотореакторов . Springer, Нидерланды, 2009, ISBN 978-90-481-8414-9 , стр. 564.
- ^ а б Мартин Фишер: Промышленное применение фотохимических синтезов. В: Angewandte Chemie International Edition на английском языке. 17, 1978, с. 16–26, DOI: 10.1002 / anie.197800161 .
- ^ Дитер Вёрле, Майкл В. Тауш, Вольф-Дитер Stohrer: Photochemie: Konzepte, Methoden, Experimente . Wiley & Sons, 1998, ISBN 978-3-527-29545-6 , стр. 271–275.
- ^ Грант США 1379367 , F. Sparre & WE Masland, "Процесс хлорирования", выданный 1921-05-24, передан Du Pont
- ^ Грант США 1459777 , Р. Лейзер и Ф. Циффер, «Процесс и устройство для хлорирования метана», выданный 14 февраля 1920 г., переданный Зифферу Фрицу и Лейзеру Ричарду
- ^ Дэвид А. Миксон, Майкл П. Борер, Патрисия А. О'Хара: Ультраочистка SiCl4 путем фотохлорирования в реакторе с барботажной колонной. В: Журнал Айше. 36, 1990, стр. 216–226, DOI: 10.1002 / aic.690360207 .
- ^ Х. Хартиг: Einfache Dimensionierung, photochemischer Reaktoren. В: Chemie Ingenieur Technik - CIT. 42, 1970, стр. 1241-1245, DOI : 10.1002 / cite.330422002 .
- ^ Cargill1, RL; Далтон, младший; Morton, GH; Caldwell1, WE (1984). «Фотоциклизация энона в алкен: 6-метилбицикло [4.2.0] октан-2-он». Органический синтез . 62 : 118. DOI : 10,15227 / orgsyn.062.0118 .
- ^ "Механистическая и исследовательская органическая фотохимия, IX. Миграция фенила при облучении 4,4-дифенилциклогексенона", Zimmerman, HE; Уилсон, JWJ Am. Chem. Soc., 1964, 86, 4036-4042.
- ^ "Фотохимические миграционные способности циклогексенонов. Механистическая и исследовательская органическая фотохимия. XXIII", Zimmerman, HE; Рике, РД; Scheffer, JRJ Am. Chem. Soc., 1967, 89, 2033-2047.
- ^ "Несимметричное замещение и направление перегруппировки ди-пи-метана; Механическая и исследовательская органическая фотохимия. LVI", Zimmerman, HE; Пратт, ACJ Am. Chem. Soc., 1970, 92, 6259-6267
- ^ "Ди-пи-метановая перегруппировка. Взаимодействие электронно возбужденных виниловых хромофоров. Циммерман, HE; Мариано, PSJ Am. Chem. Soc., 1969, 91, 1718-1727.
- ^ Циммерман, HE; Грюневальд, GL (1966). "Химия баррелена. III. Уникальная фотоизомеризация в семибулвален". Варенье. Chem. Soc. 88 (1): 183–184. DOI : 10.1021 / ja009
- ^ Ясу, Юске; Коике, Такаши; Акита, Мунетака (17 сентября 2012 г.). «Трехкомпонентное окситрифторметилирование алкенов: высокоэффективная и региоселективная дифункционализация связей C = C, опосредованная катализаторами Photoredox». Angewandte Chemie International Edition . 51 (38): 9567–9571. DOI : 10.1002 / anie.201205071 . PMID 22936394 .