| TNFSF11 | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||
| Псевдонимы | TNFSF11 , CD254, ODF, OPGL, OPTB2, RANKL, TRANCE, hRANKL2, sOdf, TNLG6B, фактор некроза опухоли надсемейство элемент 11, TNF суперсемейства элемент 11 | ||||||||||||||||||||||||
| Внешние идентификаторы | OMIM: 602642 MGI: 1100089 HomoloGene: 2744 GeneCards: TNFSF11 | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Ортологи | |||||||||||||||||||||||||
| Разновидность | Человек | Мышь | |||||||||||||||||||||||
| Entrez |
|
| |||||||||||||||||||||||
| Ансамбль |
|
| |||||||||||||||||||||||
| UniProt |
|
| |||||||||||||||||||||||
| RefSeq (мРНК) |
|
| |||||||||||||||||||||||
| RefSeq (белок) |
|
| |||||||||||||||||||||||
| Расположение (UCSC) | Chr 13: 42,56 - 42,61 Мб | Chr 14: 78.28 - 78.31 Мб | |||||||||||||||||||||||
| PubMed поиск | [3] | [4] | |||||||||||||||||||||||
| Викиданные | |||||||||||||||||||||||||
| |||||||||||||||||||||||||
Рецептор активатор ядерного фактора каппа Β лиганд ( RANKL ), также известный как фактор некроза опухоли лиганд надсемейства элемент 11 ( TNFSF11 ), TNF , связанный с индуцированной активацией цитокина ( TRANCE ), остеопротегерин лиганд ( OPGL ), и остеокластами фактор дифференцировки ( ODF ), представляет собой белок , который у человека кодируется TNFSF11 гена . [5] [6]
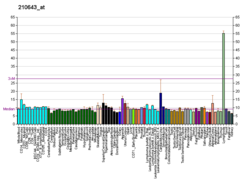
RANKL известен как мембранный белок типа II и является членом суперсемейства факторов некроза опухоли (TNF). [7] Было установлено, что RANKL влияет на иммунную систему и контролирует регенерацию и ремоделирование костей. RANKL представляет собой ген-регулятор апоптоза , партнер по связыванию остеопротегерина (OPG), лиганд рецептора RANK и контролирует пролиферацию клеток, изменяя уровни белков Id4 , Id2 и циклина D1 . [8] [9]RANKL экспрессируется в нескольких тканях и органах, включая скелетные мышцы, тимус, печень, толстую кишку, тонкий кишечник, надпочечники, остеобласты, эпителиальные клетки молочных желез, простату и поджелудочную железу. [9] Различия в уровнях концентрации RANKL в нескольких органах подтверждают важность RANKL для роста тканей (особенно роста костей) и иммунных функций в организме.
Выражение ткани [ править ]
Уровень экспрессии RANKL не коррелирует линейно с действием этого лиганда. Высокая экспрессия белка RANKL обычно обнаруживается в легких , тимусе и лимфатических узлах . Низкая экспрессия белка обнаруживается в костном мозге , желудке , периферической крови , селезенке , плаценте , лейкоцитах , сердце , щитовидной железе и скелетных мышцах . [9]В то время как костный мозг экспрессирует низкие уровни RANKL, RANKL играет решающую роль для адекватного метаболизма кости. Эта связанная с поверхностью молекула (также известная как CD254), обнаруженная на остеобластах , служит для активации остеокластов , которые критически участвуют в резорбции кости . Активность остеокластов запускается через поверхностно-связанный RANKL остеобластов, активирующий поверхностно-связанный активатор рецептора остеокластов ядерного фактора каппа-B (RANK) . Недавние исследования показывают, что в постнатальных костях остеоциты являются основным источником RANKL, регулирующего ремоделирование кости. [10] [11] [12] RANKL, полученный из других типов клеток, способствует потере костной массы в условиях, включающихвоспаление, такое как ревматоидный артрит , и при литических поражениях, вызванных раком , например, при множественной миеломе .
Ген и экспрессия [ править ]
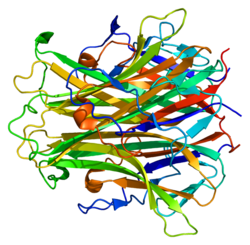
RANKL может экспрессироваться в трех различных молекулярных формах, состоящих из: (1) тримерного трансмембранного белка, (2) первично секретируемой формы и (3) укороченного эктодомена . [13] RANKL идентифицирован как часть семейства TNF; RANKL специально отнесен к TNFSF11, члену суперсемейства лигандов TNF. RANKL состоит из 314 аминокислот и первоначально описывался как имеющий последовательность гена, содержащую 5 экзонов . [14] [15] Среди экзонов, экзон 1 кодировал внутриклеточные и трансмембранные белковые домены, а экзон 2-5 кодировал внеклеточные домены. [14]Внеклеточные домены RANKL подобны другим членам семейства TNF в отношении структурной гомологии и способны отщепляться от поверхности клетки. [14] Хотя функция и значение якорного белка 11 А-киназы ( AKAP11 ) в настоящее время неизвестны, AKAP11 находится непосредственно выше RANKL для всех видов, которые имеют ген RANKL. [15] Выше AKAP11 может указывать на наличие сложного регуляторного процесса, который регулирует уровень экспрессии RANKL.
Функция [ править ]
RANKL является членом семейства цитокинов фактора некроза опухоли (TNF) . Он связывается с RANK на клетках миелоидной линии и функционирует как ключевой фактор дифференцировки и активации остеокластов . RANKL может также связываться с остеопротегерином , белком, секретируемым в основном клетками линии остеобластов, который является мощным ингибитором образования остеокластов, предотвращая связывание RANKL с RANK. RANKL также выполняет функцию в иммунной системе, где он экспрессируется Т-хелперами и, как полагают, участвует в созревании дендритных клеток . Это фактор выживания дендритных клеток и помогает регулировать Т-клетки.-зависимые иммунные ответы. Активация Т-клеток вызывает экспрессию RANKL и может привести к усилению остеокластогенеза и потере костной массы. RANKL может также активировать антиапоптотическую киназу AKT / PKB через сигнальный комплекс, включающий киназу SRC и фактор 6, связанный с рецептором фактора некроза опухоли ( TRAF6 ), что указывает на то, что RANKL может играть роль в регуляции апоптоза . [16] Дальнейшая роль RANKL в иммунитете была обнаружена в синусоидальных макрофагах в лимфатических узлах, которые предупреждают иммунную систему о лимфатических антигенах . [17] В дополнение к прямой передаче сигналов через RANK для дифференцировки макрофагов, RANKL активирует соседниелимфатические эндотелиальные клетки для создания нишевой среды для этих специализированных иммунных клеток. [17]
Модели животных [ править ]
Целенаправленное разрушение родственного гена у мышей привело к тяжелому остеопетрозу и отсутствию остеокластов. У мышей с дефицитом, с инактивацией RANKL или его рецептора RANK, наблюдались дефекты ранней дифференцировки Т- и В-лимфоцитов, и они не могли образовывать лобулоальвеолярные структуры молочной железы во время беременности. [9] [16] Было замечено, что во время беременности передача сигналов RANK-RANKL играет решающую роль в регулировании высвобождения кальция в скелетах; в котором способствовал гормональному ответу, который стимулировал пролиферацию клеток молочной железы. [9] В конечном итоге нарушение лобулоальвеолярных структур молочной железы привело к смерти плода. [9]Те, кто страдает остеопорозом, часто имеют сердечно-сосудистые дефекты, например, сердечную недостаточность. Некоторые исследования предполагают, что, поскольку путь RANK-RANKL регулирует высвобождение кальция и гомеостаз, сигнал RANK-RANKL может обратным образом влиять на сердечно-сосудистую систему; таким образом, объяснение положительной корреляции между остеопорозом и сердечно-сосудистой недостаточностью. [9]
Роль в раке [ править ]
Первичные опухоли обычно метастазируют в кость. Рак груди и простаты обычно имеет больше шансов вызвать вторичный рак в кости. [18] Стивен Педжета «семян и почвы теория ы предполагает, микроокружение в кости создает достаточную„почву“для вторичных опухолей расти в. Некоторые исследования предполагают , что экспрессия RANKL позволяет достаточно микро условия окружающей среды к миграции рака влияния клеток (т.е. хроническое лимфоцитарный лейкоз (ХЛЛ) и множественная миелома ). [19] Среди пациентов с множественной миеломой активность RANKL была значительно увеличена. Фактически, как сообщалось, поверхностная экспрессия RANKL и экспрессия секретируемого RANKL увеличивались на 80% и 50% соответственно.[19] Таким образом, RANKL считается ключевым регулятором сигнала для потери костной массы, вызванной раком.
Согласно гипотезе порочного цикла , после того, как вторичные опухолевые клетки переместились в кость, опухолевые клетки будут секретировать цитокины и факторы роста, которые могут действовать на клетки остеобластного происхождения. Поскольку остеобласты контролируют регуляцию RANKL, стимуляция цитокинами и факторами роста затем будет стимулировать остеобласты к увеличению экспрессии RANKL, часто одновременно с уменьшением образования кости. Дополнительная частота и активность остеокластов, опосредованных RANKL, в свою очередь, увеличивают секрецию факторов роста или факторов, производных от матрикса, что в конечном итоге может увеличивать рост опухоли и активность разрушения кости.
Клиническое значение [ править ]
RANKL, благодаря своей способности стимулировать образование и активность остеокластов, является важным медиатором резорбции кости и общей плотности кости. Избыточное производство RANKL связано с различными дегенеративными заболеваниями костей, такими как ревматоидный артрит и псориатический артрит . Помимо дегенеративных заболеваний костей, метастазы в кости также могут вызывать боль и другие нарушения здоровья, которые могут значительно снизить качество жизни больного раком. Некоторые примеры этих осложнений, являющихся следствием метастазов в кости: гиперкальциемия, патологические переломы и компрессия спинного мозга. [20]Некоторые результаты также предполагают, что некоторые раковые клетки, особенно клетки рака простаты, могут активировать усиление ремоделирования костей и, в конечном итоге, увеличить общее производство костей. [20] Это усиление ремоделирования и образования костей увеличивает общий рост костных метастазов. Общий контроль ремоделирования кости регулируется связыванием RANKL с его рецептором или его рецептором-ловушкой, соответственно, RANK и OPG. [20]
Деносумаб [ править ]
Деносумаб - это полностью человеческое моноклональное антитело к RANKL, одобренное Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов, и во время доклинических испытаний было впервые использовано для лечения пациентов в постменопаузе, страдающих остеопорозом. [20] [21] На третьем этапе клинического исследования деносумаба FDA было показано, что он: (1) снижает метаболизм костной ткани, (2) уменьшает количество переломов в популяции PMO и (3) увеличивает минеральную плотность кости. [20] Антитело против RANKL, деносумаб, также одобрено для использования при онкологических заболеваниях, и при этих показаниях оно обозначено как Xgeva. Как при раке предстательной железы, так и при раке груди деносумаб снижает потерю костной массы, вызванную лечением рака. [20]
Рак простаты [ править ]
В исследование HALT-рака простаты (также известное как NCT00089674) вошли 1468 пациентов с неметастатическим раком простаты, которые в настоящее время получали терапию по депривации андрогенов . [22] Случайно отобранные пациенты получали либо 60 мг деносумаба, либо добавки кальция и витамина D. Это было сделано для измерения эффективности предотвращения потери костной массы, вызванной лечением. [20] У пациентов, получавших 60 мг деносумаба, отмечалось увеличение минеральной плотности костной ткани на 5,6% и снижение частоты переломов костей на 1,5%. [20]
Другое клиническое испытание (NCT00321620) было проведено для определения безопасности и эффективности использования деносумаба по сравнению с золедроновой кислотой . [23] В этом исследовании они использовали 1901 пациента с метастатическим поражением простаты в кости, у которых также были другие осложнения костных заболеваний. Опять же, пациенты были рандомизированы, и некоторым давали 120 мг деносумаба или 4 мг золедроновой кислоты. [20] Пациенты, которым вводили 120 мг деносумаба (по сравнению с теми, кто получал 4 мг золедроновой кислоты), показали большее увеличение гипокальциемии, большую устойчивость к маркерам метаболизма костной ткани uNTx, замедленный ответ как при патологических переломах, так и при позвоночнике компрессионный шнур. [20] Однако показатели выживаемости в обеих клинических группах были сопоставимы.[20]
Рак груди [ править ]
Пациенты с раком молочной железы, положительные по рецепторам гормонов, имеют значительно повышенный риск таких осложнений, как остеопения и остеопороз . Примерно двое из трех больных раком груди имеют положительный рецептор гормонов. [24] В последние несколько лет деносумаб использовался в клинических испытаниях, в первую очередь потому, что большая часть населения страдает костными осложнениями среди тех, кто болен раком груди.
В клиническое исследование HALT-BC (также известное как NCT00089661) было включено 252 пациента. В дополнение к добавкам витамина D и кальция половине пациентов случайным образом давали 60 мг деносумаба, а другой половине - плацебо. [20] [25] У пациентов, получавших деносумаб, отмечалось увеличение минеральной плотности костей поясничного отдела позвоночника , снижение маркеров метаболизма костной ткани без значительного изменения показателей выживаемости. [20]
NCT00321464 был еще одним РКИ III фазы . [26] Подобно NCT00321620 (простата), в этом исследовании измерялась безопасность и эффективность деносумаба по сравнению с золедроновой кислотой . Обе группы показали одинаковую выживаемость и частоту нежелательных явлений. [20]
Множественная миелома [ править ]
Пациенты, у которых диагностирована множественная миелома, имеют примерно 80-100% вероятность развития костных осложнений из-за увеличения активности и / или образования остеокластов и снижения активности остеобластов. [19] [20] На стадии II клинического испытания деносумаб снижал маркеры метаболизма костной ткани, блокируя путь RANKL / RANK. [20] После завершения этого исследования 1176 пациентов с множественной миеломой или прогрессирующим раком были включены в клиническое исследование стадии III (известное как NCT00330759). [27]Основная цель исследования NCT00330759 состояла в том, чтобы сравнить эффекты пациентов, получавших 120 мг деносумаба, по сравнению с пациентами, получавшими 4 мг золедроновой кислоты. В результате этого исследования в течение месяца у пациентов, получавших деносумаб, наблюдалось снижение патологических переломов и компрессии спинного мозга; однако со временем выяснилось, что деносумаб значительно замедлил развитие костных осложнений. [20] При раке груди и простаты пациенты в группах деносумаба или золедроновой кислоты имели сопоставимые побочные эффекты и выживаемость. [20]
Медроксипрогестерона ацетат [ править ]
Женщинам в период менопаузы часто назначают различные виды гормональной терапии в постменопаузе для предотвращения остеопороза и уменьшения симптомов менопаузы. [28] Медроксипрогестерона ацетат (MPA) представляет собой синтетический прогестин и обычно используется в качестве противозачаточного средства или гормональной терапии при эндометриозе или остеопорозе. Недавние исследования показывают, что использование MPA увеличивает риск развития рака груди у пациентов из- за увеличения экспрессии RANKL. [28] MPA вызывает существенную индукцию RANKL в эпителиальных клетках молочных желез, в то время как делеция RANKL снижает частоту возникновения MPA-индуцированного рака груди. Следовательно, ингибирование RANKL имеет потенциал для профилактики и лечения рака груди. [29] [30]
См. Также [ править ]
- Кластер дифференциации
- КЛАССИФИЦИРОВАТЬ
- Остеопротегерин
- Остеоиммунология
Ссылки [ править ]
- ^ a b c GRCh38: Ensembl, выпуск 89: ENSG00000120659 - Ensembl , май 2017 г.
- ^ a b c GRCm38: выпуск Ensembl 89: ENSMUSG00000022015 - Ensembl , май 2017 г.
- ^ "Human PubMed Reference:" . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «Ссылка на Mouse PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ↑ Wong BR, Rho J, Arron J, Robinson E, Orlinick J, Chao M, Kalachikov S, Cayani E, Bartlett FS, Frankel WN, Lee SY, Choi Y (октябрь 1997 г.). «TRANCE представляет собой новый лиганд семейства рецепторов фактора некроза опухолей, который активирует N-концевую киназу c-Jun в Т-клетках» . J. Biol. Chem . 272 (40): 25190–4. DOI : 10.1074 / jbc.272.40.25190 . PMID 9312132 .
- ^ Андерсон DM, Марасковский E, Биллингсли WL, Дугалл WC, Томецко ME, Roux ER, Teepe MC, DuBose RF, Cosman D, Galibert L (ноябрь 1997). «Гомолог рецептора TNF и его лиганд усиливают рост Т-клеток и функцию дендритных клеток». Природа . 390 (6656): 175–9. Bibcode : 1997Natur.390..175A . DOI : 10.1038 / 36593 . PMID 9367155 . S2CID 4373990 .
- ^ Ханада Р, Т Ханада, Сигл В, D Schramek, Пеннингер JM (2011). «RANKL / RANK - выше костей». J. Mol. Med . 89 (7): 647–56. DOI : 10.1007 / s00109-011-0749-z . PMID 21445556 . S2CID 25285776 .
- ^ Mueller CG, Hess E (2012). «Новые функции RANKL в лимфоидных тканях» . Фронт Иммунол . 3 : 261. DOI : 10.3389 / fimmu.2012.00261 . PMC 3432452 . PMID 22969763 .
- ^ Б с д е е г Wada T, Накасима T, N, Hiroshi Пеннингер JM (2006). «Передача сигналов RANKL-RANK в остеокластогенезе и заболеваниях костей». Trends Mol Med . 12 (1): 17–25. DOI : 10.1016 / j.molmed.2005.11.007 . PMID 16356770 .
- ^ Сюн, Цзиньху; Онал, Мелда; Jilka, Роберт Л .; Вайнштейн, Роберт С .; Manolagas, Stavros C .; О'Брайен, Чарльз А. (11 сентября 2011 г.). «Встраиваемые в матрицу клетки контролируют образование остеокластов» . Природная медицина . 17 (10): 1235–1241. DOI : 10.1038 / nm.2448 . ISSN 1546-170X . PMC 3192296 . PMID 21909103 .
- ^ Сюн, Цзиньху; Пьемонтезе, Марилина; Онал, Мелда; Кэмпбелл, Джош; Goellner, Джозеф Дж .; Дусевич, Владимир; Боневальд, Линда; Manolagas, Stavros C .; О'Брайен, Чарльз А. (1 января 2015 г.). «Остеоциты, а не остеобласты или выстилающие клетки, являются основным источником RANKL, необходимого для образования остеокластов при ремоделировании кости» . PLOS ONE . 10 (9): e0138189. Bibcode : 2015PLoSO..1038189X . DOI : 10.1371 / journal.pone.0138189 . ISSN 1932-6203 . PMC 4578942 . PMID 26393791 .
- ^ Накашима, Tomoki; Хаяси, Микихито; Фукунага, Таканобу; Курата, Косаку; О-Хора, Масацугу; Feng, Jian Q .; Боневальд, Линда Ф .; Кодама, Тацухико; Вутц, Антон (11 сентября 2011 г.). «Доказательства регуляции костного гомеостаза остеоцитами посредством экспрессии RANKL». Природная медицина . 17 (10): 1231–1234. DOI : 10.1038 / nm.2452 . ISSN 1546-170X . PMID 21909105 . S2CID 21188945 .
- ^ Финдли DM, Аткинс GJ (2011). «Связь между сывороткой RANKL и RANKL в кости». Osteoporos Int . 22 (10): 2597–602. DOI : 10.1007 / s00198-011-1740-9 . PMID 21850548 . S2CID 908214 .
- ^ a b c Уолш NC, Александр KA, Manning CA, Karmakar S, Karmakar SK, Wang JF, Weyand CM, Pettit AR, Gravallese EM (2013). «Активированные человеческие Т-клетки экспрессируют альтернативные транскрипты мРНК, кодирующие секретируемую форму RANKL» . Genes Immun . 14 (5): 336–45. DOI : 10.1038 / gene.2013.29 . PMC 3740552 . PMID 23698708 .
- ^ а б О'Брайен CA (2010). «Контроль экспрессии гена RANKL» . Кость . 46 (4): 911–9. дои : 10,1016 / j.bone.2009.08.050 . PMC 2842447 . PMID 19716455 .
- ^ a b «Ген Entrez: фактор некроза опухоли TNFSF11 (лиганд) суперсемейство, член 11» .
- ^ а б Камара, Абдурамане; Кордейро, Ольга Г .; Аллуш, Фарук; Спонсель, Янина; Шипр, Мелани; Ондер, Лукас; Асано, Кеничи; Танака, Масато; Ягита, Хидео; Людвиг, Буркхард; Флачер, Винсент (18 июня 2019 г.). «Мезенхимные и эндотелиальные стромальные клетки лимфатического узла взаимодействуют через цитокиновую ось RANK-RANKL для формирования ниши синусоидальных макрофагов» . Иммунитет . 50 (6): 1467–1481.e6. DOI : 10.1016 / j.immuni.2019.05.008 . ISSN 1074-7613 . PMID 31201093 .
- ^ Coleman RE (2001). «Метастатическая болезнь костей: клиника, патофизиология и стратегии лечения». Лечение рака. Ред . 27 (3): 165–76. DOI : 10,1053 / ctrv.2000.0210 . PMID 11417967 .
- ^ a b c Schmiedel BJ, Scheible CA, Nuebling T, Kopp HG, Wirths S, Azuma M, Schneider P, Jung G, Grosse-Hovest L, Salih HR (2013). «Экспрессия RANKL, функция и терапевтическое нацеливание при множественной миеломе и хроническом лимфолейкозе» . Cancer Res . 73 (2): 683–94. DOI : 10.1158 / 0008-5472.CAN-12-2280 . PMID 23139212 .
- ^ a b c d e f g h i j k l m n o p q r Кастеллано Д., Сепульведа Дж. М., Гарсиа-Эскобар I, Родригес-Антолин А., Сундлов А., Кортес-Фунес Х (2011). «Роль ингибирования RANK-лиганда при раке: история деносумаба» . Онколог . 16 (2): 136–45. DOI : 10.1634 / теонколог.2010-0154 . PMC 3228090 . PMID 21285392 .
- Перейти ↑ Miller PD (2009). «Деносумаб: антитело против RANKL». Curr Osteoporos Rep . 7 (1): 18–22. DOI : 10.1007 / s11914-009-0004-5 . PMID 19239825 . S2CID 10465712 .
- ^ "AMG 162 в лечении потери костной массы у субъектов, проходящих терапию андрогенной депривации для неметастатического рака простаты" . NCT00089674 . ClinicalTrials.gov.
- ^ "Исследование деносумаба против золедроновой кислоты для лечения метастазов в кости у мужчин с гормонорезистентным раком простаты" . NCT00321620 . ClinicalTrials.gov.
- ^ «Гормональная терапия рака груди» . Cancer.org . Проверено 31 января 2014 года .
- ^ «AMG 162 в лечении потери костной массы у субъектов, проходящих терапию ингибиторами ароматазы для неметастатического рака молочной железы» . NCT00089661 . ClinicalTrials.gov.
- ^ «Исследование, сравнивающее деносумаб и золедроновую кислоту для лечения костных метастазов у субъектов рака груди» . NCT00321464 . ClinicalTrials.gov.
- ^ «Исследование деносумаба против золедроновой кислоты для лечения метастазов в кости у субъектов с запущенным раком или множественной миеломой» . NCT00330759 . ClinicalTrials.gov.
- ^ a b Wood CE, Бранстеттер Д., Джейкоб А.П., Клайн Дж. М., Регистр TC, Рорбах К., Хуанг Л. Ю., Боргеринк Н., Дугалл В. К. (2013). «Влияние прогестина на пути пролиферации клеток в молочной железе в постменопаузе» . Рак молочной железы Res . 15 (4): R62. DOI : 10.1186 / bcr3456 . PMC 3978455 . PMID 23938070 .
- ^ Schramek D, Leibbrandt A, Sigl V, Kenner L, Pospisilik JA, Lee HJ, Hanada R, Joshi PA, Aliprantis A, Glimcher L, Pasparakis M, Khokha R, Ormandy CJ, Widschwendter M, Schett G, Penninger JM (ноябрь 2010). «Фактор дифференцировки остеокластов RANKL контролирует развитие прогестинового рака молочной железы» . Природа . 468 (7320): 98–102. Bibcode : 2010Natur.468 ... 98S . DOI : 10,1038 / природа09387 . PMC 3084017 . PMID 20881962 .
- ^ Gonzalez-Suarez E, Jacob AP, Jones J Миллер R, Рудье-Meyer MP, Erwert R, Пинкасова J, Branstetter D, Дугал WC (ноябрь 2010). «Лиганд RANK опосредует индуцированную прогестином пролиферацию эпителия молочной железы и канцерогенез». Природа . 468 (7320): 103–7. Bibcode : 2010Natur.468..103G . DOI : 10,1038 / природа09495 . PMID 20881963 . S2CID 4322105 .
Дальнейшее чтение [ править ]
- Уайт М. (2006). «Краткое и краткое изложение костной терапии». N Engl J Med . 354 (8): 860–3. DOI : 10.1056 / NEJMe068003 . PMID 16495400 . связь
- Бакли К.А., Фрейзер В.Д. (2003). «Активатор рецепторов для ядерного фактора, лиганда kappaB и остеопротегерина: регуляторы физиологии костей и иммунных ответов / потенциальные терапевтические агенты и биохимические маркеры». Анна. Clin. Biochem . 39 (Pt 6): 551–6. DOI : 10.1258 / 000456302760413324 . PMID 12564836 .
- Джеффкоат В. (2005). "Сосудистый кальциноз и остеолиз при диабетической невропатии - это RANK-L недостающее звено?" . Диабетология . 47 (9): 1488–92. DOI : 10.1007 / s00125-004-1477-5 . PMID 15322748 .
- Коллин-Осдобы П. (2005). «Регулирование кальцификации сосудов с помощью факторов регуляции остеокластов RANKL и остеопротегерина» . Circ. Res . 95 (11): 1046–57. DOI : 10.1161 / 01.RES.0000149165.99974.12 . PMID 15564564 .
- Уайт MP, Mumm S (2005). «Наследственные нарушения сигнального пути RANKL / OPG / RANK». Журнал скелетно-мышечных и нейронных взаимодействий . 4 (3): 254–67. PMID 15615493 .
- Clohisy DR, Mantyh PW (2005). «Боль при раке костей и роль RANKL / OPG». Журнал скелетно-мышечных и нейронных взаимодействий . 4 (3): 293–300. PMID 15615497 .
- Анандараджа А.П., Шварц Е.М. (2006). «Анти-RANKL-терапия воспалительных заболеваний костей: механизмы и возможности клинического применения». J. Cell. Biochem . 97 (2): 226–32. DOI : 10.1002 / jcb.20674 . PMID 16240334 . S2CID 33543150 .
- Баудхуин М., Дупломб Л., Руис Веласко С., Фортун И., Хейманн Д., Падринес М. (2007). «Ключевые роли системы OPG-RANK-RANKL в онкологии костей». Эксперт Rev Anticancer Ther . 7 (2): 221–32. DOI : 10.1586 / 14737140.7.2.221 . PMID 17288531 . S2CID 12283459 .
- Його К., Исида-Китагава Н., Такея Т. (2007). «Отрицательная ауторегуляция передачи сигналов RANKL и c-Src в остеокластах». J. Bone Miner. Метаб . 25 (4): 205–10. DOI : 10.1007 / s00774-007-0751-2 . PMID 17593489 . S2CID 32120753 .
- Бойс Б.Ф., Син Л. (2007). «Биология RANK, RANKL и остеопротегерина» . Исследования и терапия артрита . 9 Дополнение 1: S1. DOI : 10.1186 / ar2165 . PMC 1924516 . PMID 17634140 .
- МакКлунг М (2007). «Роль ингибирования RANKL при остеопорозе» . Исследования и терапия артрита . 9 Приложение 1: S3. DOI : 10,1186 / ar2167 . PMC 1924518 . PMID 17634142 .
Внешние ссылки [ править ]
- Путь передачи сигналов RANKL
- RANKL + Protein в Национальной медицинской библиотеке США по предметным заголовкам по медицинским предметам (MeSH)
- Обзор всей структурной информации, доступной в PDB для UniProt : O14788 (член суперсемейства лиганд фактора некроза опухоли 11) в PDBe-KB .
Эта статья включает текст из Национальной медицинской библиотеки США , которая находится в свободном доступе .