Восстановительное отщепление - это элементарный этап в металлоорганической химии, на котором степень окисления металлического центра снижается при образовании новой ковалентной связи между двумя лигандами . Это микроскопическое обратный из окислительного присоединения , и часто продукт стадии формирования во многих каталитических процессах. Поскольку окислительное добавление и восстановительное отщепление являются обратными реакциями, для обоих процессов применяются одни и те же механизмы, а равновесие продуктов зависит от термодинамики обоих направлений. [1] [2]
Общая информация [ править ]
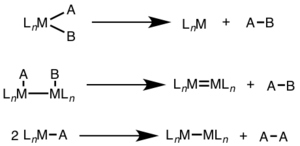
Восстановительное устранение часто наблюдается в более высоких степенях окисления и может включать двухэлектронное изменение в одном металлическом центре (моноядерном) или одноэлектронное изменение в каждом из двух металлических центров (биядерном, двухъядерном или биметаллическом). [1] [2]
При моноядерном восстановительном устранении степень окисления металла уменьшается на два, в то время как количество d-электронов металла увеличивается на два. Этот путь является общим для d 8 металлов Ni (II), Pd (II) и Au (III) и d 6 металлов Pt (IV), Pd (IV), Ir (III) и Rh (III). Кроме того, мононуклеарное восстановительное отщепление требует, чтобы удаляемые группы находились цис-друг относительно друга на металлическом центре. [3]
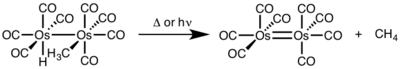
При биядерном восстановительном устранении степень окисления каждого металла уменьшается на единицу, в то время как количество d-электронов каждого металла увеличивается на единицу. Этот тип реакционной способности обычно наблюдается с металлами первого ряда, которые предпочитают изменение степени окисления на одну единицу, но наблюдается как у металлов второго, так и третьего ряда. [4]
Механизмы [ править ]
Как и в случае окислительного добавления, при восстановительном удалении возможно несколько механизмов. Выдающийся механизм - согласованный путь, что означает, что это неполярное трехцентровое переходное состояние с сохранением стереохимии . Кроме того, механизм S N 2 , который протекает с инверсией стереохимии, или радикальный механизм, который протекает с уничтожением стереохимии, являются другими возможными путями для восстановительного устранения. [1]
Октаэдрические комплексы [ править ]
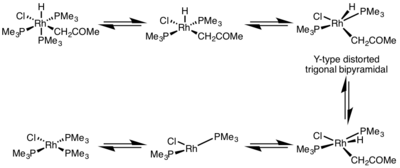
На скорость восстановительного удаления сильно влияет геометрия металлического комплекса. В октаэдрических комплексах восстановительное элиминирование может быть очень медленным из координационно насыщенного центра, и часто восстановительное элиминирование протекает только по диссоциативному механизму, когда лиганд должен сначала диссоциировать, чтобы образовать пятикоординированный комплекс. Этот комплекс принимает искаженную тригонально-бипирамидную структуру Y-типа, в которой π-донорный лиганд находится в базальном положении, а две группы, которые необходимо удалить, сближены. После удаления образуется Т-образный трехкоординатный комплекс, который будет ассоциироваться с лигандом с образованием квадратного плоского четырехкоординатного комплекса. [5]
Квадратные плоские комплексы [ править ]
Восстановительное устранение плоских квадратных комплексов может происходить с помощью различных механизмов: диссоциативных , недиссоциативных и ассоциативных . Подобно октаэдрическим комплексам, диссоциативный механизм для квадратных плоских комплексов инициируется потерей лиганда, генерируя трехкоординатный промежуточный продукт, который подвергается восстановительному отщеплению с образованием однокоординированного металлического комплекса. Для недиссоциативного пути редуктивное устранение происходит из четырехкоординатной системы с образованием двухкоординатного комплекса. Если элиминирующие лиганды являются транс-друг к другу, комплекс должен сначала подвергнуться транс-изомеризации в цис.перед устранением. В ассоциативном механизме лиганд должен первоначально ассоциироваться с четырехкоординированным комплексом металла для образования пятикоординированного комплекса, который подвергается восстановительному отщеплению, синонимичному механизму диссоциации для октаэдрических комплексов. [6] [7]
Факторы, влияющие на редуктивное устранение [ править ]
Восстановительное удаление чувствительно к множеству факторов, включая: 1) идентичность металла и электронную плотность; 2) стерика; 3) участвующие лиганды; 4) координационный номер ; 5) геометрия ; и 6) фотолиз / окисление. Кроме того, поскольку восстановительное удаление и окислительное добавление являются обратными реакциями, любые стерические или электронные устройства, которые увеличивают скорость восстановительного удаления, должны термодинамически препятствовать скорости окислительного добавления. [2]
Идентичность металла и электронная плотность [ править ]
Комплексы металлов первого ряда, как правило, подвергаются восстановительному отщеплению быстрее, чем комплексы металлов второго ряда, которые, как правило, быстрее, чем комплексы металлов третьего ряда. Это связано с прочностью связи, причем связи металл-лиганд в комплексах первого ряда слабее, чем связи металл-лиганд в комплексах третьего ряда. Кроме того, металлические центры с низким содержанием электронов подвергаются восстановительному удалению быстрее, чем металлические центры, богатые электронами, поскольку полученный металл будет приобретать электронную плотность при восстановительном удалении. [8]
Sterics [ править ]
Восстановительное удаление обычно происходит быстрее из металлического центра с более стерическими затруднениями, поскольку стерическое препятствие уменьшается после восстановительного удаления. Кроме того, широкие углы прикуса лиганда обычно ускоряют восстановительное удаление, поскольку стерические свойства заставляют удаляемые группы ближе друг к другу, что обеспечивает большее перекрытие орбит . [9]
Участвующие лиганды [ править ]
Кинетику восстановительного отщепления трудно предсказать, но реакции с участием гидридов протекают особенно быстро из-за эффектов перекрытия орбиталей в переходном состоянии. [10]
Координационный номер [ править ]
Восстановительное отщепление происходит быстрее для комплексов трех- или пятикоординатных металлических центров, чем для четырех- или шестикоординатных металлических центров. Для комплексов с четным координационным числом восстановительное отщепление приводит к промежуточному соединению с сильно разрывающей связь металл-лиганд орбиталью . Когда восстановительное отщепление происходит из комплексов с нечетным координационным числом, полученное промежуточное соединение занимает несвязывающую молекулярную орбиталь . [11]
Геометрия [ править ]
Восстановительное выведение обычно происходит быстрее для комплексов, структура которых напоминает продукт. [2]
Фотолиз / окисление [ править ]
Восстановительное удаление может быть вызвано окислением металлического центра до более высокой степени окисления с помощью света или окислителя. [12]
Приложения [ править ]
Восстановительное элиминирование нашел широкое применение в науке и промышленности, наиболее заметными из которых являются гидрирование , [13] процесс Монсанто уксусной кислоты , [14] гидроформилирование , [15] и кросс-сочетания реакций . [16] Во многих из этих каталитических циклов восстановительное отщепление является стадией образования продукта и регенерирует катализатор; Однако, в реакции Хека [17] и процесса Wacker , [18] восстановительное элиминирование участвует только в регенерации катализатора, а продукты в этих реакциях образуются посредством ликвидации бета-гидрид .
Ссылки [ править ]
- ^ a b c Крэбтри, Роберт Х. (2014). Металлоорганическая химия переходных металлов (6 изд.). Вайли. п. 173. ISBN. 978-1-118-13807-6.
- ^ a b c d Хартвиг, Джон Ф. (2010). Органопереходная химия металлов, от связывания до катализа . Книги университетских наук. п. 321. ISBN. 978-1-891389-53-5.
- ^ Гилли, А .; Стилле, Дж. К. (1980). «Механизмы 1,1-восстановительного удаления из палладия». Варенье. Chem. Soc . 102 (15): 4933–4941. DOI : 10.1021 / ja00535a018 .
- ^ Okrasinski, SJ; Нортом, младший (1977). «Механизм восстановительного удаления. 2. Контроль двухядерного против одноядерного удаления метана из цис-гидридометилтетракарбонилосмия». Варенье. Chem. Soc . 99 : 295–297. DOI : 10.1021 / ja00443a076 .
- Перейти ↑ Milstein, D. (1982). «Первые изолированные стабильные цис-гидридоалкилродиевые комплексы и реакция их восстановительного отщепления». Варенье. Chem. Soc . 104 (19): 5227–5228. DOI : 10.1021 / ja00383a039 .
- ^ Драйвер, MS; Хартвиг, Дж. Ф. (1997). "Восстановительное отщепление ариламинов от фосфиновых комплексов палладия (II), образующих углерод-азотные связи". Варенье. Chem. Soc . 119 (35): 8232–8245. DOI : 10.1021 / ja971057x .
- ^ Ямамото, Т .; Ямамото, А .; Икеда, С. (1971). «Исследование органо (дипиридил) никелевых комплексов. I. Стабильность и активация алкил-никелевых связей диалкил (дипиридил) никеля путем координации с различными замещенными олефинами». Варенье. Chem. Soc . 93 : 3350. DOI : 10.1021 / ja00743a009 .
- ^ Джованнини, Р .; Stüdemann, T .; Dussin, G .; Knochel, P. (1998). «Эффективная перекрестная связь, катализируемая никелем, между центрами углерода sp3». Энгью. Chem. Int. Эд . 37 (17): 2387–2390. DOI : 10.1002 / (SICI) 1521-3773 (19980918) 37:17 <2387 :: AID-ANIE2387> 3.0.CO; 2-M .
- ^ Marcone, JE; Молой, К.Г. (1998). «Кинетическое исследование восстановительного выведения из комплексов (дифосфин) Pd (R) (CN)». Варенье. Chem. Soc . 120 (33): 8527–8528. DOI : 10.1021 / ja980762i .
- ^ Низкий, JJ; Годдард, III, Вашингтон (1984). «Восстановительное связывание водородно-водородных, водородно-углеродных и углерод-углеродных связей из комплексов палладия». Варенье. Chem. Soc . 106 (26): 8321–8322. DOI : 10.1021 / ja00338a067 .
- ^ Крамптон-Брегель, DM; Гольдберг, К.И. (2003). "Механизмы восстановительного удаления CC и CH алкана из октаэдрической Pt (IV): реакция через пятикоординатные промежуточные соединения или прямое удаление?". Варенье. Chem. Soc . 125 : 9442. DOI : 10.1021 / ja029140u . PMID 12889975 .
- ^ Lau, W .; Хаффман, JC; Кочи, JK (1982). "Электрохимическое окисление-восстановление металлоорганических комплексов. Влияние состояния окисления на пути восстановительного отщепления комплексов диалкилжелеза". Металлоорганические соединения . 1 : 155–169. DOI : 10.1021 / om00061a027 .
- Перейти ↑ de Vries, JG (2007). Справочник по гомогенному гидрированию . Вайли. ISBN 978-3-527-31161-3.
- ^ Паулик, ИП; Рот, Дж. Ф. (1968). «Новые катализаторы карбонилирования метанола до уксусной кислоты при низком давлении». Chem. Commun. (24): 1578 DOI : 10.1039 / C1968001578A .
- ^ Ojima, I .; Tsai, C.-H .; Tzamarioudaki, M .; Бонафу, Д. (2004). «Реакция гидроформилирования». Органические реакции . 56 : 1–354. DOI : 10.1002 / 0471264180.or056.01 . ISBN 0471264180.
- ^ Новые тенденции в перекрестной связи: теория и приложения Томас Колакот (редактор) 2014 ISBN 978-1-84973-896-5
- Перейти ↑ de Vries, JG (2001). «Реакция Хека в производстве тонких химикатов» (PDF) . Может. J. Chem . 79 (5–6): 1086–1092. DOI : 10.1139 / v01-033 .
- ^ Донг, JJ; Браун, WR; Феринга, БЛ (2015). "Антимарковниковское окисление концевых алкенов, катализируемое палладием". Энгью. Chem. Int. Эд . 54 (3): 734–744. DOI : 10.1002 / anie.201404856 . PMID 25367376 .