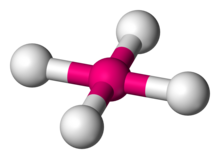
| Квадратная плоская молекулярная геометрия | |
|---|---|
 | |
| Примеры | XeF 4 , PtCl2- 4 |
| Группа точек | Д 4ч |
| Координационный номер | 4 |
| Угол крепления | 90 ° |
| μ (полярность) | 0 |

Квадратная плоская молекулярная геометрия в химии описывает стереохимию (пространственное расположение атомов) , который принимается определенными химическими соединениями . Как следует из названия, молекулы этой геометрии имеют атомы, расположенные по углам.
Примеры [ править ]
Многие соединения принимают эту геометрию, особенно много примеров для комплексов переходных металлов. Соединение благородного газа XeF 4 принимает эту структуру, как предсказывает теория VSEPR . Геометрия преобладает для комплексов переходных металлов с конфигурацией d 8 , которая включает Rh (I), Ir (I), Pd (II), Pt (II) и Au (III). Известные примеры включают противораковые препараты цисплатин [PtCl 2 (NH 3 ) 2 ] и карбоплатин . Многие гомогенные катализаторы являются квадратными плоскими в их состоянии покоя, например, катализатор Уилкинсона и катализатора компании Crabtree в . Другие примеры включаютКомплекс Васьки и соль Цейзе . Определенные лиганды (например, порфирины ) стабилизируют эту геометрию.
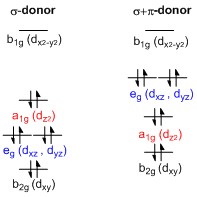
Расщепление энергии d-орбиталей в плоских квадратных комплексах переходных металлов [ править ]
Общая диаграмма d-орбитального расщепления для квадратных плоских (D 4h ) комплексов переходных металлов может быть получена из общей диаграммы октаэдрического (O h ) расщепления , в которой d z 2 и d x 2 - y 2 орбитали вырождены и выше по энергии, чем вырожденный набор орбиталей d xy , d xz и d yz . Когда два аксиальных лиганда удаляются для создания плоской квадратной геометрии, d z 2орбиталь управляется меньшей энергией, поскольку электрон-электронное отталкивание с лигандами на оси z больше не присутствует. Однако для чисто σ-донорных лигандов орбиталь d z 2 все еще выше по энергии, чем орбитали d xy , d xz и d yz, из-за выступа орбитали d z 2 в форме тора . Он несет электронную плотность на осях x и y и поэтому взаимодействует с заполненными орбиталями лиганда. Орбитали d xy , d xz и d yz обычно представляются вырожденными, но они должны расщепляться на два разных энергетических уровня по отношению к неприводимым представлениям.от точечной группы D 4h . Их относительный порядок зависит от природы конкретного комплекса. Кроме того, расщепление d-орбиталей нарушается π-донорными лигандами в отличие от октаэдрических комплексов . В квадратно-плоском случае сильно π-донорные лиганды могут привести к тому, что d xz и d yz орбитали будут выше по энергии, чем d z 2 -орбиталь, тогда как в октаэдрическом случае π-донорные лиганды влияют только на величину d-орбитального расщепления. и относительный порядок орбиталей сохраняется. [1]
См. Также [ править ]
Ссылки [ править ]
- ^ Börgel, Йонас; Кэмпбелл, Майкл Дж .; Риттер, Тобиас (12 января 2016 г.). "Диаграммы d-орбитального расщепления переходных металлов: обновленный образовательный ресурс для квадратных плоских комплексов переходных металлов". Журнал химического образования . 93 (1): 118–121. Bibcode : 2016JChEd..93..118B . DOI : 10.1021 / acs.jchemed.5b00542 . ISSN 0021-9584 .
Внешние ссылки [ править ]
- 3D Chem - химия, структуры и трехмерные молекулы
- IUMSC - Центр молекулярной структуры Университета Индианы
- Интерактивные молекулярные примеры для точечных групп
- [1] - Координационные числа и комплексные ионы