Реакция S N 2 - это тип механизма реакции, который является обычным в органической химии . В этом механизме одна связь разрывается, а одна образуется синхронно, то есть за один этап. S N 2 - это своего рода механизм реакции нуклеофильного замещения , название которого связано с символом механизма Хьюза-Ингольда . Так как два реагирующих частиц участвуют в медленной ( лимитирующей ) стадии, это приводит к термину сек ubstitution н ucleophilic ( би -molecular ) или S N 2; другой основной вид - S N 1 . [1] Многие другие более специализированные механизмы описывают реакции замещения.
Тип реакции настолько распространен, что имеет другие названия, например, «бимолекулярное нуклеофильное замещение» или, среди химиков-неоргаников, « ассоциативное замещение » или «механизм обмена».
Механизм реакции [ править ]
Реакция чаще всего происходит в алифатическом углеродном центре sp 3 с присоединенной к нему электроотрицательной стабильной уходящей группой (часто обозначаемой X), которая часто является атомом галогенида . Разрыв связи C – X и образование новой связи (часто обозначаемой C – Y или C – Nu) происходят одновременно через переходное состояние, в котором углерод, подвергающийся нуклеофильной атаке, является пятикоординированным и приблизительно sp 2 гибридизован. Нуклеофил атакует углерод под углом 180 ° к уходящей группе., так как это обеспечивает лучшее перекрытие неподеленной пары нуклеофила и антисвязывающей орбитали C – X σ *. Уходящая группа затем отталкивается с противоположной стороны, и продукт образуется с инверсией тетраэдрической геометрии у центрального атома.
Если субстрат, подвергаемый нуклеофильной атаке, является хиральным , это часто приводит к инверсии конфигурации ( стереохимии ), называемой инверсией Вальдена .
В примере реакции S N 2 атака Br - (нуклеофила) на этилхлорид (электрофил) приводит к получению бромистого этила с выбросом хлорида в качестве уходящей группы.
С Н 2 приступ происходит , если задняя сторона путь атаки не стерически затрудненные от заместителей на подложке (хлористый этил является субстратом выше). Следовательно, этот механизм обычно происходит на беспрепятственных первичных и вторичных углеродных центрах. Если на субстрате имеется стерическое скопление рядом с уходящей группой, например, в третичном углеродном центре, замещение будет включать в себя механизм S N 1, а не механизм S N 2 ( в этом случае более вероятен S N 1. потому что может образоваться достаточно стабильный карбокатион- посредник).
Факторы, влияющие на скорость реакции [ править ]
На скорость реакции влияют четыре фактора: [2] [3]
Подложка [ править ]
Субстрат играет наиболее важную роль в определении скорости реакции. Это происходит потому, что нуклеофил атакует с обратной стороны субстрата, тем самым разрывая связь уходящей углеродной группы и образуя связь углерод-нуклеофил. Следовательно, чтобы максимизировать скорость реакции S N 2, обратная сторона субстрата должна быть как можно более беспрепятственной. В целом это означает, что метильный и первичный субстраты реагируют быстрее всего, а затем вторичные субстраты. Третичные субстраты не участвуют в реакциях S N 2 из-за стерических затруднений . Структуры, которые могут образовывать высокостабильные катионы за счет простой потери уходящей группы, например, в виде резонансно-стабилизированного карбокатиона, особенно вероятно, будут реагировать через S N1 путь в конкуренции с S N 2.
Нуклеофил [ править ]
Как и субстрат, стерические препятствия влияют на силу нуклеофила. Метилат - анион, например, является одновременно сильным основанием и нуклеофилом , поскольку она представляет собой метильную нуклеофил, и, таким образом , очень беспрепятственно. С другой стороны, трет- бутоксид является сильным основанием, но плохим нуклеофилом из-за его трех метильных групп, препятствующих его приближению к углероду. На прочность нуклеофилов также влияют заряд и электроотрицательность : нуклеофильность увеличивается с увеличением отрицательного заряда и уменьшением электроотрицательности. Например, ОН - лучший нуклеофил, чем вода, а I - лучший нуклеофил, чем Br -(в полярных протонных растворителях). В полярном апротонном растворителе нуклеофильность увеличивается вверх по столбцу периодической таблицы, поскольку нет водородной связи между растворителем и нуклеофилом; в этом случае нуклеофильность отражает основность. I - следовательно, был бы более слабым нуклеофилом, чем Br - потому что это более слабое основание. Вердикт: сильный / анионный нуклеофил всегда предпочитает S N 2 способ нуклеофильного замещения.
Растворитель [ править ]
Растворитель влияет на скорость реакции, поскольку растворители могут окружать или не окружать нуклеофил, тем самым затрудняя или не препятствуя его приближению к атому углерода. [4] Полярные апротонные растворители, такие как тетрагидрофуран , являются лучшими растворителями для этой реакции, чем полярные протонные растворители, потому что полярные протонные растворители будут связывать водород с нуклеофилом, препятствуя тому, чтобы он атаковал углерод с уходящей группой. Полярный апротонный растворитель с низкой диэлектрической постоянной или с затрудненным дипольным концом будет способствовать S N 2 способу реакции нуклеофильного замещения. Примеры: диметилсульфоксид , диметилформамид , ацетон и др.
Выход из группы [ править ]
Стабильность уходящей группы как аниона и прочность ее связи с атомом углерода влияют на скорость реакции. Чем более стабильно сопряженное основание уходящей группы, тем более вероятно, что во время реакции оно возьмет два электрона своей связи с углеродом. Следовательно, чем слабее уходящая группа в виде конъюгированного основания и, следовательно, чем сильнее ее соответствующая кислота, тем лучше уходящая группа. Поэтому примерами хороших уходящих групп являются галогениды (за исключением фторида из-за его сильной связи с атомом углерода) и тозилат , тогда как HO - и H 2 N - нет.
Кинетика реакции [ править ]
Скорость реакции S N 2 является вторым порядком , так как стадия, определяющая скорость, зависит от концентрации нуклеофилов [Nu - ], а также от концентрации субстрата [RX]. [5]
- r = k [RX] [Nu - ]
Это ключевое различие между механизмами S N 1 и S N 2. В реакции S N 1 нуклеофил атакует после завершения лимитирующей стадии, тогда как в S N 2 нуклеофил отталкивает уходящую группу на лимитирующей стадии. Другими словами, скорость реакций S N 1 зависит только от концентрации субстрата, тогда как скорость реакции S N 2 зависит от концентрации как субстрата, так и нуклеофила. [5]
Было показано [6], что за исключением редких (но предсказуемых случаев) первичные и вторичные субстраты проходят исключительно по механизму S N 2, в то время как третичные субстраты проходят по реакции S N 1. Есть два фактора, которые затрудняют определение механизма реакций нуклеофильного замещения у вторичных атомов углерода:
- Многие изученные реакции являются реакциями сольволиза, в которых молекула растворителя (часто спирта) является нуклеофилом. Хотя механически все еще протекает реакция второго порядка, кинетически реакция первого порядка, поскольку концентрация нуклеофила-молекулы растворителя во время реакции эффективно постоянна. Этот тип реакции часто называют реакцией псевдопервого порядка.
- В реакциях, в которых уходящая группа также является хорошим нуклеофилом (например, бромидом), уходящая группа может выполнять реакцию S N 2 на молекуле субстрата. Если субстрат хиральный, это меняет конфигурацию субстрата перед сольволизом, приводя к рацемизированному продукту - продукту, которого можно было бы ожидать от механизма S N 1. В случае уходящей группы бромида в спиртовом растворителе Cowdrey et al. [7] показали, что бромид может иметь константу скорости S N 2 в 100-250 раз выше, чем константа скорости для этанола. Таким образом, после сольволиза энантиоспецифического субстрата всего на несколько процентов он становится рацемическим.
Примеры в учебниках вторичных субстратов, идущих по механизму S N 1, неизменно включают использование бромида (или другого хорошего нуклеофила), поскольку уходящая группа запутала понимание реакций алкил-нуклеофильного замещения у вторичных углеродов на 80 лет [3] . Работа с системой 2-адамантила (S N -не представляется возможными) по Шлейеру и сотрудниками, [8] применение азида (отличный нуклеофил , но очень бедная уходящей группа) по Weiner и Sneen, [9] [10] разработка уходящих сульфонатных групп (ненуклеофильные хорошие уходящие группы) и демонстрация значительных экспериментальных проблем в первоначальной заявке на S N1 механизм сольволиза оптически активного 2-бромоктана Hughes et al. [11] [3] убедительно продемонстрировали, что вторичные субстраты действуют исключительно (за исключением необычных, но предсказуемых случаев) по механизму S N 2.
Конкурс E2 [ править ]
Обычной побочной реакцией , происходящей с реакциями S N 2, является отщепление E2 : поступающий анион может действовать как основание, а не как нуклеофил, отщепляя протон и приводя к образованию алкена . Этот путь предпочтителен для стерически затрудненных нуклеофилов. Реакции элиминирования обычно протекают при повышенных температурах [12] из-за повышенной энтропии . Этот эффект может быть продемонстрирован в газофазной реакции между сульфонатом и простым алкилбромидом , происходящей внутри масс-спектрометра : [13] [14]
В случае бромистого этила продукт реакции является преимущественно продуктом замещения. По мере увеличения стерических препятствий вокруг электрофильного центра, как и в случае с изобутилбромидом , замещение оказывается неблагоприятным, и преобладающей реакцией является элиминирование. Другими факторами, способствующими устранению, являются прочность основы. С менее основным бензоатным субстратом изопропилбромид реагирует с замещением 55%. В общем, газофазные реакции и реакции в фазе раствора этого типа следуют одним и тем же тенденциям, хотя в первом случае устраняются эффекты растворителя .
Кольцевой механизм [ править ]
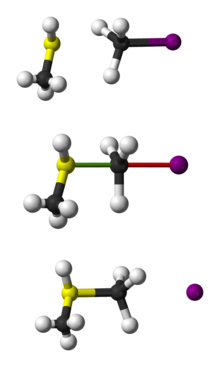
Развитие, привлекшее внимание в 2008 году, касается обходного механизма S N 2, наблюдаемого в газофазной реакции между хлорид-ионами и метилиодидом с помощью специальной техники, называемой визуализацией скрещенных молекулярных пучков . Когда ионы хлорида имеют достаточную скорость, их первоначальное столкновение с молекулой йодистого метила заставляет йодистый метил один раз вращаться до того, как имеет место действительный механизм замещения S N 2. [15] [16] [17]
См. Также [ править ]
- Нажатие стрелки
- Кристофер Келк Ингольд
- Реакция Финкельштейна
- Участие в соседней группе
- Нуклеофильное ацильное замещение
- Нуклеофильное ароматическое замещение
- S N 1 реакция
- S N i
- Реакция замещения
Ссылки [ править ]
- ^ МакМурри, Джон Е. (1992), органическая химия (3 - е изд.), Belmont: Wadsworth, ISBN 0-534-16218-5
- ^ Смит, Майкл Б .; Март, Джерри (2007), Расширенная органическая химия: реакции, механизмы и структура (6-е изд.), Нью-Йорк: Wiley-Interscience, ISBN 978-0-471-72091-1
- ^ Хэмлин, Тревор А .; Сварт, Марсель; Бикельгаупт, Ф. Матиас (2018). «Нуклеофильное замещение (SN2): зависимость от нуклеофила, уходящей группы, центрального атома, заместителей и растворителя» . ХимФисХим . 19 (11): 1315–1330. DOI : 10.1002 / cphc.201701363 . ISSN 1439-7641 . PMC 6001448 . PMID 29542853 .
- ^ Хэмлин, Тревор А .; ван Бик, Бас; Wolters, Lando P .; Бикельгаупт, Ф. Матиас (2018). «Нуклеофильное замещение в растворе: анализ штамма активации слабого и сильного действия растворителя» . Химия - европейский журнал . 24 (22): 5927–5938. DOI : 10.1002 / chem.201706075 . ISSN 1521-3765 . PMC 5947303 . PMID 29457865 .
- ^ a b Клейден, Джонатан; Гривс, Ник; Уоррен, Стюарт (2012). Органическая химия (2-е изд.). Оксфорд: Издательство Оксфордского университета. п. 330. ISBN 978-0-19-927029-3.
- ^ Отсутствие участия S N 1 в сольволизе вторичных алкильных соединений, TJ Murphy, J. Chem. Образов .; 2009; 86 (4) pp 519-24; (Статья) doi: 10.1021 / ed041p678
- ^ Связь стерической ориентации с механизмом замещения с участием атомов галогена и простых или замещенных гидроксильных групп, WA Cowdrey, ED Hughes, CK Ingold, S. Masterman, AD Scott, J. Chem. Soc .; 1937; 1252–1271. 10.1039 / JR9370001252
- ^ 2-Адамантиловая система, стандарт для ограничения сольволиза во вторичном субстрате JL Fry, CJ Lancelot, LKM Lam, J. M Harris, RC Bingham, DJ Raber, RE Hill, P. v. R. Schleyer, J. Am . Chem. Soc.,; 1970; 92, pp. 1240-42 (статья); DOI: 10.1021 / ja00478a031
- ^ Разъяснение механизма сольволиза 2-октилсульфонатов. Стереохимические соображения; H. Weiner, RA Sneen, J. Am. Chem. Soc.,; 1965; 87 стр. 287–91; (Статья) doi: 10.1021 / ja01080a026
- ^ Разъяснение механизма сольволиза 2-октилсульфонатов. Кинетические соображения; H. Weiner, RA Sneen, J. Am. Chem. Soc .; 1965; 87 стр. 292-96; (Статья) doi: 10.1021 / ja01080a027
- ^ Гомогенный гидролиз и алкоголиз β-н-октилгалогенидов, ED Hughes, CK Ingold, S. Masterman, J. Chem. Soc .; 1937; pp 1196–1201; (Статья) doi: 10.1039 / JR9370001196
- ^ «Реакциям ликвидации благоприятствует тепло - мастер органической химии» . www.masterorganicchemistry.com . Проверено 13 апреля 2018 года .
- ^ Исследования газовой фазы конкуренции между реакциями замещения и отщепления Скотт Гронерт Счета химических исследований ; 2003 ; 36 (11), стр. 848–857; (Статья) doi : 10.1021 / ar020042n
- ^ Используемая методика представляет собой ионизацию электрораспылением, и поскольку для обнаружения требуются заряженные продукты реакции, нуклеофил снабжен дополнительной сульфонатной анионной группой, неактивной и хорошо отделенной от другого аниона. Соотношение продуктов замещения и элиминирования можно измерить по интенсивности их относительных молекулярных ионов.
- ^ Визуализация динамики нуклеофильного замещения J. Mikosch, S. Trippel, C. Eichhorn, R. Otto, U. Lourderaj, JX Zhang, WL Hase, M. Weidemüller и R. Wester Science 11 января 2008 г. 319: 183-186 doi : 10.1126 / science.1150238 (в отчетах)
- ^ ПЕРСПЕКТИВЫ ХИМИЯ: Не так просто Джон И. Брауман (11 января 2008 г.) Science 319 (5860), 168. DOI : 10.1126 / science.1152387
- ^ Сюрприз из снимков SN2 Измерения скорости ионов раскрывают дополнительный непредвиденный механизм. Кармен Драл. Новости химии и инженерии 14 января 2008 г. Том 86, номер 2 с. 9 http://pubsapp.acs.org/cen/news/86/i02/8602notw1.html , видео включено