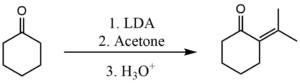Самоконденсация - это органическая реакция, в которой химическое соединение, содержащее карбонильную группу, действует как электрофил, так и нуклеофил при альдольной конденсации . Это также называется симметричной альдольной конденсацией в отличие от смешанной альдольной конденсации, в которой электрофил и нуклеофил являются разными видами.
Например, две молекулы ацетона конденсируются в одно соединение мезитилоксида в присутствии ионообменной смолы : [1]
- 2 CH 3 COCH 3 → (CH 3 ) 2 C = CH (CO) CH 3 + H 2 O
Для синтетических применений это обычно нежелательная, но спонтанная и предпочтительная побочная реакция смешанной альдольной конденсации, и для ее предотвращения необходимы особые меры предосторожности.
Предотвращение самоконденсации [ править ]
Во многих случаях самоконденсация является нежелательной побочной реакцией. Поэтому химики приняли множество способов предотвратить это при проведении перекрестной альдольной реакции.
Использование более реактивного электрофила и неэнолизируемого партнера [ править ]
Если ацетофенон и бензальдегид соединить в присутствии водного NaOH , образуется только один продукт:
Это происходит потому, что в бензальдегиде отсутствуют какие-либо енолизуемые протоны, поэтому он не может образовывать енолят, а бензальдегид гораздо более электрофилен, чем любой неенолизированный ацетофенон в растворе. Следовательно, енолят, образованный из ацетофенона, всегда будет предпочтительно атаковать бензальдегид, а не другую молекулу ацетофенона. [2]
Количественное определение енолят-иона [ править ]
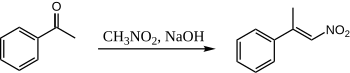
Когда нитрометан и ацетофенон объединяются с использованием водного NaOH, образуется только один продукт:
Здесь ацетофенон никогда не имеет возможности конденсироваться с самим собой, потому что нитрометан настолько кислее, что нитро «енолят» образуется количественно.
Подобный процесс также можно использовать для предотвращения самоконденсации между двумя кетонами. Однако в этом случае используемая база должна быть более мощной. Обычно используется диизопропиламид лития (LDA). Здесь он используется для осуществления перекрестной конденсации между ацетоном и циклогексаноном . [3]
Стадия депротонирования с использованием LDA настолько быстра, что образовавшийся енолят никогда не имеет возможности вступить в реакцию с какими-либо непрореагировавшими молекулами циклогексанона. Затем енолят быстро реагирует с ацетоном.
Образование силилового эфира енола [ править ]
Использование LDA не сработает при попытке получить енолят-ион из альдегидов. Они настолько реактивны, что произойдет самоконденсация. Один из способов обойти это - превратить альдегид в простой силиленоловый эфир с использованием триметилсилилхлорида и основания, такого как триэтиламин , а затем выполнить альдольную конденсацию. Здесь эта тактика используется при конденсации ацетальдегида и бензальдегида . Чтобы способствовать конденсации, необходимо использовать кислоту Льюиса, такую как TiCl 4 . [4]
Ссылки [ править ]
- ^ Конденсации кетонов с использованием ионообменной смолы сульфоновой кислоты Н. Лоретте; J. Org. Chem. ; 1957; 22 (3); 346-347.
- ^ Клейден, Джонатан. Органическая химия. Oxford University Press, Оксфорд, Нью-Йорк, стр. 689-720. ISBN 978-0-19-850346-0
- ^ Клейден, Джонатан. Органическая химия. Oxford University Press, Оксфорд, Нью-Йорк, стр. 689-720. ISBN 978-0-19-850346-0
- ^ Клейден, Джонатан. Органическая химия. Oxford University Press, Оксфорд, Нью-Йорк, стр. 689-720. ISBN 978-0-19-850346-0