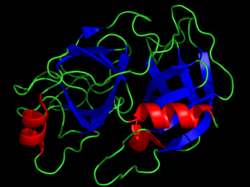
| Сериновые эндопептидазы | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 3.4.21.- | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| BRENDA | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| Структуры PDB | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||
Сериновые протеазы (или сериновые эндопептидазы ) представляют собой ферменты, которые расщепляют пептидные связи в белках , в которых серин служит нуклеофильной аминокислотой в активном центре (фермента) . [1] Они повсеместно встречаются как у эукариот, так и у прокариот . Сериновые протеазы делятся на две широкие категории в зависимости от их структуры: химотрипсиноподобные (трипсиноподобные) и субтилизиноподобные . [2]
Классификация [ править ]
Система классификации протеаз MEROPS насчитывает 16 суперсемейств (по состоянию на 2013 год), каждое из которых содержит множество семейств . Каждое надсемейство использует каталитическую триаду или диаду в другом белке сложить и так представлять сходящуюся эволюцию от каталитического механизма . Большинство из них принадлежит к семейству S1 клана (надсемейства) протеаз PA .
Для суперсемейства P = суперсемейство, содержащее смесь семейств классов нуклеофилов , S = чисто сериновые протеазы. надсемейство. Внутри каждого суперсемейства семейства обозначаются их каталитическими нуклеофилами (S = сериновые протеазы).
Семейства сериновых протеаз
| Надсемейство | Семьи | Примеры |
|---|---|---|
| SB | S8, S53 | Субтилизин ( Bacillus licheniformis ) |
| SC | S9, S10, S15, S28, S33, S37 | Пролилолигопептидаза ( Sus scrofa ) |
| SE | S11, S12, S13 | D-Ala-D-Ala пептидаза C ( Escherichia coli ) |
| SF | S24, S26 | Сигнальная пептидаза I ( Escherichia coli ) |
| SH | S21, S73, S77, S78, S80 | Цитомегаловируса assemblin (человеческий вирус герпеса 5) |
| SJ | S16, S50, S69 | Lon-A пептидаза ( Escherichia coli ) |
| SK | S14, S41, S49 | Протеаза Clp ( кишечная палочка ) |
| ТАК | S74 | Саморасщепляющийся белок эндосиалидазы CIMCD фага K1F ( фаг Enterobacteria K1F ) |
| SP | S59 | Нуклеопорин 145 ( Homo sapiens ) |
| SR | S60 | Лактоферрин ( Homo sapiens ) |
| SS | S66 | Муреинтетрапептидаза LD-карбоксипептидаза ( Pseudomonas aeruginosa ) |
| ST | S54 | Ромбовидный -1 ( Drosophila melanogaster ) |
| PA | S1, S3, S6, S7, S29, S30, S31, S32, S39, S46, S55, S64, S65, S75 | Химотрипсин А ( Bos taurus ) |
| PB | S45, S63 | Предшественник ацилазы пенициллина G ( Escherichia coli ) |
| ПК | S51 | Дипептидаза Е ( кишечная палочка ) |
| PE | P1 | Аминопептидаза DmpA ( Ochrobactrum anthropi ) |
| неназначенный | S48, S62, S68, S71, S72, S79, S81 |
Специфичность субстрата [ править ]
Сериновые протеазы характеризуются отличительной структурой, состоящей из двух бета-бочкообразных доменов, которые сходятся в каталитическом активном центре. Эти ферменты можно далее разделить на трипсиноподобные, химотрипсиноподобные или эластазоподобные, исходя из их субстратной специфичности. [3]
Подобный трипсину [ править ]
Трипсиноподобные протеазы расщепляют пептидные связи после положительно заряженной аминокислоты ( лизина или аргинина ). [4] Эта специфичность обусловлена остатком, который лежит в основе кармана S1 фермента (обычно это отрицательно заряженная аспарагиновая кислота или глутаминовая кислота ).
Химотрипсиноподобный [ править ]
Карман S1 химотрипсиноподобных ферментов более гидрофобен, чем у трипсиноподобных протеаз. Это приводит к специфичности для гидрофобных остатков среднего и большого размера, таких как тирозин , фенилаланин и триптофан .
Тромбиноподобный [ править ]
К ним относятся тромбин , плазминоген, активирующий ткани, и плазмин . Было обнаружено, что они играют роль в коагуляции и пищеварении, а также в патофизиологии нейродегенеративных расстройств, таких как деменция, вызванная болезнью Альцгеймера и Паркинсона.
Подобный эластазу [ править ]
Эластазоподобные протеазы имеют гораздо меньшую щель S1, чем трипсин- или химотрипсиноподобные протеазы. Следовательно, предпочтительны такие остатки, как аланин , глицин и валин .
Подобный субтилизину [ править ]
Субтилизин представляет собой сериновую протеазу прокариот . Субтилизин эволюционно не связан с кланом химотрипсина, но имеет тот же каталитический механизм, использующий каталитическую триаду для создания нуклеофильного серина . Это классический пример, используемый для иллюстрации конвергентной эволюции , поскольку один и тот же механизм эволюционировал дважды независимо в течение эволюции .
Каталитический механизм [ править ]
Основным участником каталитического механизма сериновых протеаз является каталитическая триада. Триада расположена в активном центре фермента, где происходит катализ, и сохраняется во всех суперсемействах ферментов сериновых протеаз. Триада представляет собой скоординированную структуру, состоящую из трех аминокислот : His 57, Ser 195 (отсюда и название «сериновая протеаза») и Asp.102. Каждая из этих трех ключевых аминокислот играет важную роль в способности протеаз к расщеплению. В то время как аминокислотные члены триады расположены далеко друг от друга в последовательности белка, из-за сворачивания они будут очень близко друг к другу в сердце фермента. Особая геометрия членов триады в высшей степени характерна для их конкретной функции: было показано, что положение всего четырех точек триады характеризует функцию содержащего фермента. [5]
В случае катализа возникает упорядоченный механизм, в котором образуются несколько промежуточных продуктов. Катализ расщепления пептида можно рассматривать как катализ пинг-понга , при котором субстрат связывается (в данном случае расщепляется полипептид), высвобождается продукт (N-концевая «половина» пептида), другой субстрат связывается (в данном случае вода), и высвобождается другой продукт (C-концевая «половина» пептида).
Каждая аминокислота в триаде выполняет определенную задачу в этом процессе:
- Серин имеет группу -ОНА , который способен действовать в качестве нуклеофильного агента , нападает на карбонильный углерод из расщеплению пептидной связи субстрата.
- Пара электронов на азоте гистидина обладает способностью принимать водород из группы серин -ОН, таким образом координируя атаку пептидной связи .
- Карбоксильная группа по аспарагиновой кислоты , в свою очередь водородных связей с гистидина , в результате чего атом азота упоминалось выше гораздо более электроотрицательным .
Всю реакцию можно резюмировать следующим образом:
- В полипептид субстрата связывается с поверхностью серин - протеазы фермента таким образом, что к расщеплению связь вставляется в активный сайт фермента, с карбонильной углерода этой связи , расположенной рядом с нуклеофильного серина .
- В серине -ОН атакует карбонил углерод и азот гистидина принимает водород из -ОНА в [серине] и пару электронов из двойной связи карбонильного кислорода двигается к кислороду. В результате образуется тетраэдрический промежуточный продукт.
- Связь, соединяющая азот и углерод в пептидной связи, теперь разорвана. Ковалентные электроны, образующие эту связь, атакуют водород гистидина , разрывая связь. Электроны, которые ранее двигались от карбонильной кислородной двойной связи, возвращаются от отрицательного кислорода, чтобы воссоздать связь, образуя промежуточное соединение ацил-фермент.
- Теперь в реакцию вступает вода. Вода заменяет N-конец отщепленного пептида и атакует карбонильный углерод. И снова электроны от двойной связи перемещаются к кислороду, делая его отрицательным, поскольку образуется связь между кислородом воды и углеродом. Это координируется азотом гистидина , который принимает протон из воды. В целом, это дает еще один тетраэдрический промежуточный продукт.
- В заключительной реакции связь, образованная на первом этапе между серином и карбонильным углеродом, движется, чтобы атаковать водород, который только что приобрел гистидин . Карбонильный углерод с недостатком электронов восстанавливает двойную связь с кислородом. В результате теперь происходит выброс С-конца пептида.
Дополнительные стабилизирующие эффекты [ править ]
Было обнаружено, что дополнительные аминокислоты протеазы, Gly 193 и Ser 195 , участвуют в создании так называемой оксианионной дыры . И Gly 193, и Ser 195 могут отдавать атомы водорода в основной цепи для образования водородных связей. Когда образуются тетраэдрические промежуточные соединения на этапах 1 и 3, отрицательный ион кислорода, приняв электроны от карбонильной двойной связи, идеально вписывается в оксианионную дырку. Фактически, сериновые протеазы предпочтительно связывают переходное состояние.и общая структура предпочтительна, что снижает энергию активации реакции. Это «предпочтительное связывание» во многом определяет каталитическую эффективность фермента.
Регулирование активности сериновой протеазы [ править ]
Организмы-хозяева должны гарантировать, что активность сериновых протеаз адекватно регулируется. Это достигается за счет необходимости начальной активации протеазы и секреции ингибиторов.
Активация зимогена [ править ]
Зимогены - обычно неактивные предшественники фермента. Если бы пищеварительные ферменты были активны при синтезе, они бы немедленно начали жевать синтезирующие органы и ткани. Острый панкреатит - это такое состояние, при котором происходит преждевременная активация пищеварительных ферментов поджелудочной железы, что приводит к самоперевариванию (автолизу). Это также затрудняет патологоанатомическое исследование , так как поджелудочная железа часто переваривает себя до того, как ее можно будет оценить визуально.
Зимогены - это большие неактивные структуры, которые обладают способностью распадаться на части или превращаться в более мелкие активированные ферменты. Разница между зимогенами и активированными ферментами заключается в том, что активный центр катализа зимогенов искажен. В результате полипептид субстрата не может эффективно связываться, и протеолиз не происходит. Только после активации, во время которой изменяются конформация и структура зимогена и открывается активный центр, может происходить протеолиз .
| Зимоген | Фермент | Примечания |
| Трипсиноген | трипсин | Когда трипсиноген попадает в тонкий кишечник из поджелудочной железы, секреция энтеропептидазы из слизистой оболочки двенадцатиперстной кишки расщепляет пептидную связь лизин 15 - изолейцин 16 зимогена. В результате трипсиноген зимогена распадается на трипсин. Напомним, что трипсин также отвечает за расщепление пептидных связей лизина , и, таким образом, как только образуется небольшое количество трипсина, он участвует в расщеплении собственного зимогена, генерируя еще больше трипсина. Таким образом, процесс активации трипсина можно назвать автокаталитическим . |
| Химотрипсиноген | химотрипсин | После того, как связь Arg 15 - Ile 16 в зимогене химотрипсиногена расщепляется трипсином, вновь созданная структура, называемая пи-химотрипсином, подвергается автолизу (самоперевариванию), давая активный химотрипсин. |
| Proelastase | эластаза | Он активируется расщеплением трипсином. |
Как можно видеть, активация трипсиногена для трипсина важна, потому что он активирует свою собственную реакцию, а также реакцию химотрипсина и эластазы . Поэтому важно, чтобы эта активация не произошла преждевременно. Организм принимает несколько защитных мер для предотвращения самопереваривания:
- Активация трипсиногена трипсином относительно медленная.
- Зимогены хранятся в гранулах зимогена, капсулах, стенки которых считаются устойчивыми к протеолизу.
Запрещение [ править ]
Есть определенные ингибиторы, которые напоминают тетраэдрический промежуточный продукт и, таким образом, заполняют активный центр, препятствуя правильной работе фермента. Трипсин, мощный пищеварительный фермент, вырабатывается в поджелудочной железе. Ингибиторы препятствуют самоперевариванию самой поджелудочной железы.
Сериновые протеазы сочетаются с ингибиторами сериновых протеаз , которые отключают свою активность, когда они больше не нужны. [6]
Сериновые протеазы ингибируются разнообразной группой ингибиторов , включая синтетические химические ингибиторы для исследовательских или терапевтических целей, а также природные белковые ингибиторы. Одно семейство природных ингибиторов, называемых «серпинами» (сокращенно от сериновых ингибиторов протеазы ), может образовывать ковалентную связь с сериновой протеазой, подавляя ее функцию. Наиболее изученными серпинами являются антитромбин и альфа-1-антитрипсин , изученные на предмет их роли в коагуляции / тромбозе и эмфиземе / A1AT , соответственно. Искусственные необратимые низкомолекулярные ингибиторы включают AEBSFи PMSF .
Семейство ингибиторов серинпептидазы членистоногих , называемых пацифастином , было обнаружено у саранчи и раков и может функционировать в иммунной системе членистоногих . [7]
Роль в болезни [ править ]
Мутации могут привести к снижению или повышению активности ферментов. Это может иметь разные последствия в зависимости от нормальной функции сериновой протеазы. Например, мутации в протеине C могут приводить к дефициту протеина C и предрасполагать к тромбозу . Кроме того, некоторые протеазы играют жизненно важную роль в активации слияния клетки-хозяина и вируса путем примирования белка Spike вируса, чтобы показать белок, названный «слитый белок» ( TMPRSS2 активирует слияние SARS-CoV-2 ).
Диагностическое использование [ править ]
Определение уровней сериновой протеазы может быть полезно в контексте конкретных заболеваний.
- Уровни фактора свертывания крови могут потребоваться при диагностике геморрагических или тромботических состояний.
- Фекальная эластаза используется для определения внешнесекреторной активности поджелудочной железы, например, при муковисцидозе или хроническом панкреатите .
- Сывороточный простатоспецифический антиген используется при скрининге рака простаты , стратификации риска и мониторинге после лечения.
- Сериновая протеаза, выделяемая тучными клетками , является важным диагностическим маркером реакций гиперчувствительности 1 типа (например, анафилаксии ). Более полезен, чем, например, гистамин, из-за более длительного периода полураспада , то есть он остается в системе в течение клинически полезного периода времени.
См. Также [ править ]
- Сериновая гидролаза
- Протеаза
- цистеин-
- треонин
- аспарагиновая
- металло-
- Клан ПА
- Конвергентная эволюция
- Протеолиз
- Каталитическая триада
- Карта протеолиза
- Протеазы в ангиогенезе
- Интрамембранные протеазы
- Ингибитор протеазы (фармакология)
- Ингибитор протеазы (биология)
- TopFIND - база данных специфичности протеаз, субстратов, продуктов и ингибиторов
- MEROPS - База данных эволюционных групп протеаз
Ссылки [ править ]
- ^ Hedstrom, L. (декабрь 2002). «Механизм и специфичность сериновой протеазы». Chem Ред . 102 (12): 4501–24. DOI : 10.1021 / cr000033x . PMID 12475199 .
- ^ МАДАЛИ ПК, Тиндальте JD, Нолл Т, Фэрели DP - июнь (2010). «Обновление 1: протеазы универсально распознают бета-цепи в своих активных сайтах». Chem Ред . 110 (6): PR1–31. DOI : 10.1021 / cr900368a . PMID 20377171 .
- ^ Ovaere P, S Липпенса, Vandenabeele P, Declercq W (август 2009). «Новые роли каскадов сериновых протеаз в эпидермисе». Trends Biochem Sci . 34 (9): 453–63. DOI : 10.1016 / j.tibs.2009.08.001 . PMID 19726197 .
- ^ Evnin, Люк Б .; Васкес, Джон Р.; Крейк, Чарльз С. (1990). «Субстратная специфичность трипсина исследована с помощью генетической селекции» . Труды Национальной академии наук Соединенных Штатов Америки . 87 (17): 6659–63. DOI : 10.1073 / pnas.87.17.6659 . JSTOR 2355359 . PMC 54596 . PMID 2204062 .
- ^ Иван, Габор .; Сабадка, Золтан; Ордог, Рафаэль; Гролмуш, Винс; Нарай-Сабо, Габор (2009). «Четыре пространственных точки, которые определяют семейства ферментов». Сообщения о биохимических и биофизических исследованиях . 383 (4): 417–420. CiteSeerX 10.1.1.150.1086 . DOI : 10.1016 / j.bbrc.2009.04.022 . PMID 19364497 .
- ^ Страницы биологии Кимбалла, сериновые протеазы [ самостоятельно опубликованный источник? ]
- ^ Breugelmans В, Г Симонет, ван Hoef В, ван Зёст S, Вэнден BJ (2009). «Пацифастин-родственные пептиды: структурные и функциональные характеристики семейства ингибиторов сериновой пептидазы». Пептиды . 30 (3): 622–32. DOI : 10.1016 / j.peptides.2008.07.026 . PMID 18775459 .
Внешние ссылки [ править ]
- Merops онлайновой базы данных для пептидазы и их ингибиторов: серин - пептидаза
- Сайт сериновых протеаз в Университете Сент-Луиса (SLU)
- Серин + протеазы в медицинских предметных рубриках Национальной медицинской библиотеки США (MeSH)