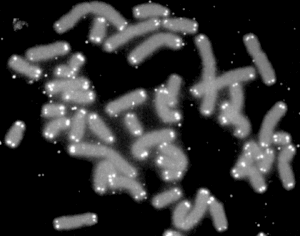
Теломеры ( / т ɛ л ə м ɪ ə г / или / т я л ə м ɪ ə г / , от древнегреческого : τέλος , латинизируется : Telos , лит «конец» и древнегреческий : μέρος , латинизируется : méros , букв. 'часть') представляет собой область повторяющегося нуклеотидапоследовательности, связанные со специализированными белками на концах линейных хромосом . Хотя существуют разные архитектуры, теломеры в широком смысле слова являются широко распространенной генетической особенностью, наиболее часто обнаруживаемой у эукариот. У большинства, если не у всех видов, обладающих ими, они защищают концевые области хромосомной ДНК от прогрессирующей деградации и обеспечивают целостность линейных хромосом, не позволяя системам репарации ДНК ошибочно принимать самые концы цепи ДНК за двухцепочечный разрыв .
Открытие [ править ]
В начале 1970-х годов русский теоретик Алексей Оловников впервые осознал, что хромосомы не могут полностью воспроизводить свои концы. Основываясь на этом, и чтобы приспособиться к идее Леонарда Хейфлика об ограниченном делении соматических клеток , Оловников предположил, что последовательности ДНК теряются каждый раз, когда клетка реплицируется, пока потеря не достигает критического уровня, на котором деление клетки заканчивается. [1]
В 1975–1977 годах Элизабет Блэкберн , работая докторантом в Йельском университете вместе с Джозефом Галлом , открыла необычную природу теломер с их простыми повторяющимися последовательностями ДНК, составляющими концы хромосом. [2] Блэкберн, Кэрол Грейдер и Джек Шостак были удостоены Нобелевской премии по физиологии и медицине 2009 года за открытие того, как хромосомы защищены теломерами и ферментом теломеразой . [3]
В 1983 году Барбара МакКлинток , американский цитогенетик и первая женщина, получившая неразделенную Нобелевскую премию по физиологии и медицине, получила Нобелевскую премию за наблюдение за тем, что хромосомы, лишенные концевых частей, стали «липкими», и выдвинула гипотезу о существовании особой структуры в этих местах. кончик хромосомы, который будет поддерживать стабильность хромосомы. [4]
Структура и функции [ править ]
Проблема с окончанием репликации [ править ]
Во время репликации ДНК ДНК-полимеразане может реплицировать последовательности, присутствующие на 3'-концах. Это является следствием его однонаправленного режима синтеза ДНК: он может присоединять новые нуклеотиды только к существующему 3'-концу (то есть синтез идет на 5'-3 '), и, следовательно, ему требуется праймер для инициации репликации. На ведущей цепи (ориентированной на 5'-3 'внутри репликационной вилки) ДНК-полимераза непрерывно реплицируется от точки инициации до конца цепи, при этом праймер (сделанный из РНК) затем вырезается и замещается ДНК. Однако отстающая цепь ориентирована на 3'-5 'относительно репликационной вилки, поэтому непрерывная репликация ДНК-полимеразой невозможна, что требует прерывистой репликации, включающей повторный синтез праймеров еще на 5'.сайта инициации (см. репликация отстающей цепи). Последний праймер, который участвует в репликации отстающей цепи, находится рядом с 3'-концом матрицы (что соответствует потенциальному 5'-концу отстающей цепи). Первоначально считалось, что последний праймер будет находиться на самом конце матрицы, поэтому после удаления ДНК-полимераза, заменяющая праймеры ДНК (ДНК-Pol δ у эукариот) [примечание 1] , не сможет синтезировать «замещающая ДНК» с 5'-конца отстающей цепи, так что матричные нуклеотиды, ранее спаренные с последним праймером, не реплицировались. [5]С тех пор был поставлен вопрос о том, находится ли последний праймер отстающей цепи точно на 3'-конце матрицы, и было продемонстрировано, что он скорее синтезируется на расстоянии примерно 70-100 нуклеотидов, что согласуется с выводом о том, что ДНК в культура клеток человека укорачивается на 50-100 пар оснований за деление клетки . [6]
Если бы кодирующие последовательности были разрушены в этом процессе, потенциально жизненно важный генетический код был бы утерян. Теломеры - это некодирующие повторяющиеся последовательности, расположенные на концах линейных хромосом, чтобы действовать как буферы для тех кодирующих последовательностей, которые находятся дальше. Они «закрывают» концевые последовательности и вместо этого постепенно разрушаются в процессе репликации ДНК.
«Проблема конечной репликации» характерна исключительно для линейных хромосом, поскольку у кольцевых хромосом нет концов, лежащих вне досягаемости ДНК-полимераз. Соответственно, большинство прокариот , опирающихся на кольцевые хромосомы, не обладают теломерами. [7] Небольшая часть бактериальных хромосом (например, у Streptomyces , Agrobacterium и Borrelia ), однако, линейна и обладает теломерами, которые сильно отличаются от хромосом эукариот по структуре и функциям. Известные структуры бактериальных теломер представляют собой белки.связаны с концами линейных хромосом или шпильками из одноцепочечной ДНК на концах линейных хромосом. [8]
Концы теломер и укрытие [ править ]
На самом 3'-конце теломера имеется выступ из 300 пар оснований, который может вторгаться в двухцепочечную часть теломера, образуя структуру, известную как Т-петля. Эта петля аналогична узлу, который стабилизирует теломеры, предотвращая распознавание концов теломер как контрольных точек механизмом репарации ДНК. Если негомологичное соединение концов происходит на концах теломеров, это может привести к слиянию хромосом. Т-петля поддерживается несколькими белками, вместе называемыми комплексом шелтерина. У человека комплекс шелтерина состоит из шести белков, идентифицированных как TRF1 , TRF2 , TIN2 , POT1 , TPP1 и RAP1. [9]У многих видов, повторяется последовательность обогащены гуанин, например TTAGGG в позвоночных животных , [10] , который позволяет формировать G-квадруплексов , специальной конформации ДНК с участием не-уотсон-Крика. Существуют различные подтипы, в зависимости, среди прочего, от участия одноцепочечной или двухцепочечной ДНК. Имеются доказательства того, что 3'-выступ у инфузорий (которые обладают теломерными повторами, сходными с таковыми у позвоночных) формирует такие G-квадруплексы, которые вмещают его, а не Т-петлю. G-квадруплексы представляют собой препятствие для таких ферментов, как ДНК-полимеразы, и поэтому считается, что они участвуют в регуляции репликации и транскрипции. [11]
Теломераза [ править ]
У многих организмов есть фермент под названием теломераза, который выполняет задачу добавления повторяющихся нуклеотидных последовательностей к концам ДНК. Теломераза «пополняет» теломерную «шапку». У большинства многоклеточных эукариотических организмов теломераза активна только в половых клетках , некоторых типах стволовых клеток, таких как эмбриональные стволовые клетки , и некоторых белых кровяных тельцах . Теломераза может быть реактивирована и теломеры возвращены в эмбриональное состояние посредством переноса ядра соматической клетки. [12] Неуклонное сокращение теломер с каждой репликацией в соматических (телесных) клетках может играть роль в старении [13] и в профилактике рака . [14][15] Это связано с тем, что теломеры действуют как своего рода «слиток» с временной задержкой, который в конечном итоге заканчивается после определенного числа клеточных делений и приводит к возможной потере жизненно важной генетической информации из хромосомы клетки с будущими делениями. [16]
Длина [ править ]
Длина теломер сильно варьируется между видами, от примерно 300 пар оснований у дрожжей [17] до многих тысяч оснований у человека, и обычно состоит из массивов богатых гуанином повторов длиной от шести до восьми пар оснований. Теломеры эукариот обычно оканчиваются выступом 3'-одноцепочечной ДНК , что важно для поддержания теломер и кэппинга. Идентифицированы множественные белки, связывающие одно- и двухцепочечную теломерную ДНК. [18] Они функционируют как для поддержания теломер, так и для покрытия. Теломеры образуют большие петлевые структуры, называемые теломерными петлями или Т-образными петлями. Здесь одноцепочечная ДНК скручивается по длинному кругу, стабилизированная белками, связывающими теломеры . [19]В самом конце Т-петли одноцепочечная теломерная ДНК удерживается на участке двухцепочечной ДНК цепью теломер, разрушающей двухспиральную ДНК, и спариванием оснований с одной из двух цепей. Эта трехцепочечная структура называется петлей смещения или D-петлей. [20]
Роль в клеточном цикле [ править ]
Укорочение теломер у человека может вызывать репликативное старение, которое блокирует деление клеток. Этот механизм, по-видимому, предотвращает геномную нестабильность и развитие рака в старых клетках человека за счет ограничения числа клеточных делений. Однако укороченные теломеры нарушают иммунную функцию, что также может повышать восприимчивость к раку. [21] Если теломеры становятся слишком короткими, у них появляется возможность разворачиваться из своей предполагаемой замкнутой структуры. Клетка может обнаружить это вскрытие как повреждение ДНК, а затем либо прекратить рост, либо вступить в клеточную старость ( старение ), либо начать запрограммированное самоуничтожение клетки ( апоптоз ) в зависимости от генетического фона клетки ( p53положение дел). Незакрытые теломеры также приводят к слиянию хромосом. Поскольку это повреждение не может быть восстановлено в нормальных соматических клетках, клетка может даже перейти в состояние апоптоза. Многие болезни, связанные со старением, связаны с укорочением теломер. Органы разрушаются, поскольку все больше и больше их клеток отмирают или вступают в клеточное старение.
Сокращение [ править ]
Окислительное повреждение [ править ]
Помимо проблемы конечной репликации, исследования in vitro показали, что теломеры накапливают повреждения из-за окислительного стресса и что повреждение ДНК, опосредованное окислительным стрессом, оказывает большое влияние на укорочение теломер in vivo . Существует множество способов, которыми окислительный стресс, опосредованный реактивными формами кислорода (АФК), может приводить к повреждению ДНК, однако пока неясно, вызвана ли повышенная скорость в теломерах присущей им восприимчивостью или пониженной активностью теломер. Системы репарации ДНК в этих областях. [22]Несмотря на широкое согласие в выводах, были отмечены широко распространенные недостатки в измерениях и взятии проб; например, считается, что предполагаемая видовая и тканевая зависимость окислительного повреждения теломер недостаточно учтена. [23] Популяционные исследования показали взаимосвязь между потреблением антиоксидантов и длиной теломер. В рамках проекта исследования рака груди на Лонг-Айленде (LIBCSP) авторы обнаружили умеренное увеличение риска рака груди у женщин с самыми короткими теломерами и низким потреблением бета-каротина, витамина С или Е с пищей [24]. Эти результаты [25] предполагают, что риск рака из-за укорочения теломер может взаимодействовать с другими механизмами повреждения ДНК, в частности с окислительным стрессом.
Связь со старением [ править ]
Укорочение теломер связано со старением, смертностью и заболеваниями, связанными со старением. Нормальное старение связано с укорочением теломер как у людей, так и у мышей, а исследования на генетически модифицированных моделях животных предполагают причинную связь между эрозией теломер и старением. [26] Однако неизвестно, являются ли короткие теломеры просто признаком старения или они сами способствуют прогрессированию процесса старения. [27]
Возраст отца играет роль в длине теломер ребенка, что имеет эволюционные последствия. Хотя теломеры лейкоцитов с возрастом укорачиваются, теломеры сперматозоидов с возрастом удлиняются. Предполагается, что более короткие теломеры вызывают более низкие энергетические затраты (из-за меньшей репликации), но также имеют связанные с иммунной системой и другие затраты, связанные со старением и болезнями, поэтому влияние возраста отца на длину теломер может быть адаптацией, увеличивающей шансы того, что ребенок будет соответствовать среде, в которой он родился. [28] [29]
Возможное влияние психологического стресса [ править ]
Мета-анализ показал, что повышенный воспринимаемый психологический стресс был связан с небольшим уменьшением длины теломер, но эти ассоциации ослабляются до незначительной связи при учете предвзятости публикации . В литературе, посвященной теломерам как интегративным биомаркерам подверженности стрессу и невзгодам, преобладают перекрестные и корреляционные исследования, что затрудняет причинную интерпретацию. [25] [30] В обзоре 2020 года утверждается, что взаимосвязь между психосоциальным стрессом и длиной теломер наиболее сильна для стресса, переживаемого в утробе матери или в раннем возрасте. [31]
Удлинение [ править ]
Феномен ограниченного клеточного деления был впервые обнаружен Леонардом Хейфликом и теперь называется пределом Хейфлика . [32] [33] Значительные открытия были впоследствии сделаны группой ученых, организованной в Geron Corporation основателем Geron Майклом Д. Вестом , которые связали сокращение теломер с пределом Хейфлика. [34] Клонирование каталитического компонента теломеразы позволило провести эксперименты, чтобы проверить, способна ли экспрессия теломеразы на уровнях, достаточных для предотвращения укорочения теломер, иммортализовать клетки человека. Теломераза была продемонстрирована в публикации 1998 года в журнале Science.чтобы быть способным увеличивать продолжительность жизни клеток, и теперь широко признано, что он способен увековечивать соматические клетки человека. [35]
Становится очевидным, что обращение вспять укорочения теломер посредством временной активации теломеразы может быть мощным средством замедления старения. Причина, по которой это продлит жизнь человека, состоит в том, что это расширит предел Хейфлика. Было предложено три пути обращения вспять укорачивания теломер: лекарства, генная терапия или подавление метаболизма, так называемое оцепенение / гибернация . До сих пор эти идеи не были доказаны на людях, но было продемонстрировано, что укорочение теломер обращается в спячку, а старение замедляется (Turbill, et al. 2012 и 2013), и что гибернация продлевает продолжительность жизни (Lyman et al. 1981). ). Также было продемонстрировано, что удлинение теломер успешно обратило вспять некоторые признаки старения у лабораторных мышей.[36] [37] и нематодный червь вида Caenorhabditis elegans . [38] Была выдвинута гипотеза, что более длинные теломеры и особенно активация теломеразы могут вызывать увеличение рака (например, Weinstein and Ciszek, 2002 [39] ). Однако более длинные теломеры также могут защищать от рака, потому что короткие теломеры связаны с раком. Также было высказано предположение, что более длинные теломеры могут вызывать повышенное потребление энергии. [21]
Методы удлинения теломер могут быть полезны для тканевой инженерии , потому что они могут позволить культивировать здоровые, доброкачественные клетки млекопитающих в количествах, достаточно больших, чтобы быть инженерными материалами для биомедицинского ремонта.
Два исследования морских птиц -долгожителей демонстрируют, что роль теломер еще далека от понимания. В 2003 году ученые наблюдали, что теломеры буревестника Лича ( Oceanodroma leucorhoa ), похоже, удлиняются с хронологическим возрастом, что стало первым наблюдаемым примером такого поведения теломер. [40] В 2006 году Juola et al. [41] сообщили, что у другого неродственного долгоживущего вида морских птиц большой фрегат ( Fregata minor), длина теломер действительно уменьшалась, по крайней мере, до c. 40 лет (то есть, вероятно, в течение всей продолжительности жизни), но скорость уменьшения значительно замедлялась с увеличением возраста, и скорость уменьшения длины теломер сильно различалась между отдельными птицами. Они пришли к выводу, что у этого вида (и, вероятно, у фрегатов и их родственников в целом) длина теломер не может использоваться для достаточно точного определения возраста птицы. Таким образом, кажется, что существует гораздо больше вариаций в поведении длины теломер, чем первоначально предполагалось.
Кроме того, Gomes et al. при исследовании сравнительной биологии теломер млекопитающих обнаружили, что длина теломер у разных видов млекопитающих коррелирует скорее обратно, чем напрямую, с продолжительностью жизни, и пришли к выводу, что вклад длины теломер в продолжительность жизни остается спорным. [42] Харрис и др. нашли мало доказательств того, что у людей длина теломер является важным биомаркером нормального старения в отношении важных когнитивных и физических способностей. [43] Гилли и Блэкберн проверили, вызвано ли клеточное старение в парамеции укорочением теломер, и обнаружили, что теломеры не укорачиваются во время старения. [44]
Последовательности [ править ]
Известные современные нуклеотидные последовательности теломер перечислены на веб-сайте базы данных теломераз .
| Группа | Организм | Теломерный повтор (от 5 футов до 3 футов к концу) |
|---|---|---|
| Позвоночные | Человек , мышь , Xenopus | TTAGGG |
| Нитчатые грибы | Neurospora crassa | TTAGGG |
| Формы для слизи | Physarum , Didymium | TTAGGG |
| Диктиостелиум | AG (1-8) | |
| Кинетопластидные простейшие | Трипаносома , Критидия | TTAGGG |
| Инфузорные простейшие | Тетрахимена , Глаукома | ТТГГГГ |
| Парамеций | ТТГГГ (Т / Г) | |
| Oxytricha , Stylonychia , Euplotes | TTTTGGGG | |
| Apicomplexan простейшие | Плазмодий | TTAGGG (Т / К) |
| Высшие растения | Arabidopsis thaliana | TTTAGGG |
| Cestrum elegans | TTTTTTAGGG [45] | |
| Allium | CTCGGTTATGGG [46] | |
| Зеленые водоросли | Хламидомонада | TTTTAGGG |
| Насекомые | Bombyx mori | TTAGG |
| Круглые черви | Аскарида люмбрикоидная | TTAGGC |
| Делящиеся дрожжи | Schizosaccharomyces pombe | TTAC (A) (C) G (1-8) |
| Бутоновые дрожжи | Saccharomyces cerevisiae | TGTGGGTGTGGTG (из матрицы РНК) или G (2-3) (TG) (1-6) T (консенсус) |
| Saccharomyces castellii | TCTGGGTG | |
| Candida glabrata | GGGGTCTGGGTGCTG | |
| грибковые микроорганизмы албиканс | GGTGTACGGATGTCTAACTTCTT | |
| Candida tropicalis | GGTGTA [C / A] GGATGTCACGATCATT | |
| Candida maltosa | GGTGTACGGATGCAGACTCGCTT | |
| Candida guillermondii | GGTGTAC | |
| Candida pseudotropicalis | GGTGTACGGATTTGATTAGTTATGT | |
| Kluyveromyces lactis | GGTGTACGGATTTGATTAGGTATGT |
Исследование риска заболеваний [ править ]
Этот раздел требует дополнительных медицинских справок для проверки или слишком сильно полагается на первоисточники . ( март 2018 ) |
Теломеры имеют решающее значение для поддержания целостности генома и могут быть факторами возрастных заболеваний. [47] Лабораторные исследования показывают, что дисфункция или укорочение теломер обычно возникает из-за клеточного старения и развития опухоли. [47] [48] Короткие теломеры могут привести к нестабильности генома, потере хромосом и образованию невзаимных транслокаций; а теломеры в опухолевых клетках и их предшественниках значительно короче, чем окружающие нормальные ткани. [49] [50]
Наблюдательные исследования обнаружили укороченные теломеры при многих типах экспериментального рака. [51] Кроме того, было обнаружено, что у людей с раком теломеры лейкоцитов короче, чем у здоровых людей. [52] Недавние мета-анализы показывают, что риск рака в 1,4–3,0 раза выше у людей с самыми короткими по сравнению с самыми длинными теломерами. [53] [54] Однако увеличение риска зависит от возраста, пола, типа опухоли и различий в факторах образа жизни. [51]
Измерение [ править ]
В настоящее время используется несколько методов для оценки средней длины теломер в эукариотических клетках. Одним из методов является саузерн-блоттинг фрагмента концевой рестрикции (TRF). [55] [56] ПЦР- анализ в реальном времени для определения длины теломер включает определение соотношения теломер и единичной копии гена (T / S), которое, как было показано, пропорционально средней длине теломер в клетке. [57]
Также были разработаны инструменты для оценки длины теломер из экспериментов по секвенированию полного генома (WGS). Среди них TelSeq, [58] telomereCat [59] и telomereHunter. [60] Оценка длины с помощью WGS обычно работает путем дифференциации считываний секвенирования теломер и последующего определения длины теломер, который произвел это количество считываний. Было показано, что эти методы коррелируют с существующими ранее методами оценки, такими как ПЦР и TRF. Flow-FISH используется для количественного определения длины теломер в лейкоцитах человека. Полуавтоматический метод измерения средней длины теломер с помощью Flow FISH был опубликован в Nature Protocols в 2006 году [61].
Хотя несколько компаний предлагают услуги по измерению длины теломер, полезность этих измерений для широкого клинического или личного использования была поставлена под сомнение. [62] [63] Лауреат Нобелевской премии Элизабет Блэкберн , которая была соучредителем одной компании, пропагандировала клиническую полезность измерения длины теломер. [64]
В ectotherms [ править ]
Большинство исследований длины и регуляции теломер, а также ее связи с раком и старением проводились на млекопитающих, особенно на людях, у которых производство соматической теломеразы незначительно или совсем отсутствует. Эктотермы значительно чаще, чем эндотермы, имеют вариации в экспрессии соматической теломеразы. Например, у многих рыб теломераза встречается по всему телу (и в связи с этим длина теломер примерно одинакова во всех тканях). Исследования эктотерм и других организмов, не относящихся к млекопитающим, показывают, что не существует единой универсальной модели эрозии теломер; скорее, существует большая разница в релевантной динамике в Metazoa.и даже в пределах более мелких таксономических групп эти закономерности кажутся разнообразными. Из-за различных репродуктивных графиков некоторых эктотермов, отбор по болезни актуален для гораздо большей части жизней этих существ, чем для млекопитающих, поэтому длина теломер на ранних и поздних этапах жизни и их возможные связи с раком кажутся особенно важными. важны для этих видов с точки зрения теории жизненного цикла. [65]
См. Также [ править ]
- Биологические часы
- Эпигенетические часы
- Центромера
- Теория повреждений ДНК старения
- Бессмертие
- Максимальный срок службы
- Омоложение (старение)
- Старение , биологическое старение
- Tankyrase
- Теломер-связывающий белок
- G-квартет
- Гипотеза бессмертной цепи ДНК
Заметки [ править ]
- ^ Во время репликации задействованы множественные ДНК-полимеразы.
Ссылки [ править ]
- ^ Mender I, Shay JW (ноябрь 2015). «Протокол повторной амплификации теломеразы (TRAP)» . Биопротокол . 5 (22): e1657. DOI : 10.21769 / bioprotoc.1657 . PMC 4863463 . PMID 27182535 .
- ↑ Blackburn EH, Gall JG (март 1978 г.). «Тандемно повторяющаяся последовательность на концах генов внехромосомной рибосомной РНК в Tetrahymena». Журнал молекулярной биологии . 120 (1): 33–53. DOI : 10.1016 / 0022-2836 (78) 90294-2 . PMID 642006 .
- ^ "Элизабет Х. Блэкберн, Кэрол В. Грейдер, Джек В. Шостак: Нобелевская премия по физиологии и медицине 2009" . Нобелевский фонд. 2009-10-05 . Проверено 12 июня 2012 .
- ^ "Барбара МакКлинток: Нобелевская премия по физиологии и медицине 1983" . Нобелевский фонд. 1983 . Проверено 10 марта 2018 .
- ^ Оловники AM (сентябрь 1973). «Теория маржинотомии. Неполное копирование границы матрицы в ферментативном синтезе полинуклеотидов и биологическое значение явления». Журнал теоретической биологии . 41 (1): 181–90. DOI : 10.1016 / 0022-5193 (73) 90198-7 . PMID 4754905 .
- ^ Chow TT, Zhao Y, Mak SS, Shay JW, Wright WE (июнь 2012). «Ранние и поздние этапы процессинга выступа теломер в нормальных клетках человека: положение последнего праймера РНК управляет укорочением теломер» . Гены и развитие . 26 (11): 1167–78. DOI : 10,1101 / gad.187211.112 . PMC 3371406 . PMID 22661228 .
- ^ Нельсон Д.Л., Ленинджер А.Л., Кокс М. (2008). Принципы биохимии Ленингера (5-е изд.). Нью-Йорк: WH Freeman. ISBN 9780716771081. OCLC 191854286 .
- Перейти ↑ Maloy S (12 июля 2002 г.). «Структура бактериальной хромосомы» . Проверено 22 июня 2008 .
- Перейти ↑ Martínez P, Blasco MA (октябрь 2010 г.). «Роль шелтерина в раке и старении» . Ячейка старения . 9 (5): 653–66. DOI : 10.1111 / j.1474-9726.2010.00596.x . PMID 20569239 .
- ^ Meyne J, Ratliff RL, Moyzis РК (сентябрь 1989). «Сохранение последовательности теломер человека (TTAGGG) n среди позвоночных» . Труды Национальной академии наук Соединенных Штатов Америки . 86 (18): 7049–53. Bibcode : 1989PNAS ... 86.7049M . DOI : 10.1073 / pnas.86.18.7049 . PMC 297991 . PMID 2780561 .
- ^ Lipps HJ, Rhodes D (август 2009). «Структуры G-квадруплекса: доказательства и функции in vivo». Тенденции в клеточной биологии . 19 (8): 414–22. DOI : 10.1016 / j.tcb.2009.05.002 . PMID 19589679 .
- ^ Lanza RP, Cibelli JB, Blackwell C, Cristofalo VJ, Francis MK, Baerlocher GM и др. (Апрель 2000 г.). «Увеличение продолжительности жизни клеток и длины теломер у животных, клонированных из стареющих соматических клеток». Наука . 288 (5466): 665–9. Bibcode : 2000Sci ... 288..665L . DOI : 10.1126 / science.288.5466.665 . PMID 10784448 . S2CID 37387314 .
- ^ Виттемор, Курт; Вера, Эльза; Мартинес-Невадо, Ева; Санпера, Карола; Бласко, Мария А. (2019). «Скорость укорочения теломер предсказывает продолжительность жизни вида» . Труды Национальной академии наук . 116 (30): 15122–15127. DOI : 10.1073 / pnas.1902452116 . ISSN 0027-8424 .
- ^ Shay JW, Wright WE (май 2005). «Старение и бессмертие: роль теломер и теломеразы» . Канцерогенез . 26 (5): 867–74. DOI : 10.1093 / carcin / bgh296 . PMID 15471900 .
- ↑ Wai LK (июль 2004 г.). «Теломеры, теломераза и туморогенез - обзор» . MedGenMed . 6 (3): 19. PMC 1435592 . PMID 15520642 .
- ^ Greider CW (август 1990). «Теломеры, теломераза и старение» . BioEssays . 12 (8): 363–9. DOI : 10.1002 / bies.950120803 . PMID 2241933 . S2CID 11920124 .
- ^ Shampay Дж, Шостак JW, Blackburn EH (1984). «Последовательности ДНК теломер, поддерживаемые дрожжами». Природа . 310 (5973): 154–7. Bibcode : 1984Natur.310..154S . DOI : 10.1038 / 310154a0 . PMID 6330571 . S2CID 4360698 .
- Перейти ↑ Williams TL, Levy DL, Maki-Yonekura S, Yonekura K, Blackburn EH (ноябрь 2010 г.). «Характеристика ядра нуклеопротеина теломер дрожжей: Rap1 независимо связывается с каждым сайтом узнавания» . Журнал биологической химии . 285 (46): 35814–24. DOI : 10.1074 / jbc.M110.170167 . PMC 2975205 . PMID 20826803 .
- ^ Гриффит JD, Комю л, Розенфельд S, Stansel Р. М., Bianchi А, Мосс Н, де Ланге T (май 1999 г.). «Теломеры млекопитающих заканчиваются большой дуплексной петлей». Cell . 97 (4): 503–14. DOI : 10.1016 / S0092-8674 (00) 80760-6 . PMID 10338214 . S2CID 721901 .
- ^ Burge S, Parkinson GN, Желто - P, Тодд AK, Neidle S (2006). «Квадруплексная ДНК: последовательность, топология и структура» . Исследования нуклеиновых кислот . 34 (19): 5402–15. DOI : 10.1093 / NAR / gkl655 . PMC 1636468 . PMID 17012276 .
- ^ a b Eisenberg DT (2011). «Эволюционный обзор биологии теломер человека: гипотеза бережливости теломер и заметки о потенциальных адаптивных отцовских эффектах». Американский журнал биологии человека . 23 (2): 149–67. DOI : 10.1002 / ajhb.21127 . PMID 21319244 . S2CID 5540894 .
- ^ Барнса R, Fouquerel Е, Opresko Р (2019). «Влияние окислительного повреждения ДНК и стресса на гомеостаз теломер» . Механизмы старения и развития . 177 : 37–45. DOI : 10.1016 / j.mad.2018.03.013 . PMC 6162185 .
- ^ Reichert S, Стир A (декабрь 2017). «Укорачивает ли оксидативный стресс теломеры in vivo ? Обзор» . Письма о биологии . 13 (12): 20170463. DOI : 10.1098 / rsbl.2017.0463 . PMC 5746531 . PMID 29212750 .
- ^ Шен Дж., Гаммон MD, Терри МБ, Ван Кью, Брэдшоу П., Тейтельбаум С.Л. и др. (Апрель 2009 г.). «Длина теломер, окислительное повреждение, антиоксиданты и риск рака груди» . Международный журнал рака . 124 (7): 1637–43. DOI : 10.1002 / ijc.24105 . PMC 2727686 . PMID 19089916 .
- ^ a b Mathur MB, Epel E, Kind S, Desai M, Parks CG, Sandler DP, Khazeni N (май 2016 г.). «Воспринимаемый стресс и длина теломер: систематический обзор, метаанализ и методологические соображения для продвижения в этой области» . Мозг, поведение и иммунитет . 54 : 158–169. DOI : 10.1016 / j.bbi.2016.02.002 . PMC 5590630 . PMID 26853993 .
- ^ Лопеса-Otin C, Бласко MA, Партридж L, M Serrano, Кремер G (июнь 2013). «Признаки старения» . Cell . 153 (6): 1194–217. DOI : 10.1016 / j.cell.2013.05.039 . PMC 3836174 . PMID 23746838 .
- Перейти ↑ Alberts B, Johnson A, Lewis J, Morgan D, Raff M, Roberts K, Walter P (2017). Молекулярная биология клетки (шестое изд.). Наука о гирляндах. С. 1230–1233. ISBN 978-1-315-73536-8.
- ↑ Eisenberg DT (17 декабря 2010 г.). «Эволюционный обзор биологии теломер человека: гипотеза бережливости теломер и заметки о потенциальных адаптивных отцовских эффектах». Американский журнал биологии человека . 23 (2): 149–67. DOI : 10.1002 / ajhb.21127 . PMID 21319244 . S2CID 5540894 .
- ^ Aston К.И., охота СК, Сассер Е, Кимура М, Фактор-Литвак Р, Карреллы Д - Авиве (ноябрь 2012 года). «Дивергенция сперматозоидов и лейкоцитов в зависимости от возрастной динамики теломер: последствия для мужской эволюции длины теломер у людей» . Молекулярная репродукция человека . 18 (11): 517–22. DOI : 10.1093 / molehr / gas028 . PMC 3480822 . PMID 22782639 .
- Перейти ↑ Pepper GV, Bateson M, Nettle D (август 2018). «Теломеры как интегративные маркеры подверженности стрессу и невзгодам: систематический обзор и метаанализ» . Королевское общество «Открытая наука» . 5 (8): 180744. Bibcode : 2018RSOS .... 580744P . DOI : 10,1098 / rsos.180744 . PMC 6124068 . PMID 30225068 .
- ^ Rentscher KE, Carroll JE, Mitchell C (апрель 2020). «Психосоциальные стрессоры и длина теломер: современный обзор науки» . Ежегодный обзор общественного здравоохранения . 41 : 223–245. DOI : 10,1146 / annurev-publhealth-040119-094239 . PMID 31900099 .
- ^ Хейфлик L, Мурхэд PS (декабрь 1961). «Серийное культивирование штаммов диплоидных клеток человека». Экспериментальные исследования клеток . 25 (3): 585–621. DOI : 10.1016 / 0014-4827 (61) 90192-6 . PMID 13905658 .
- ^ Hayflick L (март 1965). «Ограниченное время жизни штаммов диплоидных клеток человека in vitro». Экспериментальные исследования клеток . 37 (3): 614–36. DOI : 10.1016 / 0014-4827 (65) 90211-9 . PMID 14315085 .
- ^ Feng J, Funk WD, Wang SS, Weinrich SL, Avilion AA, Chiu CP, et al. (Сентябрь 1995 г.). «РНК-компонент теломеразы человека». Наука . 269 (5228): 1236–41. Bibcode : 1995Sci ... 269.1236F . DOI : 10.1126 / science.7544491 . PMID 7544491 . S2CID 9440710 .
- ^ Bodnar AG, Ouellette M, Frolkis M, Holt SE, Chiu CP, Morin GB, et al. (Январь 1998 г.). «Увеличение продолжительности жизни путем введения теломеразы в нормальные клетки человека». Наука . 279 (5349): 349–52. Bibcode : 1998Sci ... 279..349B . DOI : 10.1126 / science.279.5349.349 . PMID 9454332 . S2CID 35667874 .
- ↑ Образец I (28 ноября 2010 г.). «Гарвардские ученые обращают вспять процесс старения у мышей - теперь и у людей» . Хранитель . Лондон.
- ^ Jaskelioff M, Muller FL, Paik JH, Thomas E, Jiang S, Adams AC и др. (Январь 2011 г.). «Реактивация теломеразы обращает вспять дегенерацию тканей у старых мышей с дефицитом теломеразы» . Природа . 469 (7328): 102–6. Bibcode : 2011Natur.469..102J . DOI : 10,1038 / природа09603 . PMC 3057569 . PMID 21113150 .
- ^ Joeng KS, песни EJ, Ли KJ, Lee J (июнь 2004). «Долгая продолжительность жизни у червей с длинной теломерной ДНК» . Генетика природы . 36 (6): 607–11. DOI : 10.1038 / ng1356 . PMID 15122256 .
- ^ Вайнштейн Б.С., Ciszek D (май 2002). «Гипотеза резервной способности: эволюционное происхождение и современные последствия компромисса между подавлением опухоли и восстановлением тканей». Экспериментальная геронтология . 37 (5): 615–27. DOI : 10.1016 / S0531-5565 (02) 00012-8 . PMID 11909679 . S2CID 12912742 .
- Перейти ↑ Nakagawa S, Gemmell NJ, Burke T (сентябрь 2004 г.). «Измерение теломер позвоночных: приложения и ограничения» (PDF) . Молекулярная экология . 13 (9): 2523–33. DOI : 10.1111 / j.1365-294X.2004.02291.x . PMID 15315667 .
- ^ Juola FA, Осман MF, Дирборн DC, Флек CM (июль 2006). «Укорочение теломер у долгоживущих морских птиц: поперечный анализ и испытание инструмента старения» . Аук . 123 (3): 775–83. DOI : 10.1642 / 0004-8038 (2006) 123 [775: TSIALM] 2.0.CO; 2 . JSTOR 4090554 .
- ^ Гомес Н.М., Райдер О.А., Хаук М.Л., Чартер С.Дж., Уокер В., Форсайт Н.Р. и др. (Октябрь 2011 г.). «Сравнительная биология теломер млекопитающих: гипотезы о предковых состояниях и роли теломер в определении долголетия» . Ячейка старения . 10 (5): 761–8. DOI : 10.1111 / j.1474-9726.2011.00718.x . PMC 3387546 . PMID 21518243 .
- ^ Harris SE, Мартин-Ruiz C, фон Zglinicki T, Starr JM, Deary IJ (июль 2012). «Длина теломер и биомаркеры старения у 70-летних: когорта рождения Лотиана, 1936». Нейробиология старения . 33 (7): 1486.e3–8. DOI : 10.1016 / j.neurobiolaging.2010.11.013 . PMID 21194798 . S2CID 10309423 .
- ^ Джилли D, Blackburn EH (март 1994). «Отсутствие укорочения теломер во время старения у Paramecium» . Труды Национальной академии наук Соединенных Штатов Америки . 91 (5): 1955–8. Bibcode : 1994PNAS ... 91.1955G . DOI : 10.1073 / pnas.91.5.1955 . PMC 43283 . PMID 8127914 .
- ^ Peška V, Fajkus P, Fojtová M, Dvořáčková M, Hapala J, Dvořáček V и др. (Май 2015 г.). «Характеристика необычного мотива теломер (TTTTTTAGGG) n у растения Cestrum elegans (Solanaceae), вида с большим геномом». Заводской журнал . 82 (4): 644–54. DOI : 10.1111 / tpj.12839 . PMID 25828846 .
- ^ Файкус П., Пешка В., Ситова З., Фулнечкова Ю., Дворжачкова М., Гогела Р. и др. (Февраль 2016 г.). «Теломеры лука обнажены: необычная теломерная последовательность (CTCGGTTATGGG) n синтезируется теломеразой» . Заводской журнал . 85 (3): 337–47. DOI : 10.1111 / tpj.13115 . PMID 26716914 . S2CID 206331112 .
- ^ a b Price LH, Kao HT, Burgers DE, Carpenter LL, Tyrka AR (январь 2013 г.). «Теломеры и стресс в молодом возрасте: обзор» . Биологическая психиатрия . 73 (1): 15–23. DOI : 10.1016 / j.biopsych.2012.06.025 . PMC 3495091 . PMID 22831981 .
- ^ Рейно CM, Сабатье L, Philipot O, Olaussen К.А., Сория JC (май 2008). «Длина теломер, теломерные белки и геномная нестабильность во время многоступенчатого канцерогенного процесса». Критические обзоры в онкологии / гематологии . 66 (2): 99–117. DOI : 10.1016 / j.critrevonc.2007.11.006 . PMID 18243729 .
- ^ Бласко MA, Ли HW, Hande MP, Сампера E, Лэнсдорп PM, DePinho RA, Грейдер CW (октябрь 1997). «Укорочение теломер и образование опухолей мышиными клетками, лишенными теломеразной РНК». Cell . 91 (1): 25–34. DOI : 10.1016 / s0092-8674 (01) 80006-4 . PMID 9335332 . S2CID 13366934 .
- ^ Artandi SE, Чанг S, Ли SL, Alson S, Gottlieb GJ, Чин L, DePinho RA (август 2000). «Дисфункция теломер способствует невзаимным транслокациям и эпителиальному раку у мышей». Природа . 406 (6796): 641–5. Bibcode : 2000Natur.406..641A . DOI : 10.1038 / 35020592 . PMID 10949306 . S2CID 4420387 .
- ^ a b Armanios M (март 2013 г.). «Теломеры и возрастные заболевания: как биология теломер влияет на клинические парадигмы» . Журнал клинических исследований . 123 (3): 996–1002. DOI : 10.1172 / JCI66370 . PMC 3673231 . PMID 23454763 .
- ^ Willeit P, Willeit J, Mayr A, Weger S, Oberhollenzer F, Brandstätter A и др. (Июль 2010 г.). «Длина теломер и риск возникновения рака и смертность от рака» . ДЖАМА . 304 (1): 69–75. DOI : 10,1001 / jama.2010.897 . PMID 20606151 .
- ^ Ma H, Zhou Z, Wei S, Liu Z, Pooley KA, Dunning AM и др. (2011). «Укороченная длина теломер связана с повышенным риском рака: метаанализ» . PLOS ONE . 6 (6): e20466. Bibcode : 2011PLoSO ... 620466M . DOI : 10.1371 / journal.pone.0020466 . PMC 3112149 . PMID 21695195 .
- ^ Wentzensen IM, Mirabello L, Pfeiffer RM, Savage SA (июнь 2011). «Связь длины теломер и рака: метаанализ» . Эпидемиология, биомаркеры и профилактика рака . 20 (6): 1238–50. DOI : 10.1158 / 1055-9965.epi-11-0005 . PMC 3111877 . PMID 21467229 .
- ^ Allshire RC и др. (Июнь 1989 г.). «Человеческие теломеры содержат по крайней мере три типа G-богатых повторов, распределенных неслучайно» . Исследования нуклеиновых кислот . 17 (12): 4611–27. DOI : 10.1093 / NAR / 17.12.4611 . PMC 318019 . PMID 2664709 .
- ^ Rufer N, et al. (Август 1998 г.). «Динамика длины теломер в субпопуляциях лимфоцитов человека, измеренная с помощью проточной цитометрии». Природа Биотехнологии . 16 (8): 743–7. DOI : 10.1038 / nbt0898-743 . PMID 9702772 . S2CID 23833545 .
- ^ Cawthon RM (май 2002). «Измерение теломер с помощью количественной ПЦР» . Исследования нуклеиновых кислот . 30 (10): 47e – 47. DOI : 10.1093 / NAR / 30.10.e47 . PMC 115301 . PMID 12000852 .
- Перейти ↑ Ding Z (2014). «Оценка длины теломер по данным последовательности всего генома» . Исследования нуклеиновых кислот . 42 (9): e75. DOI : 10.1093 / NAR / gku181 . PMC 4027178 . PMID 24609383 .
- ^ Фармери J (2018). «TelomereCat: независимый от плоидности метод оценки длины теломер на основе данных секвенирования всего генома» . Научные отчеты . 8 (1): 1300. Bibcode : 2018NatSR ... 8.1300F . DOI : 10.1038 / s41598-017-14403-у . PMC 5778012 . PMID 29358629 .
- Перейти ↑ Feuerbach L (2019). «TelomereHunter - in silico оценка содержания и состава теломер из геномов рака» . BMC Bioinformatics . 20 (1): 272. DOI : 10,1186 / s12859-019-2851-0 . PMC 6540518 . PMID 31138115 .
- ^ Baerlocher GM, Vulto я, де Йонг G, Лэнсдорп PM (декабрь 2006). «Проточная цитометрия и FISH для измерения средней длины теломер (проточная FISH)». Протоколы природы . 1 (5): 2365–76. DOI : 10.1038 / nprot.2006.263 . PMID 17406480 . S2CID 20463557 .
- ↑ Поллак, Эндрю (18 мая 2011 г.). «Анализ крови подсказывает ключ к долголетию» . Нью-Йорк Таймс .
- ^ фон Zglinicki T (март 2012). «Будут ли ваши теломеры предсказать ваше будущее?». BMJ . 344 : e1727. DOI : 10.1136 / bmj.e1727 . PMID 22415954 . S2CID 44594597 .
- Перейти ↑ Marchant J (2011). «Тест на плевок предлагает путеводитель по здоровью». Природа . DOI : 10.1038 / news.2011.330 .
- ^ Олссон M, Wapstra E, Фризен C (март 2018). «Эктотермические теломеры: пора с холода приходить» . Философские труды Лондонского королевского общества. Серия B, Биологические науки . 373 (1741): 20160449. DOI : 10.1098 / rstb.2016.0449 . PMC 5784069 . PMID 29335373 .
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме теломер . |
- Теломеры и теломераза: средство для достижения цели Нобелевская лекция Элизабет Блэкберн , в которой говорится о влиянии стресса и пессимизма на длину теломер
- Теломераза и последствия дисфункции теломер Нобелевская лекция Кэрол Грейдер
- Концы ДНК: только начало Нобелевской лекции Джека Шостака