 | |
| Имена | |
|---|---|
| Название ИЮПАК ( E ) -циклооктен | |
| Другие имена транс- циклооктен | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
| Номер ЕС |
|
PubChem CID | |
| |
| |
| Характеристики | |
| С 8 Н 14 | |
| Молярная масса | 110.200 г · моль -1 |
| Внешность | бесцветная жидкость |
| Плотность | 0,848 г / мл |
| Температура плавления | -59 ° С (-74 ° F, 214 К) |
| Точка кипения | 143 ° С (1 атм); 68-72 ° C (100 торр) [2] |
| Опасности | |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Опасность |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
транс- Циклооктен представляет собой циклический углеводород с формулой [- (CH 2 ) 6 CH = CH–], где две одинарные связи C – C, смежные с двойной связью, находятся на противоположных сторонах плоскости последней. Это бесцветная жидкость с неприятным запахом.
Циклооктен примечателен как самый маленький циклоалкена , который легко выделяют в виде его транс - изомера . В цис - изомер является гораздо более стабильным; [3] энергия кольцевой деформации составляет 16,7 и 7,4 ккал / моль соответственно. [4]
 | 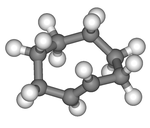 |
| цис- циклооктен | транс- циклооктен |
Плоская компоновка кольцевых атомов углерода будет слишком натянутыми, и , следовательно , устойчивые конформации по транс - формы имеют изогнутую (неплоской) кольцо. Расчеты показывают, что наиболее стабильная конформация «корона» имеет атомы углерода попеременно выше и ниже плоскости кольца. [5] Конформация «полукресло», с примерно на 6 ккал / моль более высокой энергией, имеет атомы углерода 2, 3, 5, 6 и 8 на той же стороне плоскости атомов углерода 1, 4 и 7. [5 ]
Все конформации транс- циклооктена являются хиральными (в частности, то, что некоторые называют планарно-хиральными [6] ), и энантиомеры могут быть разделены. [7] [8] [9] Теоретически преобразование между энантиомерами может быть выполнено без разрыва каких-либо связей, жестко скручивая всю группу –CH = CH– на 180 градусов. Однако это влечет за собой прохождение одного из его водородов через переполненное кольцо. [7]
Подготовка [ править ]
транс- Циклооктен был впервые синтезирован в предварительном масштабе Артуром С. Копом с помощью реакции элиминирования Хофмана N, N, N -триметилциклооктиламмониййодида. [10] Реакция дает смесь цис- и транс- изомеров, и транс- изомер селективно улавливается в виде комплекса с нитратом серебра .
Существуют и другие методы, в которых транс- изомер синтезируют из цис- изомера в несколько этапов синтеза. Например, его можно получить с почти 100% выходом путем превращения цис- изомера в 1,2-эпоксициклооктан («циклооктеноксид») с последующими реакциями с дифенилфосфидом лития ( LiPPh
2) и с метилиодидом CH
3Я . (Подобные процедуры могут дать цис- , транс- изомеры 1,4-циклооктадиена и 1,5-циклооктадиена ). [2]
Кроме того, фотохимический метод существует для прямого циса - транс - изомеризации. Хотя это равновесие сильно способствует более стабильной цис- форме, реакция может быть направлена в сторону транс- формы за счет захвата ионами серебра. [11] [12]
Реакции [ править ]
Из-за более высокого внутреннего напряжения двойной связи транс- изомер более реакционноспособен, чем цис- изомер и типичные ненасыщенные углеводороды. Например, его двойная связь будет быстро добавлять тетразин и его производные. [5] Соединение также легко полимеризуется с инициатором на основе рутения . [4]
Ссылки [ править ]
- ^ « цис- циклооктен» . Сигма-Олдрич .
- ^ a b Эдвин Ведейс, Карел А. Дж. Снобл и Филип Л. Фукс (1973): «Бетаины фосфора, полученные из циклогептена и оксидов циклооктена. Инверсия циклооктенов». Журнал органической химии , том 38, выпуск 6, страницы 1178–1183. DOI : 10.1021 / jo00946a024
- ^ Нойеншвандер, Ульрих; Германс, Айв (2011). «Конформации циклооктена: последствия для химии эпоксидирования». J. Org. Chem. 76 (24): 10236–10240. DOI : 10.1021 / jo202176j .
- ^ Б Рон Уокер, Розмари М. Конрад, и Граббс (2009): «Живые ROMP из транса -cyclooctene». Макромолекулы , том 42, выпуск 3, страницы 599–605. DOI : 10.1021 / ma801693q
- ^ a b c Рамаджеям Селварадж, Джозеф М. Фокс « транс- циклооктен - стабильный, прожорливый диенофил для биоортогональной маркировки». Текущее мнение по химической биологии , том 17, выпуск 5, страницы 753-760 doi : 10.1016 / j.cbpa.2013.07.031
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Онлайн-исправленная версия: (2006–) « Плоская хиральность ». DOI : 10,1351 / goldbook.P04681
- ^ а б Артур С. Коуп, CR Ganellin, HW Johnson, TV Van Auken и Hans JS Winkler (193): "Молекулярная асимметрия олефинов. I. Разрешение транс- циклооктена". Журнал Американской химической ассоциации , том 85, выпуск 20, страницы 3276–3279. DOI : 10.1021 / ja00903a049
- ^ Артур С. Коуп и Анил С. Мехта (1964): «Молекулярная асимметрия олефинов. II. Абсолютная конфигурация транс- циклооктена». Журнал Американской химической ассоциации , том 86, выпуск 24, страницы 5626–5630. DOI : 10.1021 / ja01078a044
- ^ Стивен Д. Пэджет (2001). «(-) - Дихлор (этилен) (α-метилбензиламин) платина (II)». Энциклопедия реагентов для органического синтеза . Джон Вили и сыновья. DOI : 10.1002 / 047084289X.rd119 .CS1 maint: использует параметр авторов ( ссылка )
- ^ Коп, Артур С .; Бах, Роберт Д. (1969). « транс- циклооктен» . Органический синтез . 49 : 39.; Сборник , 5 , с. 315
- ^ Джон С. Свентон (1969): "Фотоизомеризация цис- циклооктена до транс- циклооктена". Журнал органической химии , том 34, выпуск 10, страницы 3217–3218. DOI : 10.1021 / jo01262a102
- ^ Ройзен Максим; Yap, Glenn PA; Фокс, Джозеф М. (2008). «Фотохимический синтез функционализированных транс- циклооктенов за счет комплексообразования металлов». Варенье. Chem. Soc. 130 (12): 3760–3761. DOI : 10.1021 / ja8001919 .