| триозофосфат изомераза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
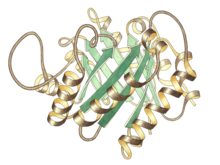 Вид сбоку мономера триозоп-изомеразы, активный центр вверху в центре | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 5.3.1.1 | ||||||||
| Количество CAS | 9023-78-3 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| BRENDA | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| Структуры PDB | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | Amigo / QuickGO | ||||||||
| |||||||||
Триозы-фосфат - изомераза ( ТПИТЕ или ТИМ ) представляет собой фермент ( ЕС 5.3.1.1 ) , который катализирует обратимое взаимопревращение в триозах фосфатного изомеры дигидроксиацетонфосфат и D - глицеральдегид - 3-фосфата .
| Дигидроксиацетонфосфат | триозофосфат изомераза | D - глицеральдегид 3-фосфат | |
 |  | ||
 | |||
| триозофосфат изомераза | |||
Соединение C00111 в базе данных KEGG Pathway. Фермент 5.3.1.1 в базе данных KEGG Pathway. Соединение C00118 в базе данных KEGG Pathway.
TPI играет важную роль в гликолизе и необходим для эффективного производства энергии. TPI был обнаружен почти в каждом организме, в котором проводился поиск фермента, включая животных, таких как млекопитающие и насекомые, а также в грибах , растениях и бактериях . Однако у некоторых бактерий, не осуществляющих гликолиз, например уреаплазмы , TPI отсутствует.
У людей дефицит TPI связан с прогрессирующим тяжелым неврологическим расстройством, называемым дефицитом триозофосфатизомеразы . Дефицит триозофосфатизомеразы характеризуется хронической гемолитической анемией . Хотя существуют различные мутации , вызывающие это заболевание, большинство из них включает мутацию глутаминовой кислоты в положении 104 на аспарагиновую кислоту. [1]
Триозофосфатизомераза - это высокоэффективный фермент, который в миллиарды раз выполняет реакцию быстрее, чем это могло бы происходить в растворе в естественных условиях. Реакция настолько эффективна, что считается каталитически совершенной : она ограничена только скоростью, с которой субстрат может диффундировать в активный центр фермента и из него. [2] [3]
Механизм [ править ]
Механизм включает промежуточное образование «эндиола» . Относительная свободная энергия каждого основного состояния и переходного состояния была определена экспериментально и показана на рисунке. [2]
Структура TPI способствует превращению дигидроксиацетонфосфата (DHAP) в глицеральдегид-3-фосфат (GAP). Нуклеофильный глутамат 165 остаток ТПИТЕ deprotonates на подложке , [4] и электрофильный гистидин 95 остаток жертвует протон , чтобы сформировать enediol промежуточного соединения. [5] [6] При депротонировании ендиолят затем коллапсирует и, отрывая протон от протонированного глутамата 165, образует продукт GAP. Катализ обратной реакции протекает аналогично, образуя тот же ендиол, но с коллапсом ендиолата из кислорода при C2. [7]
ТПИ ограничен диффузией. С точки зрения термодинамики, образование DHAP в соотношении 20: 1 предпочтительнее, чем образование GAP. [8] Однако при гликолизе использование GAP на последующих этапах метаболизма стимулирует реакцию на его производство. TPI ингибируется ионами сульфата , фосфата и арсената , которые связываются с активным центром . [9] Другие ингибиторы включают 2-фосфогликолят, аналог переходного состояния , и D-глицерин-1-фосфат, аналог субстрата . [10]
Структура [ править ]
| Триозофосфат изомераза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Символ | ТИМ | ||||||||
| Pfam | PF00121 | ||||||||
| Клан пфам | CL0036 | ||||||||
| ИнтерПро | IPR000652 | ||||||||
| PROSITE | PDOC00155 | ||||||||
| SCOP2 | 1 т / ч / SCOPe / SUPFAM | ||||||||
| |||||||||
Триозофосфатизомераза представляет собой димер идентичных субъединиц , каждая из которых состоит примерно из 250 аминокислотных остатков. Трехмерная структура субъединицы содержит восемь α-спиралей снаружи и восемь параллельных β-тяжей внутри. На иллюстрации ленточный каркас каждой субъединицы окрашен от синего до красного от N-конца к C-концу. Этот структурный мотив называется αβ-стволом или TIM-стволом , и на сегодняшний день он является наиболее часто наблюдаемой белковой складкой . Активный сайт этого фермента находится в центре ствола. Кислоты глутаминовой остаток и гистидинучаствуют в каталитическом механизме . Последовательность вокруг остатков активного сайта сохраняется во всех известных триозофосфат-изомеразах.
Структура триозофосфат-изомеразы способствует ее функции. Помимо точно размещенных остатков глутамата и гистидина для образования эндиола, цепь TPI из десяти или одиннадцати аминокислот действует как петля для стабилизации промежуточного продукта. Петля, образованная остатками от 166 до 176, замыкается и образует водородную связь с фосфатной группой субстрата. Это действие стабилизирует промежуточное соединение эндиола и другие переходные состояния на пути реакции. [7]
Помимо того, что реакция становится кинетически возможной, петля TPI изолирует реакционноспособный промежуточный эндиол, чтобы предотвратить разложение до метилглиоксаля и неорганического фосфата. Водородная связь между ферментом и фосфатной группой субстрата делает такое разложение стереоэлектронно невыгодным. [7] Метилглиоксаль - это токсин, который в случае образования удаляется через систему глиоксалазы . [11] Потеря высокоэнергетической фосфатной связи и субстрата для остальной части гликолиза делает образование метилглиоксаля неэффективным.
Исследования показывают, что лизин, расположенный рядом с активным центром (в положении 12), также имеет решающее значение для функции фермента. Лизин, протонированный при физиологическом pH, может помочь нейтрализовать отрицательный заряд фосфатной группы. Когда этот лизин превращается в нейтральную аминокислоту, TPI теряет все функции, но мутанты с другой положительно заряженной аминокислотой сохраняют некоторую функцию. [12]
См. Также [ править ]
- ТИМ ствол
- Дефицит триозофосфат-изомеразы
- TPI1
- Триозофосфат-изомераза в интерактивном 3D в Proteopedia
- Семейство триозофосфатизомеразы (TIM) в PROSITE
Ссылки [ править ]
- ^ Орос F, J Oláh, Ovádi J (декабрь 2006). «Дефицит триозофосфатизомеразы: факты и сомнения» . IUBMB Life . 58 (12): 703–15. DOI : 10.1080 / 15216540601115960 . PMID 17424909 .
- ^ Б Альбери WJ Ноулз JR (декабрь 1976). «Профиль свободной энергии реакции, катализируемой триозофосфатизомеразой». Биохимия . 15 (25): 5627–31. DOI : 10.1021 / bi00670a031 . PMID 999838 .
- ^ Rose IA, Fung WJ, Warms СП (май 1990). «Диффузия протонов в активном центре триозофосфатизомеразы». Биохимия . 29 (18): 4312–7. DOI : 10.1021 / bi00470a008 . PMID 2161683 .
- ^ Альбер Т., Баннер Д.В., Блумер А.С., Петско Г.А., Филлипс Д., Риверс П.С., Уилсон И.А. (июнь 1981 г.). «О трехмерной структуре и каталитическом механизме триозофосфатизомеразы» . Философские труды Лондонского королевского общества. Серия B, Биологические науки . 293 (1063): 159–71. DOI : 10.1098 / rstb.1981.0069 . PMID 6115415 .
- ^ Nickbarg EB, Davenport RC, Petsko Г.А., Knowles JR (август 1988). «Триозофосфатизомераза: удаление предположительно электрофильного остатка гистидина приводит к незначительному изменению каталитического механизма». Биохимия . 27 (16): 5948–60. DOI : 10.1021 / bi00416a019 . PMID 2847777 .
- ^ Komives EA, Chang LC, Lolis E, Tilton РФ, Petsko Г.А., Knowles JR (март 1991). «Электрофильный катализ в триозофосфатизомеразе: роль гистидина-95». Биохимия . 30 (12): 3011–9. DOI : 10.1021 / bi00226a005 . PMID 2007138 .
- ^ a b c Ноулз-младший (март 1991 г.). «Ферментный катализ: не иначе, просто лучше». Природа . 350 (6314): 121–4. DOI : 10.1038 / 350121a0 . PMID 2005961 .
- ^ Харрис Т., Коул Р.Н., Comer FI, Mildvan AS (ноябрь 1998). «Перенос протона в механизме триозофосфатизомеразы». Биохимия . 37 (47): 16828–38. DOI : 10.1021 / bi982089f . PMID 9843453 .
- ^ Lambeir AM, Opperdoes FR, Wierenga РК (октябрь 1987). «Кинетические свойства триозофосфатизомеразы из Trypanosoma brucei brucei. Сравнение с мышечными и дрожжевыми ферментами кролика» . Европейский журнал биохимии . 168 (1): 69–74. DOI : 10.1111 / j.1432-1033.1987.tb13388.x . PMID 3311744 .
- ^ Lolis E, Petsko Г.А. (июль 1990). «Кристаллографический анализ комплекса между триозофосфатизомеразой и 2-фосфогликолятом при разрешении 2,5 А: значение для катализа». Биохимия . 29 (28): 6619–25. DOI : 10.1021 / bi00480a010 . PMID 2204418 .
- ↑ Creighton DJ, Hamilton DS (март 2001 г.). «Краткая история глиоксалазы I и то, что мы узнали о зависимой от ионов металлов, ферментативно-катализируемой изомеризации». Архивы биохимии и биофизики . 387 (1): 1–10. DOI : 10,1006 / abbi.2000.2253 . PMID 11368170 .
- ^ Лоди PJ, Chang LC Ноулз JR, Komives EA (март 1994). «Триозофосфатизомераза требует положительно заряженного активного сайта: роль лизина-12». Биохимия . 33 (10): 2809–14. DOI : 10.1021 / bi00176a009 . PMID 8130193 .
Внешние ссылки [ править ]
- PDBe-KB предоставляет обзор всей структурной информации, доступной в PDB для триозофосфатизомеразы человека.
| vте Путь метаболизма гликолиза |
|---|
Глюкоза Гексокиназа АТФ ADP Глюкозо-6-фосфат Глюкозо-6-фосфат- изомераза Фруктоза 6-фосфат Фосфофруктокиназа-1 АТФ ADP 1,6-бисфосфат фруктозы Фруктозо-бисфосфат альдолаза Дигидроксиацетонфосфат + + Глицеральдегид 3-фосфат Триозофосфат изомераза 2 × Глицеральдегид-3-фосфат 2 × Глицеральдегид-3- фосфатдегидрогеназа НАД + + P i НАДН + Н + НАД + + P i НАДН + Н + 2 × 1,3-бисфосфоглицерат 2 × Фосфоглицераткиназа ADP АТФ ADP АТФ 2 × 3-фосфоглицерат 2 × Фосфоглицерат мутаза 2 × 2-фосфоглицерат 2 × Phosphopyruvate гидратаз ( енолаз ) H 2 O H 2 O 2 × Фосфоенолпируват 2 × Пируваткиназа ADP АТФ 2 × Пируват 2 × |