Нитраты щелочных металлов - это химические соединения, состоящие из щелочного металла ( лития , натрия , калия , рубидия и цезия ) и нитрат- иона. Только две из них имеют большую коммерческую ценность - соли натрия и калия. [1] [2] Это белые водорастворимые соли с относительно близкими температурами плавления. [3]
| Сложный | Химическая формула | Молярная масса | Температура плавления | состав |
|---|---|---|---|---|
| Нитрат лития | LiNO 3 | 68,946 г / моль | 255 ° С (491 ° F, 528 К) |  |
| Нитрат натрия | NaNO 3 | 84,9947 г / моль | 308 ° С (586 ° F, 581 ° К) | 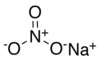 |
| Азотнокислый калий | KNO 3 | 101,1032 г / моль | 334 ° С (633 ° F, 607 К) |  |
| Нитрат рубидия | RbNO 3 | 147,473 г / моль | 310 ° С (590 ° F, 583 К) |  |
| Нитрат цезия | CsNO 3 | 194,91 г / моль | 414 ° С (777 ° F, 687 К) |  |
Приложения [ править ]
В основном нитраты щелочных металлов используются в удобрениях в случае производных натрия и калия. Они также широко используются во взрывчатых веществах и пиротехнических составах ; [1] они являются сильными окислителями. Другие виды использования для окрашивания в пиротехнических : Нитрат цезия производит индиго цвет, нитрат калия и рубидия нитрата производят фиолетовые цвета, нитрат лития производит красный цвет, и нитрат натрия дает желтый цвет. [4]
Нитрат натрия и калия также широко используются в качестве удобрений.
См. Также [ править ]
Ссылки [ править ]
- ^ a b Вольфганг Лауэ, Майкл Тиманн, Эрих Шайблер, Карл Вильгельм Виганд «Нитраты и нитриты» в Энциклопедии промышленной химии Ульмана , 2006, Wiley-VCH, Weinheim. DOI : 10.1002 / 14356007.a17_265
- ^ [email protected], Йинон Бентор -. «Chemical Elements.com - Щелочные металлы» . www.chemicalelements.com . Проверено 26 сентября 2016 .
- ^ "ТЕРМОДИНАМИЧЕСКИЕ СВОЙСТВА РАСПЛАВЛЕННЫХ НИТРАТНЫХ СОЛЕЙ" (PDF) .
- ^ «Фантомный фейерверк: Университет фейерверков: пиротехнические соединения» . Фантомный фейерверк . Архивировано из оригинала на 2020-08-06 . Проверено 16 октября 2016 .
