 | |
| Имена | |
|---|---|
| Систематическое название ИЮПАК Нитрат | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ChemSpider | |
PubChem CID | |
| UNII | |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| НЕТ- 3 | |
| Молярная масса | 62,004 г · моль -1 |
| Конъюгированная кислота | Азотная кислота |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Нитрат - это многоатомный ион с химической формулой NO.-
3. Соли, содержащие этот ион , называются нитратами . Нитраты - обычные компоненты удобрений и взрывчатых веществ. [1] Почти все неорганические нитраты растворимы в воде . Примером нерастворимого нитрата является оксинитрат висмута . Удаление одного электрона дает нитратный радикал , также называемый триоксидом азота NO.
3.
Структура [ править ]
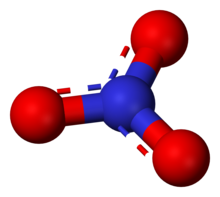
Ион является сопряженным основанием из азотной кислоты , состоящее из одного центрального азота атома в окружении трех одинаково связанных атомами кислорода в тригональной плоской договоренности. Нитрат-ион несет формальный заряд -1. Этот заряд является результат комбинации формального заряда , в котором каждый из трех атомов кислорода несет в себе - 2 / 3 заряда, в то время как азот несет заряд +1, все эти добавления до формального заряда многоатомного иона нитрата. Такое расположение обычно используется в качестве примера резонанса . Как изоэлектронный карбонат иона нитрат-ион может быть представлен резонансными структурами:
Пищевые нитраты [ править ]
Богатый источник неорганических нитратов в рационе человека - это листовые зеленые продукты, такие как шпинат и руккола . НЕТ-
3(неорганический нитрат) является жизнеспособным активным компонентом свекольного сока и других овощей. Питьевая вода также является диетическим источником. [2]
Добавка нитратов дает положительные результаты при тестировании результатов упражнений на выносливость. [3]
Прием больших доз нитрата в форме чистого нитрата натрия или свекольного сока у молодых здоровых людей быстро увеличивает концентрацию нитратов в плазме примерно в 2-3 раза, и эта повышенная концентрация нитратов может сохраняться в течение как минимум 2 недель. Повышенный уровень нитратов в плазме стимулирует выработку оксида азота. Оксид азота является важной физиологической сигнальной молекулой, которая используется, среди прочего, в регулировании кровотока в мышцах и дыхания митохондрий. [4]
Колбасные изделия [ править ]
Потребление нитритов в первую очередь определяется количеством съеденного обработанного мяса и концентрацией нитратов в этом мясе. Хотя нитриты - это азотистые соединения, которые в основном используются при консервировании мяса, нитраты также используются. Нитраты приводят к образованию нитрозаминов . [5] Производство канцерогенных нитрозаминов может быть подавлено за счет использования антиоксидантов витамина С и альфа-токоферольной формы витамина Е во время лечения. [6]
Антигипертензивные диеты, такие как диета DASH , обычно содержат высокие уровни нитратов, которые сначала восстанавливаются до нитритов в слюне, как это обнаруживается при тестировании слюны , до образования оксида азота . [2]
Возникновение и производство [ править ]
Нитратные соли найдены естественно на земле , как крупные месторождения, в частности нитронатрит , основной источник нитрата натрия.
Нитраты производятся рядом видов нитрифицирующих бактерий , а нитратные соединения для пороха (подробнее см. В этой теме) исторически производились в отсутствие источников минеральных нитратов с помощью различных процессов ферментации с использованием мочи и навоза.
В качестве побочного продукта ударов молнии в атмосфере, богатой азотом и кислородом Земли, азотная кислота образуется при взаимодействии диоксида азота с водяным паром.
Нитраты производятся промышленным способом из азотной кислоты . [1]
Использует [ редактировать ]
Нитраты в основном производятся для использования в качестве удобрений в сельском хозяйстве из-за их высокой растворимости и способности к биологическому разложению. Основные нитратные удобрения - соли аммония , натрия , калия , кальция и магния . Для этого ежегодно производится несколько миллионов килограммов. [1]
Второе основное применение нитратов - это окислители, особенно во взрывчатых веществах, где быстрое окисление углеродных соединений высвобождает большие объемы газов (см. , Например, порох ). Нитрат натрия используется для удаления пузырьков воздуха из расплавленного стекла и некоторых керамических изделий. Смеси расплавленной соли используются для упрочнения некоторых металлов. [1]
Обнаружение [ править ]
Практически все методы обнаружения нитратов основаны на его преобразовании в нитрит с последующим проведением тестов на нитриты. Восстановление нитрата до нитрита осуществляется медно-кадмиевым материалом. Проба вводится с помощью анализатора впрыска потока, и полученный нитритсодержащий сток затем объединяется с реагентом для колориметрического или электрохимического обнаружения. Самым популярным из этих анализов является тест Грисса , при котором нитрит превращается в сильно окрашенный азокраситель , подходящий для спектроскопического анализа в УФ-видимой области. В методе используется реакционная способность азотистой кислоты, полученной при подкислении нитрита. Азотистая кислота избирательно реагирует с ароматическими аминами с образованием солей диазония, которые, в свою очередь, соединяются со вторым реагентом, давая азокраситель. Предел обнаружениясоставляет от 0,02 до 2 мкМ. [7] Методы были адаптированы к биологическим образцам. [8]
Безопасность [ править ]
Острая токсичность нитратов невысока. Существуют «существенные разногласия» относительно долгосрочных рисков воздействия нитратов. Две области, которые могут вызывать беспокойство, заключаются в том, что (i) нитрат может быть предшественником нитрита в нижнем отделе кишечника, а нитрит является предшественником нитрозаминов, которые участвуют в канцерогенезе, и (ii) нитрат участвует в метгемоглобинемии , расстройстве гемоглобин эритроцитов. [9] [10]
Метгемоглобинемия [ править ]
Нитраты не действуют на младенцев и беременных. [11] [12] Синдром синего ребенка вызван рядом других факторов, таких как расстройство желудка, например, диарейная инфекция, непереносимость белков, токсичность тяжелых металлов и т. Д., При этом нитраты играют второстепенную роль. [13]
Стандарты питьевой воды [ править ]
В Законе о безопасной питьевой воде Агентство по охране окружающей среды США установило максимальный уровень загрязнения 10 мг / л или 10 частей на миллион нитратов в питьевой воде. [14]
Совместным комитетом экспертов ФАО / ВОЗ по пищевым добавкам (JEFCA) была установлена приемлемая суточная доза (ДСД) нитрат-ионов в диапазоне 0–3,7 мг (кг массы тела) -1 день -1 . [15]
Водная токсичность [ править ]
В пресноводных или эстуарных системах вблизи суши концентрация нитратов может достигать смертельных для рыб концентраций. Хотя нитраты намного менее токсичны, чем аммиак, [16] уровни нитратов более 30 ppm могут подавлять рост, ослаблять иммунную систему и вызывать стресс у некоторых водных видов. [17] Нитратная токсичность остается предметом споров. [18]
В большинстве случаев избыточных концентраций нитратов в водных системах основным источником является поверхностный сток с сельскохозяйственных или ландшафтных территорий, которые получили избыток нитратных удобрений. В результате эвтрофикация и цветение водорослей приводят к аноксии и мертвым зонам . Как следствие, поскольку нитраты составляют компонент всех растворенных твердых веществ , они широко используются в качестве индикатора качества воды .
Корм для домашних животных [ править ]
Симптомы отравления нитратами у домашних животных включают учащение пульса и дыхания; в запущенных случаях кровь и ткани могут стать синими или коричневыми. Корм можно проверить на нитраты; обработка состоит из дополнения или замены существующих запасов материалом с более низким содержанием нитратов. Безопасные уровни нитратов для различных видов домашнего скота следующие: [19]
| Категория | % НЕТ 3 | % NO 3 –N | % KNO 3 | Последствия |
|---|---|---|---|---|
| 1 | <0,5 | <0,12 | <0,81 | В целом безопасно для мясного скота и овец |
| 2 | 0,5–1,0 | 0,12–0,23 | 0,81–1,63 | Внимание: некоторые субклинические симптомы могут проявляться у беременных лошадей, овец и мясного скота. |
| 3 | 1.0 | 0,23 | 1,63 | Проблемы с высоким содержанием нитратов: гибель крупного рогатого скота и овец могут быть причиной абортов. |
| 4 | <1,23 | <0,28 | <2,00 | Максимально безопасный уровень для лошадей. Не кормите беременных кобыл фуражами с высоким содержанием нитратов. |
Вышеуказанные значения указаны для сухой (без влаги) основы.
Соли и ковалентные производные [ править ]
Образование нитратов с элементами таблицы Менделеева.
| HNO 3 | Он | ||||||||||||||||
| LiNO 3 | Быть (NO 3 ) 2 | B (НЕТ3)- 4 | RONO 2 | НЕТ- 3 NH 4 NO 3 | HOONO 2 | FNO 3 | Ne | ||||||||||
| NaNO 3 | Mg (NO 3 ) 2 | Al (NO 3 ) 3 | Si | п | S | ClONO 2 | Ar | ||||||||||
| KNO 3 | Ca (NO 3 ) 2 | СБН (№ 3 ) 3 | Ti (NO 3 ) 4 | VO (NO 3 ) 3 | Cr (NO 3 ) 3 | Mn (NO 3 ) 2 | Fe (NO 3 ) 2 Fe (NO 3 ) 3 | Co (NO 3 ) 2 Co (NO 3 ) 3 | Ni (NO 3 ) 2 | CuNO 3 Cu (NO 3 ) 2 | Zn (NO 3 ) 2 | Ga (NO 3 ) 3 | Ge | В качестве | Se | Br | Kr |
| RbNO 3 | Sr (NO 3 ) 2 | Д (НЕТ 3 ) 3 | Zr (NO 3 ) 4 | Nb | Пн | Tc | Ru (NO 3 ) 3 | Rh (NO 3 ) 3 | Pd (NO 3 ) 2 Pd (NO 3 ) 4 | AgNO 3 Ag (NO 3 ) 2 | Cd (NO 3 ) 2 | В (NO 3 ) 3 | Sn | Сб (NO 3 ) 3 | Te | INO 3 | Xe (NO 3 ) 2 |
| CsNO 3 | Ba (NO 3 ) 2 | Hf (NO 3 ) 4 | Та | W | Re | Операционные системы | Ir | Pt (NO 3 ) 2 Pt (NO 3 ) 4 | Au (NO 3 ) 3 | Hg 2 (NO 3 ) 2 Hg (NO 3 ) 2 | TlNO 3 Tl (NO 3 ) 3 | Pb (NO 3 ) 2 | Би (NO 3 ) 3 BiO (NO 3 ) | Po (NO 3 ) 4 | В | Rn | |
| Пт № 3 | Ра (NO 3 ) 2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ц | Og | |
| ↓ | |||||||||||||||||
| Ла (NO 3 ) 3 | Ce (NO 3 ) 3 Ce (NO 3 ) 4 | Pr (NO 3 ) 3 | Nd (NO 3 ) 3 | PM (NO 3 ) 3 | См (NO 3 ) 3 | Eu (NO 3 ) 3 | Б-г (NO 3 ) 3 | Tb (NO 3 ) 3 | Dy (NO 3 ) 3 | Хо (нет 3 ) 3 | Er (NO 3 ) 3 | Тм (№ 3 ) 3 | Yb (NO 3 ) 3 | Лу (NO 3 ) 3 | |||
| Ac (NO 3 ) 3 | Чт (NO 3 ) 4 | PaO 2 (NO 3 ) 3 | UO 2 (NO 3 ) 2 | Np (NO 3 ) 4 | Pu (NO 3 ) 4 | Am (NO 3 ) 3 | См (NO 3 ) 3 | Bk | Cf | Es | FM | Мкр | Нет | Lr | |||
См. Также [ править ]
- Аммоний
- f-соотношение
- Нитрификация
- Нитратин
- Нитрит , анион NO-
2 - Триоксид азота , нейтральный радикал NO
3 - Пероксинитрат , OONO-
2 - Нитрат натрия
Ссылки [ править ]
- ^ a b c d Лауэ В., Тиманн М., Шайблер Э., Виганд К.В. (2006). «Нитраты и нитриты». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a17_265 .
- ^ a b Hord NG, Tang Y, Bryan NS (июль 2009 г.). «Пищевые источники нитратов и нитритов: физиологический контекст потенциальной пользы для здоровья» . Американский журнал клинического питания . 90 (1): 1–10. DOI : 10,3945 / ajcn.2008.27131 . PMID 19439460 .
- ^ McMahon NF, Leveritt MD, Пейви TG (апрель 2017). «Влияние пищевых добавок с нитратами на выполнение упражнений на выносливость у здоровых взрослых: систематический обзор и метаанализ» (PDF) . Спортивная медицина (Окленд, Новая Зеландия) . 47 (4): 735–756. DOI : 10.1007 / s40279-016-0617-7 . PMID 27600147 . S2CID 207494150 .
- ^ Maughan, Ronald J (2013). Еда, питание и спортивные результаты III . Нью-Йорк: Тейлор и Фрэнсис. п. 63. ISBN 978-0-415-62792-4.
- ↑ Bingham SA, Hughes R, Cross AJ (ноябрь 2002 г.). «Влияние белого и красного мяса на эндогенное N-нитрозирование в толстой кишке человека и дальнейшее доказательство дозовой зависимости» . Журнал питания . 132 (11 доп.): 3522S – 3525S. DOI : 10.1093 / JN / 132.11.3522S . PMID 12421881 .
- ^ Партасарати DK, Bryan NS (ноябрь 2012). «Нитрит натрия:« лекарство »от недостаточности оксида азота». Мясная наука . 92 (3): 274–9. DOI : 10.1016 / j.meatsci.2012.03.001 . PMID 22464105 .
- ^ Moorcroft, M .; Дэвис, Дж .; Комптон, Р.Г. (2001). «Обнаружение и определение нитратов и нитритов: обзор». Таланта . 54 (5): 785–803. DOI : 10.1016 / S0039-9140 (01) 00323-X . PMID 18968301 .
- ^ Эллис, Грэм; Адатия, Ян; Йазданпанах, Мехрдад; Макела, Синикка К. (1998). «Анализы нитритов и нитратов: перспективы клинической биохимии». Клиническая биохимия . 31 (4): 195–220. DOI : 10.1016 / S0009-9120 (98) 00015-0 . PMID 9646943 .
- ^ Powlson, Дэвид S .; Аддискотт, Том М .; Бенджамин, Найджел; Cassman, Ken G .; Де Кок, Тео М .; Ван Гринсвен, Ханс; l'Hirondel, Жан-Луи; Эйвери, Алекс А .; Ван Кессель, Крис (2008). «Когда нитраты становятся опасными для человека?» . Журнал качества окружающей среды . 37 (2): 291–5. DOI : 10,2134 / jeq2007.0177 . PMID 18268290 .
- ^ «Нитраты и отравление нитритами: Введение» . Ветеринарное руководство Merck . Проверено 27 декабря 2008 .
- ^ Аддискотт, TM; Бенджамин, Н. (2006). «Нитраты и здоровье человека». Использование и управление почвами . 20 (2): 98–104. DOI : 10.1111 / j.1475-2743.2004.tb00344.x .
- ↑ AA Avery: Детская метгемоглобинемия - Пересмотр роли нитратов в питьевой воде , Environmental Health Perspectives , Volume 107, Number 7, July 1999.
- ^ Manassaram DM, Backer LC, Мессинг R, Fleming LE, Люк B, Monteilh CP (октябрь 2010). «Нитраты в питьевой воде и уровни метгемоглобина во время беременности: продольное исследование» . Здоровье окружающей среды . 9 (1): 60. DOI : 10,1186 / 1476-069x-9-60 . PMC 2967503 . PMID 20946657 .
- ^ "4. Каковы правила EPA для питьевой воды для нитратов?" . Грунтовые воды и питьевая вода . Проверено 13 ноября 2018 .
- ^ Багери, H .; Hajian, A .; Rezaei, M .; Ширзадмехр, А. (2017). «Композит наночастиц металла Cu - многослойные углеродные нанотрубки - восстановленный оксид графена как новая и высокоэффективная платформа электрохимического датчика для одновременного определения нитрита и нитрата». Журнал опасных материалов . 324 (Pt B): 762–772. DOI : 10.1016 / j.jhazmat.2016.11.055 . PMID 27894754 .
- Перейти ↑ Romano N, Zeng C (сентябрь 2007 г.). «Острая токсичность нитрата натрия, нитрата калия и хлорида калия и их влияние на состав гемолимфы и структуру жабр ранних молодых синих крабов-пловцов (Portunus pelagicus Linnaeus, 1758) (Decapoda, Brachyura, Portunidae)». Экологическая токсикология и химия . 26 (9): 1955–62. DOI : 10.1897 / 07-144r.1 . PMID 17705664 .
- ↑ Шарп, Ширли. «Нитраты в аквариуме» . About.com . Проверено 30 октября 2013 года .
- ↑ Romano N, Zeng C (декабрь 2007 г.). «Влияние калия на опосредованные нитратами изменения осморегуляции у морских крабов». Водная токсикология . 85 (3): 202–8. DOI : 10.1016 / j.aquatox.2007.09.004 . PMID 17942166 .
- ^ «Риск нитратов в кормовых культурах - часто задаваемые вопросы» . Сельское хозяйство и развитие сельских районов . Правительство Альберты . Проверено 30 октября 2013 года .
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме нитратов . |
- ATSDR - Примеры из практики экологической медицины - Нитраты / нитритная токсичность ( архив )