 | |
 | |
 | |
| Идентификаторы | |
|---|---|
3D модель ( JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.029.290 |
PubChem CID | |
| Номер RTECS |
|
| UNII | |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| LiNO 3 | |
| Молярная масса | 68,946 г / моль |
| Внешность | От белого до светло-желтого твердого вещества |
| Плотность | 2,38 г / см 3 |
| Температура плавления | 255 ° С (491 ° F, 528 К) |
| Точка кипения | 600 ° С (1112 ° F, 873 К) (разлагается) |
| 52,2 г / 100 мл (20 ° C) 90 г / 100 мл (28 ° C) 234 г / 100 мл (100 ° C) | |
| Растворимость | растворим в этаноле , метаноле , пиридине , аммиаке , ацетоне |
| −62,0 · 10 −6 см 3 / моль (+3 H 2 O) | |
Показатель преломления ( n D ) | 1,735 [1] |
| Термохимия | |
Теплоемкость ( C ) | 64 Дж / моль К |
Стандартная мольная энтропия ( S | 105 Дж / моль К |
Std энтальпия формации (Δ F H ⦵ 298 ) | -7,007 кДж / г или -482,3 кДж / моль |
Свободная энергия Гиббса (Δ f G ˚) | -389,5 кДж / моль |
Стандартная энтальпия сгорания (Δ c H ⦵ 298 ) | 25,5 кДж / моль |
| Опасности | |
| Основные опасности | Окислитель, раздражитель |
| NFPA 704 (огненный алмаз) |  1 0 0 OX |
| точка возгорания | Негорючий |
| Смертельная доза или концентрация (LD, LC): | |
LD 50 ( средняя доза ) | 1426 мг / кг (перорально, крыса) |
| Родственные соединения | |
Другие катионы | Нитрат натрия Нитрат калия Нитрат рубидия Нитрат цезия |
Родственные соединения | Сульфат лития Хлорид лития |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
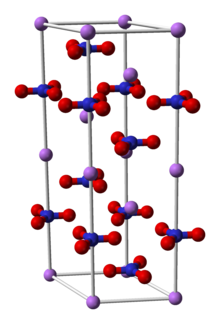
Нитрат лития - это неорганическое соединение с формулой LiNO 3 . Это лития соль из азотной кислоты (ый нитрат щелочного металла ). Соль расплывается , абсорбирует воду с образованием гидратированной формы, тригидрата нитрата лития. Его эвтектика представляет интерес для теплоносителей. [2]
Это сделано путем обработки карбоната лития или гидроксид лития с азотной кислотой .
Использует [ редактировать ]
Эта расплывающаяся бесцветная соль представляет собой окислитель, используемый при производстве красных фейерверков и ракет .
Тепловое хранение [ править ]
Гидратированные формы, лития нитрат тригидрат, имеет чрезвычайно высокую удельную теплоту плавления , 287 (± 7) Дж / г, [3] и , следовательно , может быть использован для хранения тепловой энергии при ее температуре расплава 303.3 K. [4]
Нитрат лития был предложен в качестве среды для хранения тепла, собираемого от солнца для приготовления пищи. Линзы Френеля будет использоваться для плавления твердого нитрата лития, который затем функционировать в качестве «солнечной батареи», что позволяет теплу быть перераспределены позже за счет конвекции. [5]
Синтез [ править ]
Нитрат лития можно синтезировать путем взаимодействия азотной кислоты и карбоната лития.
- Li 2 CO 3 + 2 HNO 3 → 2 LiNO 3 + H 2 O + CO 2
Обычно при образовании LiNO 3 используется индикатор pH, чтобы определить, когда вся кислота нейтрализована. Однако эту нейтрализацию можно также распознать по потере производства диоксида углерода . [6] Чтобы избавить конечный продукт от лишней воды, образец нагревают.
Токсичность [ править ]
Нитрат лития может быть токсичным для организма при приеме внутрь, поражая центральную нервную систему, щитовидную железу, почки и сердечно-сосудистую систему. [7] При контакте с кожей, глазами и слизистыми оболочками нитрат лития может вызвать раздражение этих участков. [8]
Дальнейшее чтение [ править ]
- Беркизи, Джанфранческо; Витали, Джованни; Амико, Антонио (1985). «Транспортные свойства бинарных растворов нитрата лития и нитрата кальция в расплаве ацетамида». Журнал химических и технических данных . 30 (2): 208–9. DOI : 10.1021 / je00040a023 .
- Келли, Майкл Т; Туан, Кристофер Y (2006). «Пример использования нитрата лития для остановки щелочно-кремнеземной реакции в существующем бетонном покрытии». Аэродром и тротуар . С. 625–35. DOI : 10.1061 / 40838 (191) 53 . ISBN 978-0-7844-0838-4.
- Мунис-Миранда, Франческо; Пальяи, Марко; Кардини, Джанни; Ригини, Роберто (2012). «Бифуркационная водородная связь в тригидрате нитрата лития, исследованная ab Initio Molecular Dynamics». Журнал физической химии . 116 (9): 2147–53. Bibcode : 2012JPCA..116.2147M . DOI : 10.1021 / jp2120115 . PMID 22309150 .
- Руис, Мария Л; Лик, Илеана Д; Легуисамон Апарисио, Мария С. Понци, Марта I; Родригес-Кастельон, Энрике; Понци, Эстер Н. (2012). «НЕТ ВЛИЯНИЯ на каталитическое горение сажи: нитрат лития и золотые катализаторы». Промышленные и инженерные химические исследования . 51 (3): 1150–7. DOI : 10.1021 / ie201295s .
Ссылки [ править ]
- ^ Прадёт Патнаик. Справочник неорганических химикатов . Макгроу-Хилл, 2002, ISBN 0-07-049439-8 . [ требуется страница ]
- ^ Вительманн, Ульрих и Бауэр, Ричард Дж. (2005) «Литий и литиевые соединения» в Энциклопедии промышленной химии Ульмана , Wiley-VCH: Weinheim. DOI : 10.1002 / 14356007.a15_393 .
- ^ Шамбергер, Патрик Дж; Рид, Тимоти (2012). «Теплофизические свойства тригидрата нитрата лития от (253 до 353) K». Журнал химических и технических данных . 57 (5): 1404–11. DOI : 10.1021 / je3000469 .
- ^ Кенисарин, Мурат; Махкамов, Хамид (2016). «Солевые гидраты как аккумуляторы скрытой теплоты: теплофизические свойства и стоимость». Материалы солнечной энергии и солнечные элементы . 145 (3): 255–86. DOI : 10.1016 / j.solmat.2015.10.029 .
- ^ http://barbequelovers.com/grills/a-solar-grill-prototype-for-a-greener-tomorrow [ требуется полная ссылка ]
- ^ «Синтез базы данных: синтез нитрата лития» . Сеть любительской науки . Проверено 18 июня 2012 года .
- ^ «Паспорт безопасности материала» . Каталог Sigma-Aldrich . Проверено 12 апреля 2012 года .
- ^ "Химический лист данных" . CAMEO Chemicals . Проверено 26 апреля 2012 года .
Внешние ссылки [ править ]
- База данных по опасным химическим веществам [ постоянная мертвая ссылка ]
| HNO 3 | Он | ||||||||||||||||
| LiNO 3 | Быть (NO 3 ) 2 | B (НЕТ3)- 4 | RONO 2 | НЕТ- 3 NH 4 NO 3 | HOONO 2 | FNO 3 | Ne | ||||||||||
| NaNO 3 | Mg (NO 3 ) 2 | Al (NO 3 ) 3 | Si | п | S | ClONO 2 | Ar | ||||||||||
| KNO 3 | Ca (NO 3 ) 2 | СБН (№ 3 ) 3 | Ti (NO 3 ) 4 | VO (NO 3 ) 3 | Cr (NO 3 ) 3 | Mn (NO 3 ) 2 | Fe (NO 3 ) 2 Fe (NO 3 ) 3 | Co (NO 3 ) 2 Co (NO 3 ) 3 | Ni (NO 3 ) 2 | CuNO 3 Cu (NO 3 ) 2 | Zn (NO 3 ) 2 | Ga (NO 3 ) 3 | Ge | В качестве | Se | Br | Kr |
| RbNO 3 | Sr (NO 3 ) 2 | Д (НЕТ 3 ) 3 | Zr (NO 3 ) 4 | Nb | Пн | Tc | Ru (NO 3 ) 3 | Rh (NO 3 ) 3 | Pd (NO 3 ) 2 Pd (NO 3 ) 4 | AgNO 3 Ag (NO 3 ) 2 | Cd (NO 3 ) 2 | В (NO 3 ) 3 | Sn | Сб (NO 3 ) 3 | Te | INO 3 | Xe (NO 3 ) 2 |
| CsNO 3 | Ba (NO 3 ) 2 | Hf (NO 3 ) 4 | Та | W | Re | Операционные системы | Ir | Pt (NO 3 ) 2 Pt (NO 3 ) 4 | Au (NO 3 ) 3 | Hg 2 (NO 3 ) 2 Hg (NO 3 ) 2 | TlNO 3 Tl (NO 3 ) 3 | Pb (NO 3 ) 2 | Би (NO 3 ) 3 BiO (NO 3 ) | Po (NO 3 ) 4 | В | Rn | |
| Пт № 3 | Ра (NO 3 ) 2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ц | Og | |
| ↓ | |||||||||||||||||
| Ла (NO 3 ) 3 | Ce (NO 3 ) 3 Ce (NO 3 ) 4 | Pr (NO 3 ) 3 | Nd (NO 3 ) 3 | PM (NO 3 ) 3 | См (NO 3 ) 3 | Eu (NO 3 ) 3 | Б-г (NO 3 ) 3 | Tb (NO 3 ) 3 | Dy (NO 3 ) 3 | Хо (нет 3 ) 3 | Er (NO 3 ) 3 | Тм (№ 3 ) 3 | Yb (NO 3 ) 3 | Лу (NO 3 ) 3 | |||
| Ac (NO 3 ) 3 | Чт (NO 3 ) 4 | PaO 2 (NO 3 ) 3 | UO 2 (NO 3 ) 2 | Np (NO 3 ) 4 | Pu (NO 3 ) 4 | Am (NO 3 ) 3 | См (NO 3 ) 3 | Bk | Cf | Es | FM | Мкр | Нет | Lr | |||