 | |
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Нитрат аммония | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.026.680 |
| Номер ЕС |
|
PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 0222 - с> 0,2% горючих веществ 1942 - с ≤ 0,2% горючих веществ 2067 - удобрения 2426 - жидкие |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| NH 4 NO 3 | |
| Молярная масса | 80,043 г / моль |
| Внешность | бесцветный |
| Плотность | 1,725 г / см 3 (20 ° C) |
| Температура плавления | 169,6 ° С (337,3 ° F, 442,8 К) |
| Точка кипения | ок. 210 ° С (410 ° F, 483 К) разлагается |
| Эндотермический 118 г / 100 мл (0 ° C) 150 г / 100 мл (20 ° C) 297 г / 100 мл (40 ° C) 410 г / 100 мл (60 ° C) 576 г / 100 мл (80 ° C) ) 1024 г / 100 мл (100 ° C) [1] | |
| -33,6 · 10 −6 см 3 / моль | |
| Структура | |
| тригональный | |
| Взрывоопасные данные | |
| Чувствительность к ударам | очень низкий |
| Чувствительность к трению | очень низкий |
| Скорость детонации | 2500 м / с |
| Опасности | |
| Основные опасности | Взрывчатое вещество, окислитель |
| Пиктограммы GHS | |
| Сигнальное слово GHS | Опасность |
Формулировки опасности GHS | H201 , H271 , H319 |
Меры предосторожности GHS | P220 , P221 , P271 , P280 , P264 , P372 |
| NFPA 704 (огненный алмаз) |  0 1 3 OX |
| Смертельная доза или концентрация (LD, LC): | |
LD 50 ( средняя доза ) | 2085–5300 мг / кг (перорально крысам, мышам) [2] |
| Родственные соединения | |
Другие анионы | Нитрит аммония |
Другие катионы | Нитрат натрия Нитрат калия Нитрат гидроксиламмония |
Родственные соединения | Перхлорат аммония |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
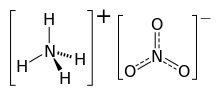
Аммиачная селитра - химическое соединение с химической формулой NH 4.НЕТ 3. Это представляет собой белое кристаллическое твердое вещество , состоящее из ионов из аммония и нитрата . Он хорошо растворяется в воде и гигроскопичен в твердом виде, хотя не образует гидратов . Он преимущественно используется в сельском хозяйстве как удобрение с высоким содержанием азота . [4] Мировое производство оценивается в 21,6 млн тонн в 2017 году. [5]
Другое его основное применение - это компонент взрывчатых смесей, используемых в горнодобывающей промышленности, разработке карьеров и гражданском строительстве. Это основной компонент ANFO , популярного промышленного взрывчатого вещества, на долю которого приходится 80% взрывчатых веществ, используемых в Северной Америке; аналогичные составы использовались в самодельных взрывных устройствах .
Многие страны постепенно отказываются от его использования в потребительских приложениях из-за опасений по поводу его возможности неправильного использования. [6] С начала 20 века в результате случайных взрывов нитрата аммония погибли тысячи людей.
Возникновение [ править ]
Нитрат аммония встречается как природный минерал гвихабаит (ранее известный как нитраммит) [7] - аммонийный аналог селитры (минералогическое название: селитра) [8] [9] - в самых засушливых регионах пустыни Атакама в Чили , часто как корка на земле или в сочетании с другими минералами нитратов, йодатов и галогенидов . Здесь раньше добывали нитрат аммония, [ когда? ], но фактически 100% химического вещества, которое сейчас используется, синтетическое.
Производство, реакции и кристаллические фазы [ править ]
Промышленное производство нитрата аммония влечет за собой кислотно-щелочную реакцию с аммиаком с азотной кислотой : [10]
- HNO 3 + NH 3 → NH 4 NO 3
Аммиак используется в безводной форме (газ), а азотная кислота - в концентрированном виде. Реакция бурная из-за ее сильно экзотермического характера. После образования раствора, обычно с концентрацией около 83%, избыток воды испаряется, чтобы оставить содержание нитрата аммония (AN) от 95% до 99,9% концентрации (расплав AN), в зависимости от марки. Затем расплав AN превращается в «гранулы» или маленькие шарики в распылительной башне или в гранулы путем распыления и переворачивания во вращающемся барабане. Гранулы или гранулы можно дополнительно высушить, охладить и затем покрыть для предотвращения слеживания. Эти гранулы или гранулы являются типичными коммерческими продуктами AN.
Аммиак, необходимый для этого процесса, получают по методу Габера из азота и водорода. Аммиак, полученный по методу Габера, может быть окислен до азотной кислоты по методу Оствальда . Другой способ производства - это вариант нитрофосфатного процесса :
- Ca (NO 3 ) 2 + 2 NH 3 + CO 2 + H 2 O → 2 NH 4 NO 3 + CaCO 3
Эти продукты, карбонат кальция и нитрат аммония, могут очищаться отдельно или продаваться вместе как нитрат кальция и аммония .
Нитрат аммония также может быть получен посредством реакций метатезиса :
- (NH 4 ) 2 SO 4 + Ba (NO 3 ) 2 → 2 NH 4 NO 3 + BaSO 4
- NH 4 Cl + AgNO 3 → NH 4 NO 3 + AgCl
Реакции [ править ]
Поскольку нитрат аммония представляет собой соль , как катион, NH 4 + , так и анион NO 3 - могут принимать участие в химических реакциях.
Твердый нитрат аммония разлагается при нагревании. При температуре ниже 300 ° C в результате разложения в основном образуются закись азота и вода:
- NH 4 NO 3 → N 2 O + 2H 2 O
При более высоких температурах преобладает следующая реакция. [11]
- 2NH 4 NO 3 → 2N 2 + O 2 + 4H 2 O
Обе реакции разложения являются экзотермическими, а их продуктами являются газы. При определенных условиях это может привести к неуправляемой реакции , в результате которой процесс разложения может стать взрывоопасным. [12] Подробности см. В § Катастрофы . Произошло много бедствий , связанных с нитратом аммония , с человеческими жертвами.
Красно-оранжевый цвет во взрывном облаке обусловлен двуокисью азота , вторичным продуктом реакции. [12]
Кристаллические фазы [ править ]
Наблюдается ряд кристаллических фаз нитрата аммония. Следующее происходит при атмосферном давлении.
Фаза Температура (° C) Симметрия (жидкость) (выше 169,6) я От 169,6 до 125,2 кубический II 125,2 к 84,2 четырехугольный III 84,2 до 32,3 α-ромбический IV От 32,3 до -16,8 β-ромбический V ниже −16,8 тетрагональный [13]
Обе формы от β-ромбической до α-ромбической потенциально присутствуют при температуре окружающей среды во многих частях мира, но имеют разницу в плотности на 3,6%. В результате этот фазовый переход и сопутствующее изменение объема с практическим следствием того, что нитрат аммония, образующийся в качестве топлива твердого ракетного двигателя, образует трещины. По этой причине был исследован стабилизированный фазой нитрат аммония (PSAN), который включает галогениды металлов в качестве стабилизаторов. [14]
Приложения [ править ]
Удобрение [ править ]
Аммиачная селитра - важное удобрение с рейтингом NPK 34-0-0 (34% азота). [15] Он менее концентрирован, чем мочевина (46-0-0), что дает нитрату аммония небольшой недостаток транспортировки. Преимущество нитрата аммония перед мочевиной состоит в том, что он более стабилен и не теряет быстро азот в атмосферу.
Взрывчатые вещества [ править ]
Нитрат аммония входит в состав некоторых взрывчатых веществ. Примеры взрывчатых веществ, содержащих нитрат аммония, включают:
- Астролит ( ракетное топливо из нитрата аммония и гидразина )
- Аматол (нитрат аммония и тротил )
- Аммонал (нитрат аммония и алюминиевый порошок)
- Аматекс (нитрат аммония, TNT и RDX )
- ANFO (нитрат аммония и мазут )
- DBX (нитрат аммония, гексоген , тротил и алюминиевый порошок)
- Товекс (нитрат аммония и нитрат метиламмония )
- Минол (взрывчатое вещество) (нитрат аммония, тротил и алюминиевый порошок)
- Гома-2 (нитрат аммония, нитрогликоль , нитроцеллюлоза , дибутилфталат и топливо )
Смесь с мазутом [ править ]
ANFO представляет собой смесь 94% нитрата аммония («AN») и 6% мазута («FO»), широко используемого в качестве массового промышленного взрывчатого вещества . [16] : 1 Он используется в угледобыче , карьерах , горнодобывающей промышленности и гражданском строительстве в нетребовательных приложениях, где преимущества низкой стоимости и простоты использования ANFO имеют большее значение, чем преимущества, предлагаемые обычными промышленными взрывчатыми веществами, такие как водонепроницаемость, кислородный баланс, высокая скорость детонации и производительность при малых диаметрах. [16] : 2
Терроризм [ править ]
Аммоний взрывчатых веществ на основе нитрата использовались в бомбежке Sterling Hall в Мэдисоне, штат Висконсин, 1970 года, взрыв в Оклахома - Сити в 1995 году, 2011 - Дели взрывы , то 2011 взрыв в Осло , и 2013 Хайдарабад бластов .
В ноябре 2009 года правительство Северо-Западной пограничной провинции (СЗПП) Пакистана ввело запрет на использование сульфата аммония, нитрата аммония и кальций-аммиачной селитры в бывшем Малакандском дивизионе, включая Верхний Дир , Нижний Дир , Сват , Читрал , и Малакандские районы СЗПП - после сообщений о том, что эти химические вещества использовались боевиками для изготовления взрывчатых веществ. Из-за этих запретов " Хлорат калия - вещество, которое делает безопасные спички"«загореться» - превзошло удобрения в качестве взрывчатого вещества, предпочитаемого повстанцами » [17].
Ниша использует [ править ]
Нитрат аммония используется в некоторых холодных компрессах быстрого приготовления , так как его растворение в воде сильно эндотермично . Он также использовался в сочетании с независимо взрывоопасным «топливом», таким как нитрат гуанидина , [18] [19] как более дешевая (но менее стабильная) альтернатива 5-аминотетразолу в надувных устройствах подушек безопасности, производимых Takata Corporation , которые были отозваны. как небезопасно после убийства 14 человек. [20]
Раствор нитрата аммония с азотной кислотой под названием Cavea-b оказался многообещающим для использования в космических кораблях в качестве более энергетической альтернативы обычному монотопливному гидразину . В 1960-х годах было проведено несколько испытаний, но это вещество не было принято НАСА.
Безопасность, обращение и хранение [ править ]
Существуют многочисленные инструкции по безопасности при хранении и обращении с нитратом аммония. Данные о здоровье и безопасности показаны в паспортах безопасности, которые можно получить у поставщиков и от различных правительств. [21] [22] [23]
Чистая нитрат аммония не горит, но как сильный окислитель поддерживает и ускоряет горение органических (и некоторых неорганических) материалов. [21] [24] [25] Не хранить рядом с горючими веществами.
Хотя нитрат аммония стабилен при температуре и давлении окружающей среды во многих условиях, он может взорваться от сильного инициирующего заряда. Его нельзя хранить рядом с взрывчатыми веществами или взрывчатыми веществами.
Расплавленный нитрат аммония очень чувствителен к ударам и детонации, особенно если он загрязняется несовместимыми материалами, такими как горючие, легковоспламеняющиеся жидкости, кислоты, хлораты, хлориды, сера, металлы, древесный уголь и опилки. [26] [21]
Контакт с некоторыми веществами, такими как хлораты , минеральные кислоты и сульфиды металлов , может привести к интенсивному или даже бурному разложению, способному воспламенить близлежащий горючий материал или взорвать. [27] [28]
Нитрат аммония начинает разлагаться после плавления с выделением NO. Икс , HNO 3 , NH3и Н 2 О . Его нельзя нагревать в замкнутом пространстве. [21] Возникающие при разложении тепло и давление повышают чувствительность к детонации и увеличивают скорость разложения. Детонация может произойти при 80 атмосфер . Загрязнение может снизить это до 20 атмосфер. [26]
Нитрат аммония имеет критическую относительную влажность 59,4%, выше которой он будет поглощать влагу из атмосферы. Поэтому важно хранить нитрат аммония в плотно закрытой таре. В противном случае он может слиться в большую твердую массу. Нитрат аммония может поглощать достаточно влаги для разжижения. Смешивание нитрата аммония с некоторыми другими удобрениями может снизить критическую относительную влажность. [29]
Возможность использования материала в качестве взрывчатого вещества побудила принять меры регулирования. Например, в Австралии в августе 2005 года вступили в силу Положения об опасных грузах, призванные обеспечить лицензирование обращения с такими веществами. [30] Лицензии предоставляются только заявителям (отрасли) с соответствующими мерами безопасности для предотвращения любого неправомерного использования. [31] Также могут быть рассмотрены дополнительные виды использования, например, в образовательных и исследовательских целях, но не для индивидуального использования. Сотрудники тех, у кого есть лицензии на работу с этим веществом, по-прежнему должны находиться под надзором уполномоченного персонала и должны пройти проверку безопасности и национальной полиции перед выдачей лицензии.
Опасности для здоровья [ править ]
Данные о здоровье и безопасности показаны в паспортах безопасности материалов , которые можно получить у поставщиков и найти в Интернете. [32]
Аммиачная селитра не опасна для здоровья и обычно используется в удобрениях. [32] [33] [34]
Нитрат аммония имеет LD 50 2217 мг / кг [35], что для сравнения составляет примерно две трети от показателя поваренной соли .
Катастрофы [ править ]
Нитрат аммония при нагревании разлагается без взрыва на газы закись азота и водяной пар . Однако его можно вызвать взрывным разложением при детонации . [36] Большие запасы материала также могут быть серьезным риском пожара из-за их поддерживающего окисления , ситуация, которая может легко перерасти в детонацию. Взрывы не редкость: в большинстве лет происходят относительно небольшие инциденты, а также произошло несколько крупных и разрушительных взрывов. Примеры включают взрыв Оппау в 1921 году (один из крупнейших искусственных неядерных взрывов ), катастрофу в Техас-Сити в 1947 году,Взрывы в Тяньцзине в 2015 году в Китае и взрыв в Бейруте в 2020 году . [37] [38]
Нитрат аммония может взорваться по двум причинам:
- Переход от удара к детонации. Заряд взрывчатого вещества внутри или при контакте с массой нитрата аммония вызывает детонацию нитрата аммония. Примерами таких бедствий являются Кривальд , Морган (современный Сейревиль, Нью-Джерси ), Оппау и Тессендерло .
- Переход от дефлаграции к детонации . Взрыв нитрата аммония возникает в результате пожара, который распространяется на нитрат аммония ( Техас-Сити, Техас ; Брест ; Уэст, Техас ; Тяньцзинь ; Бейрут ) или в результате смешивания нитрата аммония с горючим материалом во время пожара ( Репауно , Чероки, Нададорес ) . Для успешного перехода от пожара к взрыву огонь должен быть ограничен хотя бы до определенной степени.
См. Также [ править ]
- Восстановление ресурсов
Ссылки [ править ]
- ^ Прадёт Патнаик. Справочник неорганических химикатов . Макгроу-Хилл, 2002, ISBN 0-07-049439-8
- ^ Мартель, B .; Кэссиди, К. (2004). Анализ химического риска: Практическое пособие . Баттерворт-Хайнеманн. п. 362. ISBN. 1-903996-65-1.
- ^ "Архивная копия" . Архивировано из оригинала 17 февраля 2015 года . Проверено 13 марта 2015 года .CS1 maint: archived copy as title (link)
- ↑ Karl-Heinz Zapp «Ammonium Compounds» в Энциклопедии промышленной химии Ульмана 2012, Wiley-VCH, Weinheim. DOI : 10.1002 / 14356007.a02_243
- ^ "Производство аммиачной селитры по странам, 2019 - knoema.com" . Knoema . Дата обращения 14 августа 2020 .
- ^ Аммиачная селитра продается тоннами в связи с нарушением законодательства США. Архивировано 28 февраля 2018 года в Wayback Machine - The Dallas Morning News.
- ^ https://www.mindat.org/min-6983.html
- ^ https://www.mindat.org/min-2917.html
- ^ https://www.ima-mineralogy.org/Minlist.htm
- ^ «Архивная копия» (PDF) . Архивировано из оригинального (PDF) 23 января 2012 года . Проверено 11 ноября 2008 года . CS1 maint: archived copy as title (link)
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . п. 469. ISBN 978-0-08-037941-8.
- ^ a b «Химия взрыва в Бейруте» .
- ^ Чой, CS; Праск, HJ (1983). «Структура фазы V ND 4 NO 3 методом нейтронной порошковой дифракции» . Acta Crystallographica Б . 39 (4): 414–420. DOI : 10.1107 / S0108768183002669 .
- ^ Кумар, Pratim (декабрь 2019). «Достижения в методах фазовой стабилизации АН с использованием КДН и других химических соединений для получения зеленых окислителей» . Оборонные технологии . 15 (6): 949–957. DOI : 10.1016 / j.dt.2019.03.002 .
- ^ «Содержание питательных веществ в удобрениях» (PDF) . Архивировано из оригинального (PDF) 24 декабря 2012 года . Проверено 27 июня 2012 года .
- ^ a b Кук, Мелвин А. (1974). Наука о промышленных взрывчатых веществах . IRECO Chemicals. п. 1. ASIN B0000EGDJT .
- ^ Брук, Том Ванден. «Афганские производители бомб переходят на новые взрывные устройства для СВУ» . США СЕГОДНЯ .
- ^ США 5531941
- ^ Соединение подушки безопасности Спорного Takata для Лет - The New York Times
- ↑ Более дешевая подушка безопасности и дорога Такаты к смертельному кризису. - Нью-Йорк Таймс
- ^ a b c d Рекомендации по химическим веществам: безопасное хранение, обращение и обращение с нитратом аммония Агентство по охране окружающей среды США
- ^ «Хранение и обращение с нитратом аммония» (PDF) . Архивировано 4 июля 2011 года (PDF) . Проверено 22 марта 2006 года .
- ^ "Аммиачная селитра MSDS" .
- ^ Pradyot Patnaik (2002). Справочник неорганических химикатов . Макгроу-Хилл. ISBN 0-07-049439-8.
- ^ «Аммиачная селитра» . PubChem . Дата обращения 6 августа 2020 .
- ^ a b «Отчет об обновлении острова Кураганг Отчет PHA MOD1» . Orica Mining Services . 1 апреля 2012 . Дата обращения 6 августа 2020 .
- ^ «Сделки химической инженерии» (PDF) . Архивировано из оригинального (PDF) 14 апреля 2016 года.
- ^ "Нитрат аммония" . webwiser.nlm.nih.gov . Дата обращения 6 августа 2020 .
- ^ Удобрения Европа (2006). «Руководство по совместимости материалов для смешивания удобрений» (PDF) .
- ^ «Правила перевозки опасных грузов (HCDG)» (PDF) .
- ^ Нитрат аммония - Регулирование его использования, балансировка доступа и защиты от "Worksafe Victoria" . Архивировано из оригинального 11 -го марта 2011 года.
- ^ a b CF Industries. «MSDS аммиачной селитры» (PDF) . Архивировано из оригинального (PDF) 27 марта 2014 года.
- ^ "Chemicalland21 - Нитрат аммония" . Архивировано из оригинального 10 января 2012 года.
- ^ "Нитрат аммония". Paton Fertilizers Pty Ltd. 2005.
- ^ "Паспорт безопасности материала, MSDS нитрата аммония" .
- ^ Чатурведи, Шалини; Дэйв, Прагнеш Н. (январь 2013 г.). «Обзор термического разложения нитрата аммония». Журнал энергетических материалов . 31 (1): 1-26. DOI : 10.1080 / 07370652.2011.573523 . S2CID 94427830 .
- ^ «Президент Ливана требует двухнедельного чрезвычайного положения в Бейруте после взрыва» . Рейтер . Бейрут. 4 августа 2020 . Дата обращения 4 августа 2020 .
Аун в комментариях, опубликованных в Twitter-аккаунте президентства, сказал, что «неприемлемо», что 2750 тонн аммиачной селитры хранились на складе в течение шести лет без мер безопасности, и пообещал, что виновные понесут «самые суровые наказания».
- ^ Урбина, Ян (2020). «За взрывом в Бейруте: опасности брошенных кораблей и грузов» . Хроники Сан-Франциско .
Источники [ править ]
- Свойства: ЮНИДО и Международный центр разработки удобрений (1998), Руководство по удобрениям , Kluwer Academic Publishers, ISBN 0-7923-5032-4 .
Внешние ссылки [ править ]
- Международная карта химической безопасности 0216
- "Хранение и обращение с нитратом аммония" , Исполнительная публикация по вопросам здравоохранения и безопасности Соединенного Королевства INDG230 (1986)
- Консультации по химическим веществам: безопасное хранение, обращение и обращение с нитратом аммония Агентство по охране окружающей среды США
- Калькуляторы: поверхностное натяжение , плотность, молярность и моляльность водного раствора нитрата аммония.
| HNO 3 | Он | ||||||||||||||||
| LiNO 3 | Быть (NO 3 ) 2 | B (НЕТ3)- 4 | RONO 2 | НЕТ- 3 NH 4 NO 3 | HOONO 2 | FNO 3 | Ne | ||||||||||
| NaNO 3 | Mg (NO 3 ) 2 | Al (NO 3 ) 3 | Si | п | S | ClONO 2 | Ar | ||||||||||
| KNO 3 | Ca (NO 3 ) 2 | СБН (№ 3 ) 3 | Ti (NO 3 ) 4 | VO (NO 3 ) 3 | Cr (NO 3 ) 3 | Mn (NO 3 ) 2 | Fe (NO 3 ) 2 Fe (NO 3 ) 3 | Co (NO 3 ) 2 Co (NO 3 ) 3 | Ni (NO 3 ) 2 | CuNO 3 Cu (NO 3 ) 2 | Zn (NO 3 ) 2 | Ga (NO 3 ) 3 | Ge | В качестве | Se | Br | Kr |
| RbNO 3 | Sr (NO 3 ) 2 | Д (НЕТ 3 ) 3 | Zr (NO 3 ) 4 | Nb | Пн | Tc | Ru (NO 3 ) 3 | Rh (NO 3 ) 3 | Pd (NO 3 ) 2 Pd (NO 3 ) 4 | AgNO 3 Ag (NO 3 ) 2 | Cd (NO 3 ) 2 | В (NO 3 ) 3 | Sn | Сб (NO 3 ) 3 | Te | INO 3 | Xe (NO 3 ) 2 |
| CsNO 3 | Ba (NO 3 ) 2 | Hf (NO 3 ) 4 | Та | W | Re | Операционные системы | Ir | Pt (NO 3 ) 2 Pt (NO 3 ) 4 | Au (NO 3 ) 3 | Hg 2 (NO 3 ) 2 Hg (NO 3 ) 2 | TlNO 3 Tl (NO 3 ) 3 | Pb (NO 3 ) 2 | Би (NO 3 ) 3 BiO (NO 3 ) | Po (NO 3 ) 4 | В | Rn | |
| Пт № 3 | Ра (NO 3 ) 2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ц | Og | |
| ↓ | |||||||||||||||||
| Ла (NO 3 ) 3 | Ce (NO 3 ) 3 Ce (NO 3 ) 4 | Pr (NO 3 ) 3 | Nd (NO 3 ) 3 | PM (NO 3 ) 3 | См (NO 3 ) 3 | Eu (NO 3 ) 3 | Б-г (NO 3 ) 3 | Tb (NO 3 ) 3 | Dy (NO 3 ) 3 | Хо (нет 3 ) 3 | Er (NO 3 ) 3 | Тм (№ 3 ) 3 | Yb (NO 3 ) 3 | Лу (NO 3 ) 3 | |||
| Ac (NO 3 ) 3 | Чт (NO 3 ) 4 | PaO 2 (NO 3 ) 3 | UO 2 (NO 3 ) 2 | Np (NO 3 ) 4 | Pu (NO 3 ) 4 | Am (NO 3 ) 3 | См (NO 3 ) 3 | Bk | Cf | Es | FM | Мкр | Нет | Lr | |||