Окиси амина , также известные как амино- N - оксид и N - оксид , представляет собой химическое соединение , которое содержит функциональную группу , R 3 N + -O - , N-O координаты ковалентной связи с три дополнительными водородом и / или углеводородом стороны цепочки, присоединенные к N. Иногда это записывается как R 3 N → O или, ошибочно, как R 3 N = O.
В строгом смысле термин оксид амина применяется только к оксидам третичных аминов . Иногда его также используют для аналогичных производных первичных и вторичных аминов.
Примеры аминооксидов включают пиридин- N- оксид , водорастворимое кристаллическое твердое вещество с температурой плавления 62–67 ° C, и N- метилморфолин N- оксид , который является окислителем.
Приложения [ править ]
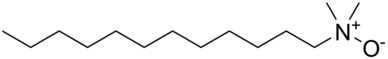
Оксиды аминов - это поверхностно-активные вещества, обычно используемые в потребительских товарах, таких как шампуни, кондиционеры, моющие средства и чистящие средства для твердых поверхностей. [1] Оксид алкилдиметиламина (длина цепи C10 – C16) является наиболее коммерчески используемым оксидом амина. [2] Они считаются классом соединений с большим объемом производства более чем в одной стране-члене Организации экономического сотрудничества и развития (ОЭСР) ; с годовым объемом производства более 26 000, 16 000 и 6 800 метрических тонн в США, Европе и Японии соответственно. [1] В Северной Америке более 95% оксидов аминов используется в бытовых чистящих средствах. [3]Они служат стабилизаторами, загустителями, смягчающими веществами, эмульгаторами и кондиционерами с активными концентрациями в диапазоне 0,1–10%. [1] Остальная часть (<5%) используется в продуктах личной гигиены, учреждениях, коммерческих продуктах [4] и для уникальных запатентованных применений, таких как фотография. [1]
Свойства [ править ]
Оксиды аминов используются в качестве защитных групп для аминов и в качестве промежуточных химических продуктов. Оксиды алкиламинов с длинной цепью используются в качестве амфотерных поверхностно-активных веществ и стабилизаторов пены .
Оксиды аминов представляют собой высокополярные молекулы и имеют полярность, близкую к полярности солей четвертичного аммония . Небольшие оксиды аминов очень гидрофильные и имеют отличную воду растворимость и очень плохую растворимость в большинстве органических растворителей .
Оксиды аминов представляют собой слабые основания с p K b около 4,5, которые образуют R 3 N + -OH, катионные гидроксиламины , при протонировании при pH ниже их p K b .
Синтез [ править ]
Почти все оксиды аминов получают окислением либо третичных алифатических аминов, либо ароматических N-гетероциклов. Перекись водорода является наиболее распространенным реагентом как в промышленности, так и в академических кругах, однако перкислоты также важны. [5] Более специализированные окислители могут найти применение нишу, например , кислота Каро или m CPBA . Спонтанные или каталитические реакции с использованием молекулярного кислорода редки. Некоторые другие реакции также будут давать оксиды аминов, такие как элиминирование ретро-Коупа , однако они используются редко.
Реакции [ править ]
Окиси аминов вступают в разные реакции. [6]
- Пиролитическое устранение. Оксиды аминов при нагревании до 150–200 ° C удаляют гидроксиламин, в результате чего образуется алкен . Эта реакция пиролитического синтеза известна под названием реакция Копа . Механизм аналогичен устранению Хофмана .
- Восстановление до аминов. Оксиды амина легко превращаются в исходный амин с помощью обычных восстанавливающих реагентов, включая алюмогидрид лития , боргидрид натрия , каталитическое восстановление , цинк / уксусную кислоту и железо / уксусную кислоту. Пиридин N -оксиды могут быть дезоксигенированы оксихлоридом фосфора.
- Жертвенный катализ. Окислители могут быть восстановлены путем восстановления N - оксиды, как и в случае регенерации осмия с помощью N - метилморфолин N - оксида.
- О- алкилирование. Пиридин N- оксиды реагируют с алкилгалогенидами с образованием O- алкилированного продукта.
- Обсуждается, что производные бис-тер-пиридина, адсорбированные на поверхности серебра, реагируют с кислородом с образованием бис-тер-пиридин- N- оксида. За этой реакцией можно проследить видео- сканирующую туннельную микроскопию с субмолекулярным разрешением. [7]
- В перегруппировке Мейзенгеймера (после Якоба Мейзенгеймера ) некоторые N- оксиды R 1 R 2 R 3 N + O - перегруппировываются в гидроксиламины R 2 R 3 N − O − R 1 [8] [9]
- в 1,2-перегруппировке:
- или 2,3-перегруппировка:
- В реакции Полоновского третичный N- оксид расщепляется ангидридом уксусной кислоты до соответствующих ацетамида и альдегида : [10] [11] [12]
Метаболиты [ править ]
Окиси аминов являются обычными метаболитами лекарств и психоактивных веществ . Примеры включают никотин , золмитриптан и морфин .
Окиси аминов противораковых лекарств были разработаны как пролекарства , которые метаболизируются в дефицитной по кислороду раковой ткани до активного лекарства.
Безопасность человека [ править ]
Окиси аминов (АО) не являются канцерогенными, кожными сенсибилизаторами или вызывают репродуктивную токсичность. Они легко метаболизируются и выводятся из организма при приеме внутрь. При хроническом проглатывании кроликами наблюдались снижение массы тела, диарея и помутнение хрусталика при самых низких наблюдаемых уровнях побочных эффектов (LOAEL) в диапазоне 87–150 мг АО / кВт мт / день. Тесты на воздействие на кожу человека показали, что через 8 часов в организм всасывается менее 1%. Раздражение глаз из-за оксидов аминов и других поверхностно-активных веществ является умеренным и временным, без длительного воздействия. [1]
Экологическая безопасность [ править ]
Аминоксиды со средней длиной цепи , равной 12,6, были измерены , чтобы быть водорастворимыми при ~ 410 г L -1 . Считается, что они обладают низким потенциалом биоаккумуляции у водных видов на основании данных log Kow для цепей с длиной цепи менее C14 (коэффициент биоконцентрации <87%). [1] были найдены Уровни AO в необработанной втекающий быть 2.3-27.8 мкг л -1 , в то время как сточные воды , они были признаны 0.4-2.91 мкг л -1 . Самые высокие концентрации стоков были обнаружены в окислительной канаве и очистных сооружениях капельного фильтра. В среднем при вторичной обработке активным илом удаляется более 96%. [2] Острая токсичность для рыб, по данным 96-часового анализа LC50, находится в диапазоне 1000–3000 мкг л.-1 для углеродной цепи с длиной меньше C14. Значения LC50 для цепи длиной более диапазоне С14 от 600 до 1400 мкг L -1 . Данные о хронической токсичности для рыб составляют 420 мкг / л. Когда нормирована на C12.9, КНЭ составляет 310 мкг л -1 для роста и выводимости. [2]
См. Также [ править ]
- Функциональная группа
- Амин , NR 3
- Гидроксиламин , NR 2 OH
- Оксид фосфина , PR 3 = O
- Сульфоксид , R 2 S = O
- Азокси , RN = N + (O - ) R RN = N + RO -
- Аминоксильная группа. Радикалы с общей структурой R 2 N – O •
- Категория: аминооксиды , содержащие все статьи о конкретных аминооксидных соединениях
Ссылки [ править ]
- ^ a b c d e f Организация экономического сотрудничества и развития (ОЭСР) (2006 г.). «Окиси аминов» . База данных по существующим химическим веществам ОЭСР . Архивировано из оригинального 22 февраля 2014 года.
- ^ а б в Сандерсон, H; C Tibazarwa; В. Греггс; DJ Versteeg (2009). «Химические оксиды аминов в больших объемах производства [C 8 –C 20 ]». Анализ рисков . 29 (6): 857–867. DOI : 10.1111 / j.1539-6924.2009.01208.x . PMID 19504658 .
- ^ Модлер, РФ; Иногучи Y (2004). «Отчет о маркетинговых исследованиях CEH: поверхностно-активные вещества, бытовые моющие средства и их сырье» . Справочник по химической экономике . Менло-Парк, Калифорния: SRI Consulting.
- ^ Сандерсон, H; Считает JL; Стэнтон К; Седлак Р (2006). «Воздействие и расстановка приоритетов - данные и методы скрининга людей для химикатов большого объема в потребительских товарах: тематическое исследование аминовых оксидов». Анализ рисков . 26 (6): 1637–1657. DOI : 10.1111 / j.1539-6924.2006.00829.x . PMID 17184403 .
- ^ Смит, Майкл Б .; Марч, Джерри (2007), Расширенная органическая химия: реакции, механизмы и структура (6-е изд.), Нью-Йорк: Wiley-Interscience, стр. 1779, ISBN 978-0-471-72091-1
- ^ Альбини, Анджело (1993). «Синтетическое применение N- оксидов амина ». Синтез . 1993 (3): 263–77. DOI : 10,1055 / с-1993-25843 .
- ^ Вальдманн, Т .; и другие. (2012). «Окисление органического адсорбента: взгляд с высоты птичьего полета». Журнал Американского химического общества . 134 (21): 8817–22. DOI : 10.1021 / ja302593v . PMID 22571820 .
- ^ J. Meisenheimer, Бер. 52. 1667 (1919)
- ^ Мартовская продвинутая органическая химия: реакции, механизмы и структура Майкл Б. Смит, Джерри Марч Wiley-Interscience, 5-е издание, 2001, ISBN 0-471-58589-0
- ^ Грирсон, D (1990). «Реакция Полоновского». Орг. Реагировать. 39 : 85. DOI : 10.1002 / 0471264180.or039.02 . ISBN 0471264180.
- ^ М. Полоновски, М. Полоновски, Bull. Soc. Чим. Франция 41, 1190 ( 1927 ).
- ^ Стратегическое применение названных реакций в органическом синтезе (в мягкой обложке) Ласло Кюрти, Барбара Чако ISBN 0-12-429785-4 .
Внешние ссылки [ править ]
- Химия аминоксидов
- Поверхностно-активные вещества, типы и использование (pdf)
- Домашняя страница аминоксидов
- Номенклатура соединений азота
- Определение ИЮПАК
