Перейти к навигации Перейти к поиску
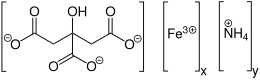 Структура цитрата железа (аммония) | |
 Кристаллическая структура (NH 4 ) 5 [Fe (C 6 H 4 O 7 ) 2 ] · 2H 2 O [1] | |
| Имена | |
|---|---|
| Название ИЮПАК 2-гидроксипропан-1,2,3-трикарбоксилат, аммонийная соль железа (3+) | |
| Другие имена Цитрат железа и аммония Цитрат железа (III) аммония Цитрат железа аммония Цитрат аммония железа FerriSeltz | |
| Идентификаторы | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ECHA InfoCard | 100.013.351 |
| Номер ЕС |
|
| Номер E | E381 (антиоксиданты, ...) |
| КЕГГ | |
PubChem CID | |
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| Характеристики | |
| C 6 H 8 O 7 ⋅ x Fe 3+ ⋅ y NH 3 | |
| Внешность | желтые кристаллы |
| Фармакология | |
| V08CA07 ( ВОЗ ) | |
| Опасности | |
| Паспорт безопасности | [1] |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Цитрат аммония и железа имеет формулу (NH 4 ) 5 [Fe (C 6 H 4 O 7 ) 2 ]. Отличительной особенностью этого соединения является то, что оно хорошо растворяется в воде, в отличие от цитрата железа, который не очень растворим.
В своей кристаллической структуре каждый фрагмент из лимонной кислоты потерял четыре протона. Депротонированная гидроксильная группа и две карбоксилатные группы связываются с центром трехвалентного железа, в то время как третья карбоксилатная группа координируется с аммонием. [1]
Использует [ редактировать ]
Цитрат аммония и железа имеет ряд применений, в том числе:
- В качестве пищевого ингредиента он имеет номер INS и используется в качестве регулятора кислотности [ необходима цитата ] . Наиболее часто используется в шотландском напитке Irn-Bru .
- Очистка воды.
- Как восстановитель солей металлов с низкой активностью, таких как золото и серебро .
- С феррицианидом калия как часть процесса фотографирования цианотипа .
- Используется в железных глубинах Клиглера для определения выработки сероводорода в микробном метаболизме.
- В медицинской визуализации в качестве контрастного вещества используется цитрат аммония и железа .
- Как гематиновый . [3]
См. Также [ править ]
- Пищевая добавка
- Список пищевых добавок
Ссылки [ править ]
- ^ a b Мацапетакис, М .; Raptopoulou, CP; Tsohos, A .; Papaefthymiou, V .; Moon, N .; Салифоглу, А. (1998). «Синтез, спектроскопические и структурные характеристики первого одноядерного водорастворимого комплекса железо-цитрат, (NH 4 ) 5 Fe (C 6 H 4 O 7 ) 2 · 2H 2 O». Варенье. Chem. Soc . 120 (50): 13266–13267. DOI : 10.1021 / ja9807035 .
- ^ «КЕГГ НАРКОТИК: Цитрат аммония железа» .
- ^ Budavari, Сьюзен, изд. (2001), The Merck Index: Encyclopedia of Chemicals, Drugs, and Biologicals (13-е изд.), Merck, ISBN 0911910131