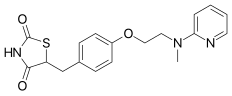
Росиглитазон
 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Avandia |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a699023 |
| Данные лицензии |
|
| Категория беременности |
|
| Пути администрирования | Устно |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетические данные | |
| Биодоступность | 99% |
| Связывание с белками | 99,8% |
| Метаболизм | Печень ( опосредованная CYP2C8 ) |
| Ликвидация Период полураспада | 3–4 часа |
| Экскреция | Почки (64%) и кал (23%) |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Лиганд PDB | |
| Панель управления CompTox ( EPA ) | |
| ECHA InfoCard | 100.108.114 |
| Химические и физические данные | |
| Формула | C 18 H 19 N 3 O 3 S |
| Молярная масса | 357,43 г · моль -1 |
| 3D модель ( JSmol ) | |
| Хиральность | Рацемическая смесь |
| Температура плавления | От 122 до 123 ° C (от 252 до 253 ° F) |
| |
| |
| | |
Розиглитазон (торговое название Avandia ) был противодиабетическим препаратом из класса тиазолидиндионов . Он действует как сенсибилизатор инсулина , связываясь с PPAR в жировых клетках и делая клетки более чувствительными к инсулину. Он продавался фармацевтической компанией GlaxoSmithKline (GSK) как самостоятельный препарат или для использования в комбинации с метформином или глимепиридом . Впервые выпущенный в 1999 году, годовой объем продаж достиг пика примерно в 2,5 миллиарда долларов в 2006 году; однако, после метаанализа в 2007 году, который связал употребление наркотиков с повышенным риском сердечного приступа , [1]В 2012 году продажи упали до 9,5 миллионов долларов. Срок действия патента на препарат истек в 2012 году [2].
Он был запатентован в 1987 году и одобрен для медицинского применения в 1999 году. [3] Несмотря на эффективность розиглитазона в снижении уровня сахара в крови при сахарном диабете 2 типа , его использование резко сократилось, поскольку исследования показали очевидную связь с повышенным риском сердечных приступов и смерти. [4] Побочные эффекты, предположительно вызванные розиглитазоном, стали предметом более 13 000 исков против GSK; [5] По состоянию на июль 2010 года GSK согласилась урегулировать более 11 500 таких исков.
Некоторые обозреватели рекомендовали исключить розиглитазон с рынка, но группа FDA не согласилась с этим, и он остается доступным в США. [6] С ноября 2011 года по ноябрь 2013 года федеральное правительство не разрешало продавать Avandia без рецепта сертифицированного врача. ; кроме того, пациенты должны были быть проинформированы о рисках, связанных с его использованием, и лекарство необходимо было покупать по почте через определенные аптеки. [7] В 2013 году FDA сняло ранее применявшиеся ограничения на розиглитазон после рассмотрения результатов исследования 2009 года, которое не продемонстрировало повышенного риска сердечного приступа. [8] [9]
В Европе Европейское агентство по лекарственным средствам (EMA) в сентябре 2010 г. рекомендовало приостановить прием препарата, поскольку польза от него больше не перевешивает риски. [10] [11] Он был снят с рынка в Великобритании, Испании и Индии в 2010 году, [12] и в Новой Зеландии и Южной Африке в 2011 году. [13]
Медицинское использование
Розиглитазон был одобрен для контроля гликемии у людей с диабетом 2 типа , что было измерено по гликированному гемоглобину A1c (HbA1c) в качестве суррогатной конечной точки, как и у других пероральных противодиабетических препаратов. [14] [15] Споры по поводу побочных эффектов резко сократили использование розиглитазона. [16]
Опубликованные исследования не предоставили доказательств того, что розиглитазон положительно влияет на такие исходы, как смертность, заболеваемость, побочные эффекты, затраты и качество жизни, связанное со здоровьем. [14]
Побочные эффекты
Сердечная недостаточность
Одной из проблем безопасности, выявленных перед утверждением, была задержка жидкости. Более того, комбинация розиглитазона с инсулином приводила к более высокому уровню застойной сердечной недостаточности. В Европе были противопоказания к применению при сердечной недостаточности и комбинации с инсулином. [17]
Мета-анализ всех исследований 2010 и 2019 годов подтвердил более высокий риск сердечной недостаточности и двойной риск, когда розиглитазон вводился в качестве дополнительной терапии к инсулину. [18] [19] Два метаанализа реальных когортных исследований показали более высокий риск сердечной недостаточности по сравнению с пиоглитазоном. [4] [20] На каждые 100 000 пациентов, получавших розиглитазон, а не пиоглитазон, приходилось 649 случаев сердечной недостаточности.
Сердечные приступы
Относительный риск ишемических сердечных событий, наблюдаемый в испытаниях розиглитазона до утверждения, был аналогичен таковому у сопоставимых препаратов, но был повышен уровень холестерина ЛПНП, соотношение холестерина ЛПНП / ЛПВП, триглицеридов и веса. [21] [22]
В 2005 году по настоянию Всемирной организации здравоохранения GSK провела метаанализ всех 37 исследований, связанных с использованием розиглитазона, и обнаружила, что коэффициент риска составляет 1,29 (от 0,99 до 1,89). В 2006 году GSK обновил анализ, который теперь включает 42 испытания и показывает коэффициент риска 1,31 (от 1,01 до 1,70). Большое обсервационное исследование, сравнивающее пациентов, получавших розиглитизон, с пациентами, получавшими другие методы лечения диабета, было проведено в то же время и обнаружило относительный риск 0,93 (95% ДИ 0,8–1,1) для пациентов, получавших розиглитазон. Информация была передана в FDA и размещена на веб-сайте компании, но не опубликована иным образом. GSK предоставила эти анализы в FDA, но ни компания, ни FDA не предупредили врачей и пациентов об опасности. [23]Согласно FDA, Агентство не выпускало бюллетень по безопасности, потому что результаты метаанализа противоречили результатам наблюдательного исследования и результатам исследования ADOPT. [24]
Мета-анализ в мае 2007 года сообщили об использовании росиглитазона ассоциировался с 1,4 раза повышенный риск сердечного приступа и численно выше (но не значительное) увеличение риска смерти от всех сердечно - сосудистых заболеваний , против контроля. Он содержал 42 исследования, 27 из которых не были опубликованы. [1] Другой мета-анализ 4 испытаний с последующим наблюдением более 1 года показал аналогичные результаты. [25] Метаанализ Ниссена подвергся критике в статье Джорджа Даймонда и др. В 2007 году . в Анналах внутренней медицины. Авторы пришли к выводу, что из анализа Ниссенса были исключены испытания с важными данными о сердечно-сосудистом профиле розиглитазона, были необоснованно объединены испытания с сильно различающимся дизайном и были необоснованно исключены испытания без сердечно-сосудистых событий. Авторы пришли к выводу, что нельзя сделать однозначного вывода относительно того, увеличивает или снижает риск сердечно-сосудистых заболеваний розиглитазон. [26] Исследователи из Кокрановского сотрудничества.опубликовали собственный метаанализ использования розиглитазона при диабете II типа, сделав вывод, что не было достаточных доказательств, подтверждающих какую-либо пользу для здоровья от розиглитазона. Отмечая недавнюю публикацию Ниссена, они повторили свой мета-анализ, включив только испытания, включенные в исследование Ниссена, которые касались диабетиков II типа. (Исследование Nissen включало некоторые испытания на людях с другими расстройствами.) Они не обнаружили статистически значимого увеличения сердечно-сосудистых событий, но отметили, что все проанализированные ими сердечно-сосудистые конечные точки показали незначительную тенденцию к худшим результатам в группах розиглитазона. [27]
В июле 2007 года FDA провело совместное заседание Консультативного комитета по эндокринологическим и метаболическим препаратам и Консультативного комитета по безопасности лекарственных средств и управлению рисками. Ученый FDA Джой Меле представила метаанализ, изучающий сердечно-сосудистый риск розиглитазона в завершенных клинических испытаниях. Исследование показало, что в целом риск сердечно-сосудистых ишемических событий увеличился в 1,4 раза по сравнению с контрольной группой. Результаты были неоднородными, с четкими доказательствами повышенного риска по сравнению с плацебо, но не по сравнению с другими видами лечения диабета, и более высокого риска, связанного с комбинациями розиглитазона с инсулином или метформином. [28]Основываясь на увеличении риска в 1,4 раза по сравнению с контрольными группами, ученый FDA Дэвид Грэм представил анализ, предполагающий, что розиглитазон вызвал 83 000 дополнительных сердечных приступов в период с 1999 по 2007 гг. [29] : 4 [30] Консультативная группа проголосовала 20: 3 за то, что Имеющиеся данные показали, что розиглитазон увеличивает риск сердечно-сосудистых событий и 22: 1, что общее соотношение риск / польза от розиглитазона оправдывает его дальнейший маркетинг в Соединенных Штатах. FDA наложило ограничения на препарат, в том числе добавило предупреждение о сердечных приступах, но не отменило его. [31]
В 2000 году Европейское агентство по лекарственным средствам (EMA) запросило исследование, направленное на решение проблем, связанных с безопасностью сердечно-сосудистой системы . GSK согласилась провести постмаркетинговое исследование долгосрочной сердечно-сосудистой заболеваемости / смертности у пациентов, принимающих розиглитазон в сочетании с сульфонилмочевиной или метформином: исследование RECORD. Результаты, опубликованные в 2009 году, показали, что розиглитазон не уступает лечению метформином или сульфонилмочевиной в отношении частоты сердечно-сосудистых событий и смертности от сердечно-сосудистых заболеваний. Европейские регулирующие органы пришли к выводу, что отчасти из-за ограничений конструкции, результаты не подтверждают и не устраняют опасения чрезмерного сердечно-сосудистого риска. [17]
В феврале 2010 года заместитель директора FDA по безопасности лекарственных средств рекомендовал снять розиглитазон с рынка. В июне 2010 года они опубликовали ретроспективное исследование, в котором сравнивали розиглитазон с пиоглитазоном, другим тиазолидиндионом, продаваемым в Соединенных Штатах, и пришли к выводу, что розиглитазон связан с «повышенным риском инсульта, сердечной недостаточности и общей смертности, а также повышенным риском комбинированного препарата. ОИМ, инсульта, сердечной недостаточности или общей смертности у пациентов 65 лет и старше ». [32] число , необходимое для вреда с roziglitazone было шестьдесят. Грэм утверждал, что розиглитазон вызывает на 500 сердечных приступов больше и на 300 сердечных приступов больше, чем его основной конкурент.
Два метаанализа, выпущенные в 2010 году, один из которых включает 56 испытаний, а второй - 164, пришли к противоречивым выводам. Nissen et al. снова обнаружили повышенный риск инфаркта сердца по сравнению с контролем, но не увеличили риск смерти от сердечно-сосудистых заболеваний. [33] Mannucci et al. не обнаружили статистически значимого увеличения сердечных событий, но значительно увеличили сердечную недостаточность. [34] Обзор класса лекарств 2011 года выявил повышенный риск сердечно-сосудистых побочных эффектов. [35]
В метаанализе 16 обсервационных исследований, опубликованных в марте 2011 года, розиглитазон сравнивался с пиоглитазоном, что свидетельствует о большей безопасности пиоглитазона для сердечно-сосудистой системы. В метаанализе приняли участие 810 000 пациентов, принимавших розиглитазон или пиоглитазон . Исследование предполагает 170 избыточных инфарктов миокарда, 649 избыточных случаев сердечной недостаточности и 431 избыточную смерть на каждые 100 000 пациентов, которые получали розиглитазон, а не пиоглитазон. [20] [36] Это было подтверждено другим метаанализом с участием 945 286 пациентов в 8 ретроспективных когортных исследованиях, большинство из которых в США. [4]
В 2012 году Министерство юстиции США объявило, что GlaxoSmithKline согласился признать себя виновным и выплатить штраф в размере 3 миллиардов долларов, в частности, за утаивание результатов двух исследований сердечно-сосудистой безопасности Avandia в период с 2001 по 2007 год [37].
Смерть
В метаанализе 4 испытаний с контролем не было различий по всем причинам и смерти от сосудов. [35] [25] Два метаанализа когортных исследований выявили повышенную смертность от пиоглитазона. [4] [20]
Инсульт
Ретроспективное обсервационное исследование, проведенное с использованием данных Medicare, показало, что пациенты, получавшие розиглитазон, имели на 27% более высокий риск инсульта по сравнению с пациентами, получавшими пиоглитазон. [38]
Переломы костей
GlaxoSmithKline сообщил о более высокой частоте переломов предплечий, кистей и стоп у женщин с диабетом, получавших розиглитазон, по сравнению с теми, кто получал метформин или глибурид . [39] Информация основана на данных исследования ADOPT [40] Такое же увеличение было обнаружено с пиоглитазоном (Actos), другим тиазолидиндионом .
Мета-анализ 10 РКИ с участием 13 715 пациентов, в том числе пациентов, получавших как розиглитазон, так и пиоглитазон, показал в целом 45% повышение риска переломов при использовании тиазолидона по сравнению с плацебо или активным препаратом сравнения. Это вдвое увеличило риск переломов среди женщин с диабетом 2 типа без значительного увеличения риска переломов среди мужчин с диабетом 2 типа. [41]
Гипогликемия
Риск гипогликемии снижается при применении тиазолидиндионов по сравнению с сульфонилмочевиной ; риск аналогичен риску при применении метформина (высокая степень доказательности). [35]
Увеличение веса
Оба тиазолидиндиона вызывают прибавку в весе в той же степени, что и при приеме сульфонилмочевины (умеренная сила доказательств). [35]
Повреждение глаз
Предполагается, что розиглитазон и пиоглитазон вызывают отек желтого пятна , который повреждает сетчатку глаза и вызывает частичную слепоту. Слепота также является возможным следствием диабета, для лечения которого предназначен росиглитазон. В одном отчете [42] задокументировано несколько случаев и рекомендовано прекратить прием при первых признаках проблем со зрением. Ретроспективное когортное исследование показало связь между использованием тиазолидиндионов и частотой диабетического макулярного отека (DME). Оба применения были связаны с повышением риска в 2,3 раза через 1 год и через 10 лет наблюдения, увеличиваясь до 3, если они были связаны с инсулином. [35]
Гепатотоксичность
У нескольких взрослых, принимавших препарат в рекомендованной дозе в течение двух-четырех недель, развился острый гепатит от умеренной до тяжелой степени. Концентрация розиглитазона в плазме может быть увеличена у людей с существующими проблемами с печенью. [43]
Противопоказания
И розиглитазон, и пиоглитазон противопоказаны людям с сердечной недостаточностью III и IV класса по NYHA . Их не рекомендуется использовать при сердечной недостаточности. [44]
В Европе розиглитазон противопоказан при сердечной недостаточности или сердечной недостаточности в анамнезе на всех стадиях NYHA, для комбинированного применения с инсулином и при остром коронарном синдроме. [17] 23 сентября 2010 г. Европейское агентство по лекарственным средствам рекомендовало приостановить продажу Avandia на европейском рынке. [10] [11]
Фармакология
Розиглитазон относится к классу препаратов тиазолидиндиона. Тиазолидиндионы действуют как сенсибилизаторы инсулина. Они снижают концентрацию глюкозы, жирных кислот и инсулина в крови. Они работают путем связывания с рецепторами, активируемыми пролифератором пероксисом (PPAR). PPAR представляют собой факторы транскрипции, которые находятся в ядре и активируются лигандами, такими как тиазолидиндионы. Тиазолидиндионы проникают в клетку, связываются с ядерными рецепторами и изменяют экспрессию генов. Несколько PPAR включают PPARα, PPARβ / δ и PPARγ. Тиазолидиндионы связываются с PPARγ .
PPAR экспрессируются в жировых клетках, клетках печени, мышц, сердца, внутренней стенки (эндотелия) и гладких мышцах кровеносных сосудов. PPARγ экспрессируется в основном в жировой ткани, где он регулирует гены, участвующие в дифференцировке жировых клеток (адипоцитов), поглощении и хранении жирных кислот и поглощении глюкозы. Он также обнаружен в бета-клетках поджелудочной железы, эндотелии сосудов и макрофагах [45]. Розиглитазон является селективным лигандом PPARγ и не обладает связывающим действием с PPARα. Другие препараты связываются с PPARα.
Росиглитазон также обладает противовоспалительным действием в дополнение к его влиянию на инсулинорезистентность . Ядерный фактор каппа-B ( NF-κB ), сигнальная молекула, стимулирует воспалительные пути. Ингибитор NF-κB (IκB) подавляет воспалительные пути. Когда пациенты принимают розиглитазон, уровни NF-κB падают, а уровни IκB повышаются. [46]
История
Росиглитазон был одобрен FDA США в 1999 г. и EMA в 2000 г .; Тем не менее, EMA потребовалось провести два постмаркетинговых исследования долгосрочных побочных эффектов, одно - для хронической сердечной недостаточности, а другое - для сердечно-сосудистых. [10]
Общество и культура
Продажи
Продажи препарата в США составили 2,2 миллиарда долларов в 2006 году. [47] Продажи во 2 квартале 2007 года снизились на 22% по сравнению с 2006 годом. [48] Продажи в 4 квартале 2007 года снизились до 252 миллионов долларов. [49]
Хотя продажи снизились с 2007 года из-за проблем с безопасностью, общий объем продаж Avandia в 2009 году во всем мире составил 1,2 миллиарда долларов. [50]
Судебные иски
По данным аналитиков UBS, к марту 2010 года было подано 13 000 исков. [51] Среди тех, кто подает иск: округ Санта-Клара, Калифорния , который утверждает, что в период с 1999 по 2007 год в своей государственной больнице потратил 2 миллиона долларов на розиглитазон и просит «тройные убытки». [52] В мае 2010 года GlaxoSmithKline (GSK) достигла соглашения об урегулировании некоторых исков против компании, согласившись выплатить 60 миллионов долларов для урегулирования 700 исков. [53] В июле 2010 года GSK достигла мирового соглашения о закрытии еще 10 000 исков против нее, согласившись выплатить около 460 миллионов долларов для урегулирования этих исков. [54] [55] [56]
В 2012 году Министерство юстиции США объявило, что GlaxoSmithKline согласился признать себя виновным и выплатить штраф в размере 3 миллиардов долларов, в частности, за утаивание результатов двух исследований сердечно-сосудистой безопасности Avandia в период с 2001 по 2007 годы. из GlaxoSmithKline, включая бывшего старшего менеджера по развитию маркетинга компании и регионального вице-президента, который информировал правительство о ряде ненадлежащих практик с конца 1990-х до середины 2000-х годов. [37]
Расследования Соединенных Штатов
GlaxoSmithKline расследовалась FDA и Конгрессом США в отношении Avandia.
Сенаторы-демократ Макс Бокус и республиканец Чарльз Грассли подали отчет, в котором призвали GSK отозвать Avandia в 2008 году из-за побочных эффектов. В отчете отмечалось, что препарат вызывал 500 сердечных приступов, которых можно было избежать в месяц, и официальные лица Glaxo пытались запугать врачей, критиковавших препарат. В нем также говорится, что GSK продолжает продавать и продвигать препарат, несмотря на то, что знает о повышенном риске сердечных приступов и инсульта. [57]
Финансовый комитет Сената , в исследовании панели, показал электронные письма от должностных лиц компании GSK , которые предлагают компанию преувеличивать результаты научных исследований о безопасности рисков , уходящей в 2000 Утверждалось также комитет , что компания инициировала «Ghostwriting кампании», в результате чего GSK искал сторонние компании для написания положительных статей об Avandia для публикации в медицинских журналах. [58] GSK защищалась, представив данные о том, что ее собственные тесты показали, что Avandia безопасна, хотя отчет персонала FDA показал, что выводы были ошибочными. [59]
14 июля 2010 года, после двух дней обширных обсуждений, комиссия FDA, расследовавшая Avandia, пришла к смешанному голосованию. Двенадцать членов комиссии проголосовали за изъятие препарата из продажи, 17 рекомендовали оставить его, но с более пересмотренной предупреждающей этикеткой, а трое проголосовали за то, чтобы оставить его на рынке с нынешней предупреждающей этикеткой. [60] [61] Однако комиссия пришла к некоторому противоречию; 20 июля 2010 года было обнаружено, что один из участников дискуссии был платным докладчиком GlaxoSmithKline, что вызвало вопросы о конфликте интересов. Этот член комиссии был одним из трех, кто проголосовал за то, чтобы Avandia оставалась на рынке без дополнительных предупреждающих надписей. [62] [63]
В 2011 году FDA приняло решение о пересмотре информации о назначениях и руководствах по лекарствам для всех лекарств, содержащих росилитазон. Этикетка в США для розиглитазона ( Avandia , GlaxoSmithKline ) и всех препаратов, содержащих розиглитазон ( Avandamet и Avandaryl ), теперь включает дополнительную информацию о безопасности и ограничения. [64] [65] Пересмотренные этикетки ограничивают использование пациентами, которые уже принимают лекарство, содержащее розиглитазон, или новыми пациентами, которые не могут достичь адекватного гликемического контроля на других лекарствах от диабета, а также теми, кто после консультации со своим лечащим врачом решил не принимать Актос ( пиоглитазон) или другие лекарства, содержащие пиоглитазон, по медицинским показаниям. [66]
В июне 2013 года Консультативный комитет FDA рассмотрел все доступные данные, в том числе пересмотренное исследование RECORD, не обнаружил доказательств повышенного сердечно-сосудистого риска с Avandia и проголосовал за снятие ограничений на маркетинг Avandia в Соединенных Штатах. В ноябре 2013 года FDA США сняло эти маркетинговые ограничения на продукт. [67]По указанию FDA производитель Avandia, GlaxoSmithKline, профинансировал Институт клинических исследований Дьюка для повторного анализа необработанных данных исследования. На панели 2010 года три члена комиссии проголосовали за то, что существующие предупреждения достаточно хороши; двое были еще в 2013 году. Семь проголосовали за усиление этих предупреждений, и пять из них вернулись. Но из 10 проголосовавших за ограничение использования Avandia вернулись только четверо. Из 12 проголосовавших в 2010 году за вывод Avandia с рынка только трое вернулись. [68]
Европейские расследования
В 2000 году EMA запросило исследование, направленное на решение проблем безопасности сердечно-сосудистой системы, и разработчики согласились провести постмаркетинговое исследование долгосрочной сердечно-сосудистой заболеваемости / смертности у пациентов, принимающих розиглитазон в сочетании с сульфонилмочевиной или метформином: исследование RECORD . Результаты, опубликованные в 2009 году, показали не меньшую эффективность в отношении сердечно-сосудистых событий и смерти от сердечно-сосудистых заболеваний при сравнении лечения розиглитазоном с метформином или сульфонилмочевиной. Для инфаркта миокарда было статистически недостоверное увеличение риска. В своей оценке европейские регулирующие органы признали слабые стороны исследования, такие как неожиданно низкая частота сердечно-сосудистых событий и открытоедизайн, который может привести к предвзятости в отчетности. Они обнаружили, что результаты неубедительны. [17] 23 сентября 2010 г. Европейское агентство по лекарственным средствам рекомендовало приостановить продажу Avandia на европейском рынке. [10] [11]
Согласно исследованию, проведенному British Medical Journal в сентябре 2010 года, Комиссия Соединенного Королевства по лекарственным средствам для человека еще в июле 2010 года рекомендовала Агентству по регулированию лекарственных средств и товаров медицинского назначения (MHRA) отозвать продажу Avandia, поскольку ее «риски перевешивают ее преимущества». Кроме того, расследование показало, что в 2000 году члены Европейской комиссии, отвечающие за проверку Avandia до ее утверждения, были обеспокоены долгосрочными рисками, связанными с этим препаратом. [69] [70]
Новая Зеландия
Росиглитазон был отозван с рынка Новой Зеландии в апреле 2011 года, поскольку Medsafe пришла к выводу, что предполагаемые сердечно-сосудистые риски препарата для пациентов с диабетом 2 типа перевешивают его преимущества. [71]
Южная Африка
В уведомлении, выпущенном Советом по контролю за лекарственными средствами Южной Африки 5 июля 2011 г., говорится, что 3 июля 2011 г. он принял решение отозвать все лекарства, содержащие розиглитазон, с рынка Южной Африки из-за рисков для безопасности. Это запретило все новые рецепты Avandia. [72]
Споры и ответ
После сообщений в 2007 году о том, что Avandia может значительно увеличить риск сердечных приступов, препарат вызвал споры. Статья 2010 года в журнале Timeиспользует дело Avandia как доказательство неработоспособности регулирующей системы FDA, которая «может оказаться не только фатальной, но и преступной». В нем подробно рассказывается о неудачах в раскрытии информации, а также добавляется, что «отчеты Конгресса показали, что GSK располагала ранними доказательствами сердечного риска, связанного с его препаратом, и что FDA знало об опасностях за несколько месяцев до того, как оно проинформировало общественность». В нем сообщается, что «FDA расследует, нарушила ли GSK закон, не проинформировав агентство о сердечных рисках Avandia», - сообщил заместитель комиссара FDA доктор Джошуа Шарфштейн. GSK пригрозила ученым, которые сообщали о неблагоприятных результатах исследований, и получила несколько писем с предупреждениями от FDA за вводящий в заблуждение маркетинг и отказ сообщить клинические данные. [73] Производитель препарата GlaxoSmithKline,имел дело с серьезной негативной реакцией против компании из-за разногласий по поводу препарата.[74] Продажи препарата значительно упали после того, как история впервые появилась в 2007 году, упав с 2,5 миллиардов долларов в 2006 году до менее чем 408 миллионов долларов в 2009 году в США. [75]
В ответ на рост риска сердечных приступов правительство Индии приказало GSK приостановить свое исследование под названием TIDE в 2010 году. [76] [77] FDA также приостановило исследование TIDE в Соединенных Штатах. [78]
Три группы врачей, Эндокринное общество , Американская диабетическая ассоциация и Американская ассоциация клинических эндокринологов , призвали пациентов продолжать прием препарата, поскольку было бы намного хуже прекратить все лечение, несмотря на любой связанный с этим риск, но пациенты могли бы проконсультироваться. своих врачей и начнут переходить на другой препарат, если они или их врачи обнаружат беспокойство. [79] [80] [81] Американская ассоциация сердцав заявлении от июня 2010 г. говорится: «... отчеты заслуживают серьезного рассмотрения, и пациенты с диабетом в возрасте 65 лет и старше, получающие розиглитазон, должны обсудить результаты со своим лечащим врачом ...». «Для пациентов с диабетом наиболее серьезными последствиями являются болезни сердца и инсульт, и риск их возникновения значительно увеличивается при наличии диабета. Как и в большинстве ситуаций, пациенты не должны менять или прекращать прием лекарств, не посоветовавшись со своим лечащим врачом». [82] [83]
В результате дела Avandia FDA потребовало продемонстрировать кардиологическую безопасность новых препаратов для лечения диабета 2 типа. Этот процесс описан доктором Робертом Мисбином в INSULIN-History от FDA Insider, опубликованном 1 июня 2020 года на Amazon. Доктор Мисбин был первым рецензентом FDA для розиглитазона (Avandia) и предупредил о его способности повышать риск сердечно-сосудистых заболеваний.
Исследовать
Rosiglitazone думали , чтобы иметь возможность пациентов выгоды с болезнью Альцгеймера , которые не экспрессируют apoE4 аллели , [84] , но испытания фазы III , предназначенных для тестирования это показало , что розиглитазон оказался неэффективным у всех пациентов, в том числе apoE4 -отрицательных пациентов. [85]
Розиглитазон также может лечить язвенный колит легкой и средней степени тяжести из-за его противовоспалительных свойств в качестве лиганда PPAR. [86]
Синтез
использованная литература
- ^ a b Nissen SE, Wolski K (2007). «Влияние розиглитазона на риск инфаркта миокарда и смерти от сердечно-сосудистых причин» . N. Engl. J. Med . 356 (24): 2457–71. DOI : 10.1056 / NEJMoa072761 . PMID 17517853 . S2CID 46431986 .
- ^ США 5002953
- ^ Фишер, Джнос; Ганеллин, С. Робин (2006). Открытие лекарств на основе аналогов . Джон Вили и сыновья. п. 450. ISBN 9783527607495.
- ^ а б в г Чен X, Ян Л., Чжай С.Д. (2012). «Риск сердечно-сосудистых заболеваний и общей смертности среди пациентов с диабетом, которым назначают розиглитазон или пиоглитазон: метаанализ ретроспективных когортных исследований». Подбородок. Med. Дж . 125 (23): 4301–6. PMID 23217404 .
- ^ "Glaxo Удержал исследование Avandia, бывший регулятор сказал, чтобы дать показания" . Блумберг.
- ↑ Гардинер Харрис (19 февраля 2010 г.). «Противоречивое лекарство от диабета вредит сердцу, - заключает США» . Нью-Йорк Таймс .
- ^ «Самый популярный информационный бюллетень по электронной почте» . USA Today . 2011-05-24.
- ^ "Авандия Glaxo освобождена от ограничений продаж FDA" . Блумберг.
- ^ Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (25 ноября 2013 г.). «FDA требует снятия определенных ограничений на лекарство от диабета Avandia» .
- ^ a b c d «Европейское агентство по лекарственным средствам рекомендует приостановить прием Avandia, Avandamet и Avaglim» . Новости и события . Европейское агентство по лекарственным средствам. 2018-09-17.
- ^ a b c «Призыв« приостановить действие »лекарства от диабета» . Новости BBC. 2010-09-23.
- ^ «Наркотики запрещены в Индии» . Центральная организация по контролю за стандартами лекарственных средств, Dte.GHS, Министерство здравоохранения и благополучия семьи, правительство Индии. Архивировано из оригинала на 2015-02-21 . Проверено 17 сентября 2013 .
- ^ "Лекарство от диабета снято" . Stuff.co.nz . NZPA . 17 февраля 2011 года Архивировано из оригинала 13 октября 2013 года . Проверено 5 ноября 2011 года .
- ^ a b Рихтер Б., Бандейра-Эхтлер Э, Бергерхофф К., Клар С., Эбрахим С.Х. (2007). «Росиглитазон при сахарном диабете 2 типа» . Кокрановская база данных Syst Rev (3): CD006063. DOI : 10.1002 / 14651858.CD006063.pub2 . PMC 7389529 . PMID 17636824 .
- ^ Selvin Е, Болен С, Е НС, Уайли С, Уилсон Л.М., Marinopoulos С.С., Фельдман л, Vassy Дж, Уилсон R, бас Е.Б., Brancati FL (2008). «Сердечно-сосудистые исходы в испытаниях пероральных лекарств от диабета: систематический обзор» . Arch. Междунар. Med . 168 (19): 2070–80. DOI : 10,1001 / archinte.168.19.2070 . PMC 2765722 . PMID 18955635 .
- ^ Ajjan РА Грант PJ (2008). «Сердечно-сосудистая безопасность розиглитазона». Экспертное мнение Drug Saf . 7 (4): 367–76. DOI : 10.1517 / 14740338.7.4.367 . PMID 18613801 . S2CID 73109231 .
- ^ a b c d Blind E, Dunder K, de Graeff PA, Abadie E (2011). «Росиглитазон: перспективы европейского регулирования» . Диабетология . 54 (2): 213–8. DOI : 10.1007 / s00125-010-1992-5 . PMID 21153629 . S2CID 33360502 .
- ^ Mannucci Е, Monami М, Ди Бари М, Lamanna С, Р Гори, Gensini Г.Ф., Маркьонен N (2010). «Профиль сердечной безопасности розиглитазона: комплексный метаанализ рандомизированных клинических исследований». Int. J. Cardiol . 143 (2): 135–40. DOI : 10.1016 / j.ijcard.2009.01.064 . PMID 19328563 .
- ^ Уоллах, Джошуа Д.; Ван, Кун; Чжан, Одри Д; Ченг, Дина; Гроссетта Нардини, Холли К.; Линь, Хайцюнь; Bracken, Майкл Б.; Десаи, Маюр; Крумхольц, Харлан М; Росс, Джозеф С. (5 февраля 2020 г.). «Обновление информации о розиглитазоне и риске сердечно-сосудистых заболеваний с помощью общих данных: метаанализ индивидуального пациента и сводного уровня» . BMJ . 368 : 17078. DOI : 10.1136 / bmj.l7078 . PMC 7190063 . PMID 32024657 .
- ^ a b c Локи Ю.К., Квок С.С., Сингх С. (2011). «Сравнительные сердечно-сосудистые эффекты тиазолидиндионов: систематический обзор и метаанализ обсервационных исследований» . BMJ . 342 : d1309. DOI : 10.1136 / bmj.d1309 . PMC 3230110 . PMID 21415101 .
- ^ Ниссен, Стивен. «Росиглитазон - критический обзор. Презентация для Консультативного комитета FDA» (PDF) . Проверено 30 марта 2014 .
- ^ «Обзор медицинского специалиста по заявке на новое лекарство 21-071: Росиглитазон (Авандия)» (PDF) . 19 апреля 1999 . Проверено 26 мая 2014 года .
- ^ Ниссен, Стивен (2013). «Росиглитазон: случай регуляторного высокомерия» . BMJ . 347 : f7428. DOI : 10.1136 / bmj.f7428 . PMID 24335808 . S2CID 42125428 .
- ^ «Безопасность Rosiglitazone Maleate (Avandia)» .
- ^ а б Сингх, S; Loke, YK; Furberg, CD (12 сентября 2007 г.). «Долгосрочный риск сердечно-сосудистых событий с розиглитазоном: метаанализ» . JAMA: Журнал Американской медицинской ассоциации . 298 (10): 1189–95. DOI : 10,1001 / jama.298.10.1189 . PMID 17848653 . S2CID 41755937 .
- Перейти ↑ Diamond GA, Bax L, Kaul S (2007). «Неопределенные эффекты розиглитазона на риск инфаркта миокарда и смерти от сердечно-сосудистых заболеваний» . Анна. Междунар. Med . 147 (8): 578–81. DOI : 10.7326 / 0003-4819-147-8-200710160-00182 . PMID 17679700 .
- ^ Рихтер В, Бандейре-Echtler Е, Bergerhoff К, Clar С, Эбраимом SH (2007). «Росиглитазон при сахарном диабете 2 типа» (PDF) . Кокрановская база данных Syst Rev (3): CD006063. DOI : 10.1002 / 14651858.CD006063.pub2 . PMC 7389529 . PMID 17636824 .
- ^ "Документы" .
- ^ «Отчет персонала о GlaxoSmithKline и лекарстве от диабета Avandia» , Комитет по финансам, Сенат США, январь 2010 г.
- ^ Дэвид Грэм , «Оценка сердечно-сосудистых рисков и пользы для здоровья от розиглитазона» , Управление по надзору и эпидемиологии, Управление по санитарному надзору за качеством пищевых продуктов и медикаментов, 30 июля 2007 г.
- ^ «FDA добавляет предупреждение о рисках, связанных с сердцем, в антидиабетический препарат Avandia. Агентство требует, чтобы лекарство оставалось на рынке, пока продолжается оценка безопасности» , Управление по санитарному надзору за качеством пищевых продуктов и медикаментов, 14 ноября 2007 г.
- ^ Graham DJ, Уэлла-Хеллстр R, MaCurdy TE, Али F, Sholley C, Уорролл C, Kelman JA (2010). «Риск острого инфаркта миокарда, инсульта, сердечной недостаточности и смерти у пожилых пациентов Medicare, получающих розиглитазон или пиоглитазон» . ДЖАМА . 304 (4): 411–8. DOI : 10,1001 / jama.2010.920 . PMID 20584880 .
- Перейти ↑ Nissen SE, Wolski K (2010). «Возвращение к розиглитазону: обновленный метаанализ риска инфаркта миокарда и сердечно-сосудистой смертности» . Arch. Междунар. Med . 170 (14): 1191–1201. DOI : 10,1001 / archinternmed.2010.207 . PMID 20656674 .
- ^ Mannucci Е, Monami М, Ди Бари М, Lamanna С, Р Гори, Gensini Г.Ф., Маркьонен N (2010). «Профиль сердечной безопасности розиглитазона: комплексный метаанализ рандомизированных клинических исследований». Int. J. Cardiol . 143 (2): 135–40. DOI : 10.1016 / j.ijcard.2009.01.064 . PMID 19328563 .
- ^ a b c d e Джонас, Дэн. «Обзор класса лекарств: новые лекарства от диабета, TZD и их комбинации. Обзоры классов лекарств в окончательном исходном отчете» . Орегонский университет здоровья и науки . Проверено 1 апреля 2014 года .
- ↑ Hughes S (27 марта 2011 г.). «Еще более убедительные данные о розиглитазоне» . theheart.org . Проверено 6 апреля 2011 года .
- ^ a b Томас, Кэти; Шмидт, Майкл С. (2 июля 2012 г.). «Glaxo соглашается выплатить 3 миллиарда долларов в рамках урегулирования мошенничества» . Нью-Йорк Таймс .
- ^ Graham DJ, Ouellet-Hellstrom R, MaCurdy TE и др. (Июль 2010 г.). «Риск острого инфаркта миокарда, инсульта, сердечной недостаточности и смерти у пожилых пациентов Medicare, получающих розиглитазон или пиоглитазон» . ДЖАМА . 304 (4): 411–8. DOI : 10,1001 / jama.2010.920 . PMID 20584880 .
- ^ Cobitz Александр R (февраль 2007). «Наблюдение в клинических испытаниях увеличения частоты переломов у женщин-пациентов, получавших длительное лечение таблетками авандии (розиглитазона малеат) для лечения сахарного диабета 2 типа» (PDF) . (49,9 КБ ) . GlaxoSmithKline . Проверено 10 апреля 2007 г.
- ^ Кан SE, Хэффнер С.М., Heise М.А., Herman WH, Холман RR, Jones Н.П., Kravitz Б.Г., Лачин JM, O'Neill MC, Zinman B, Viberti G (2006). «Гликемическая стойкость монотерапии розиглитазоном, метформином или глибуридом» . N. Engl. J. Med . 355 (23): 2427–43. DOI : 10.1056 / NEJMoa066224 . PMID 17145742 . S2CID 30076668 .
- ^ Loke, YK; Singh, S .; Фурберг, CD (6 января 2009 г.). «Длительное использование тиазолидиндионов и переломов при диабете 2 типа: метаанализ» . Журнал Канадской медицинской ассоциации . 180 (1): 32–39. DOI : 10,1503 / cmaj.080486 . PMC 2612065 . PMID 19073651 .
- ^ Kendall C, Wooltorton E (2006). «Росиглитазон (Авандия) и отек желтого пятна» . CMAJ . 174 (5): 623. DOI : 10,1503 / cmaj.060074 . PMC 1389823 . PMID 16467508 .
- ^ Р. Базельт, Распоряжение токсичными лекарствами и химическими веществами у человека , 8-е издание, Биомедицинские публикации, Фостер-Сити, Калифорния, 2008, стр. 1399-1400.
- ^ «розиглитазон» . DailyMed Национальная медицинская библиотека.
- ^ Ики-Järvinen H (2004). «Тиазолидиндионы». N. Engl. J. Med . 351 (11): 1106–18. DOI : 10.1056 / NEJMra041001 . PMID 15356308 .
- ^ Моханти П., Альджада А., Ганим Х, Хофмейер Д., Трипати Д., Сайед Т., Аль-Хаддад В., Дхинда С., Дандона П. (2004). «Доказательства мощного противовоспалительного эффекта розиглитазона» . J. Clin. Эндокринол. Метаб . 89 (6): 2728–35. DOI : 10.1210 / jc.2003-032103 . PMID 15181049 .
- ^ «FDA ужесточает предупреждения Avandia» . Медицинский маркетинг и СМИ. 2007-11-14.
- ↑ Рубин, Рита (26 июля 2007). «Панели FDA для взвешивания сердечного риска Avandia» . USA Today . Проверено 22 мая 2010 .
- ^ «Прибыль Glaxo за четвертый квартал упала на 10% на продажах Avandia (Обновление 6)» . Блумберг . 2008-02-07.
- ^ Ranii, Дэвид (2010-02-23). «Осадки Avandia могут поразить Треугольник» . Новости и обозреватель . Архивировано из оригинала на 2011-03-04 . Проверено 5 марта 2010 .
- ^ Рании, Дэвид (2010-03-05). «Avandia может стоить GSK миллиарды» . Новости и обозреватель . Архивировано из оригинала на 2012-10-02 . Проверено 5 марта 2010 .
- ^ «Округ Калифорния подает в суд на Glaxo из-за лекарства от диабета» . Бостон Глоуб . 2010-03-01. Архивировано из оригинала на 5 мая 2015 года . Проверено 25 февраля 2013 .
- ^ Фили Дж, Келли Т (2010-05-11). «Glaxo обещала заплатить около 60 миллионов долларов в рамках первого урегулирования проблемы сердечного риска в Avandia» . Блумберг.
- ^ Фили Дж, Келли Т (2010-07-13). «Glaxo обещала заплатить 460 миллионов долларов для урегулирования исков Avandia о возмещении ущерба» . Блумберг. Архивировано из оригинала на 2012-07-13.
- ^ Добер, Алистер (2010-07-14). «GSK» урегулирует претензии Avandia «в первый день слушаний по вопросам безопасности» . Независимый . Лондон.
- ^ "GSK оплачивает большую часть костюмов Avandia за 460 миллионов долларов" . FiercePharma.
- ^ "Интерактивный: Хронология: История Avandia | Необходимо знать" . PBS. 16 июля 2010 г.
- ^ "Судьба Авандии может быть решена сегодня" .
- ^ «Безопасность Avandia снова подвергается сомнению» .
- ^ «12 членов комиссии рекомендуют отказаться от Avandia» . FiercePharma.
- ^ "Что означает голосование Avandia?" . FiercePharma.
- Перейти ↑ Mundy A (2010-07-20). «Член комиссии, поддержавший Avandia, получает гонорары от Glaxo» . The Wall Street Journal .
- ^ Галлахер, Джеймс (2010-07-20). «Отчет: участник дискуссии Avandia оплачен GSK» .
- ^ Росс JS, Jackevicius C, Krumholz HM, Ridgeway J, Montori VM, Alexander GC, Zerzan J, Fan J, Shah ND (2012). «Государственные программы Medicaid не использовали предварительное разрешение для обеспечения более безопасного назначения после предупреждения о розиглитазоне» . Aff Health (Миллвуд) . 31 (1): 188–98. DOI : 10,1377 / hlthaff.2011.1068 . PMC 3319744 . PMID 22232110 .
- ^ О'Риордан М. «Новая этикетка розиглитазона включает ограничения на использование» . theheart.org . Проверено 1 апреля 2011 года .
- ^ "GSK пересматривает этикетку US Avandia, чтобы включить новые ограничения на использование" . GlaxoSmithKline. Архивировано из оригинального 17 февраля 2011 года . Проверено 1 апреля 2011 года .
- ^ «Росиглитазон-содержащие лекарства от диабета: сообщение о безопасности лекарств - снятие некоторых ограничений по назначению и отпуску» . Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США.
- ^ Херпер, Мэтью (2013-06-06). «Голосование Avandia положило конец эре скандалов, связанных с безопасностью лекарств» . Forbes . Проверено 31 марта 2014 года .
- ^ Дуглас, Джейсон (06.09.2010). «Медицинский журнал Великобритании ставит под сомнение лицензию Avandia» . The Wall Street Journal .
- ^ «Британские сторожевые псы голосуют за отзыв Avandia» . FiercePharma.
- ^ "Препарат от диабета будет отменен из-за опасений сердечного риска" . New Zealand Herald. 17 февраля 2011 г.
- ^ Совет по контролю за лекарствами. «Изъятие препаратов, содержащих розиглитазон, с рынка ЮА» . Департамент здравоохранения Южно-Африканской Республики. Архивировано из оригинала 5 ноября 2011 года . Проверено 25 ноября 2012 года .
- ^ "После Avandia: есть ли у FDA проблема с лекарствами?" . Время . 12 августа, 2010. Архивировано из оригинального 15 августа 2010 года.
- ^ "Будет ли Avandia удалена с рынка?" . Новости США.
- ^ «Эксклюзив: Сегодня Такеда запускает кампанию Actos DTC» . Медицинский маркетинг и СМИ. 2010-07-15.
- Перейти ↑ Silverman E (2010-07-20). "Нераскрытый конфликт на панели FDA Avandia?" . Фармалот. Архивировано из оригинала на 2010-07-23.
- ^ "Испытания препарата Avandia прекращены в Индии" . CBS Detroit. 2010-07-14.
- ^ «FDA приказывает Glaxo остановить испытание Avandia» . foodconsumer.org. Архивировано из оригинала на 2014-11-09.
- ^ "Не выбрасывайте Avandia, диабетики призывают пациентов" . Рейтер . 2010-07-15.
- ^ Maugh II, Томас Х. (2010-07-15). «Пациенты, принимающие Avandia, должны продолжать это делать, - говорят врачи» . Лос-Анджелес Таймс .
- ^ Кац, Нил (16.07.2010). «Avandia News: что нужно знать» . CBS News .
- ^ "Booster Shots" . Лос-Анджелес Таймс . 2010-06-29.
- ^ «Комментарий Американской кардиологической ассоциации: Консультативный комитет рекомендует Управлению по санитарному надзору за качеством пищевых продуктов и медикаментов США оставить на рынке розиглитазон (авандия), продолжить клинические испытания безопасности и эффективности» . Новости здоровья . redOrbit.
- ^ Риснер ME, Saunders AM, Альтман JF, Орманди GC, Ремесло S, Foley IM, Zvartau-Hind ME, Хосфорд DA, Розы AD (2006). «Эффективность розиглитазона в генетически определенной популяции с легкой и умеренной болезнью Альцгеймера» . Фармакогеномика Дж . 6 (4): 246–54. DOI : 10.1038 / sj.tpj.6500369 . PMID 16446752 .
- ^ Gold M, Alderton C, Zvartau-Hind M, S Egginton, Saunders AM, Irizarry M, S Craft, Ландрету G, Linnamägi U, Sawchak S (2010). «Монотерапия розиглитазоном при болезни Альцгеймера легкой и средней степени тяжести: результаты рандомизированного двойного слепого плацебо-контролируемого исследования III фазы» . Dement Geriatr Cogn Disord . 30 (2): 131–46. DOI : 10.1159 / 000318845 . PMC 3214882 . PMID 20733306 .
- ^ Льюис, JD (2008). «Означает ли 2008 год начало новой эры клинических исследований в гастроэнтерологии?». Гастроэнтерология . 134 (5): 1289. DOI : 10,1053 / j.gastro.2008.03.030 . PMID 18471502 .
- ^ Cantello, Бэрри CC (1994). «Синтез BRL 49653 - нового и мощного антигипергликемического средства». Биоорганический . 4 (10): 1181–1184. DOI : 10.1016 / S0960-894X (01) 80325-5 .
- ^ 2 ° Источник: Искусство синтеза наркотиков. Дуглас С. Джонсон (редактор), Джи Джек Ли (редактор), стр. 121–122.
внешние ссылки
- Статья в MedlinePlus
- Medscape
- Национальная медицинская библиотека США: Портал информации о лекарствах - Росиглитазон
- Ингибиторы 3β-гидроксистероиддегидрогеназы
- Ингибиторы CYP17A1
- Гепатотоксины
- Тиазолидиндионы
- Аминопиридины
- Фенольные эфиры
- Изъятые препараты
- Бренды GlaxoSmithKline