| Имена | |||
|---|---|---|---|
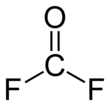
| Предпочтительное название IUPAC Карбонил дифторид | |||
| Другие имена Фторфосген; Оксид дифторида углерода; Фторметаноил фторид | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.005.941 | ||
| Номер ЕС |
| ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 2417 | ||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| COF 2 | |||
| Молярная масса | 66.01 г моль -1 | ||
| Внешность | Бесцветный газ | ||
| Плотность | 2,698 г / л (газ), 1,139 г / см 3 (жидкость при температуре плавления) | ||
| Температура плавления | -111,26 ° С (-168,27 ° F, 161,89 К) | ||
| Точка кипения | -84,57 ° С (-120,23 ° F, 188,58 К) | ||
| бурно реагирует с водой [1] | |||
| Давление газа | 55,4 атм (20 ° C) [1] | ||
| Структура | |||
| C 2v | |||
| 0,95 Д | |||
| Опасности | |||
| Основные опасности | Смертельно при вдыхании, реагирует с водой. | ||
| Пиктограммы GHS |     | ||
| Сигнальное слово GHS | Опасность | ||
| H280 , H290 , H314 , H330 , H331 , H370 | |||
| P234 , P260 , P261 , P264 , P270 , P271 , P280 , P284 , P301 + 330 + 331 , P303 + 361 + 353 , Р304 + 340 , P305 + 351 + 338 , P307 + 311 , Р310 , Р311 , P320 , P321 , P363 , P390 , P403 + 233 , Р404 , Р405 , Р410 + 403 , Р501 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | Негорючий | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | нет [1] | ||
REL (рекомендуется) | TWA 2 ppm (5 мг / м 3 ) ST 5 ppm (15 мг / м 3 ) [1] | ||
IDLH (Непосредственная опасность) | ND [1] | ||
| Родственные соединения | |||
Родственные соединения | Фосген карбонильного бромид формил фторид тиокарбонил хлорид Ацетон Мочевина Углекислота | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Карбонилфторид - это химическое соединение с формулой COF 2 . Этот газ, как и его аналог фосген , бесцветен и очень токсичен. Молекула плоская с симметрией C 2v .
Подготовка и свойства [ править ]
Карбонилфторид обычно получают как продукт разложения фторированных углеводородов при их термическом разложении, например, из трифторметанола или тетрафторметана в присутствии воды:
- CF
4+ H
2O → COF
2+ 2 ВЧ
Карбонилфторид можно также получить реакцией фосгена с фтористым водородом и окислением монооксида углерода , хотя последний имеет тенденцию приводить к чрезмерному окислению до четырехфтористого углерода . Окисление окиси углерода дифторидом серебра удобно:
- CO + 2 AgF
2→ COF
2+ 2 AgF
Карбонилфторид нестабилен в присутствии воды, гидролизуется до диоксида углерода и фтороводорода : [2]
- COF
2+ H
2O → CO
2+ 2 ВЧ
Безопасность [ править ]
Карбонилфторид токсичен с рекомендуемым пределом воздействия 2 ppm в качестве 8-часового среднего взвешенного по времени и 5 ppm в качестве краткосрочного (15-минутного среднего) воздействия. [3]
Ссылки [ править ]
- ^ a b c d e Карманный справочник NIOSH по химической опасности. «# 0108» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ MW Фарлоу; EH Man; CW Таллок (1960). «Карбонилфторид». Неорганические синтезы . Неорганические синтезы. 6 . С. 155–158. DOI : 10.1002 / 9780470132371.ch48 . ISBN 9780470132371.
- ^ «Карбонил фторид» . Карманный справочник NIOSH по химической опасности . Центры CDC по контролю и профилактике заболеваний . Проверено 10 сентября 2013 .