| |||
| Идентификаторы | |||
|---|---|---|---|
3D модель ( JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.033.734 | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
CompTox Dashboard ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| ClF 5 | |||
| Молярная масса | 130,445 г моль -1 | ||
| Внешность | бесцветный газ | ||
| Плотность | 4,5 кг / м 3 (г / л) | ||
| Температура плавления | -103 ° С (-153 ° F, 170 К) | ||
| Точка кипения | -13,1 ° С (8,4 ° F, 260,0 К) | ||
| Гидролизует | |||
| Структура | |||
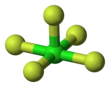
| Квадрат пирамидальный | |||
| Термохимия | |||
Стандартная мольная энтропия ( S | 310,73 Дж -1 моль -1 | ||
Std энтальпия формации (Δ F H ⦵ 298 ) | −238,49 кДж моль −1 | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Пентафторид хлора представляет собой межгалогенное соединение с формулой ClF 5 . Этот бесцветный газ является сильным окислителем, который когда-то был кандидатом в окислитель ракет. Молекула принимает квадратную пирамидальную структуру с C 4V симметрии , [1] , что подтверждается его высокой разрешающей способностью 19 F - ЯМР - спектр . [2]
Подготовка [ править ]
Некоторые из самых ранних исследований препарата были засекречены. [3] [4] Он был впервые получены путем фторирования из трифторида хлора при высоких температурах и высоких давлениях: [3]
- ClF 3 + F 2 → ClF 5
- ClF + 2F 2 → ClF 5
- Cl 2 + 5F 2 → 2ClF 5
- CsClF 4 + F 2 → CsF + ClF 5
NiF 2 катализирует эту реакцию. [5]
Фториды некоторых металлов, MClF 4 (т.е. KClF 4 , RbClF 4 , CsClF 4 ), реагируют с F 2 с образованием ClF 5 и соответствующего фторида щелочного металла. [4]
Реакции [ править ]
В сильно экзотермической реакции ClF 5 реагирует с водой с образованием фтористого хлорида и фтороводорода : [6]
- ClF
5+ 2 часа
2O → ClO
2F + 4 HF
Это также сильный фторирующий агент. При комнатной температуре он легко вступает в реакцию со всеми элементами (включая «инертные» элементы, такие как платина и золото ), за исключением благородных газов , азота , кислорода и фтора . [2]
См. Также [ править ]
- Трифторид хлора
- Гипервалентная молекула
Ссылки [ править ]
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . п. 833. ISBN 978-0-08-037941-8.
- ^ а б Пилипович, Д .; Maya, W .; Лоутон, EA; Бауэр, ВЧ; Шихан, Д.Ф .; Огимачи, штат Нью-Йорк; Wilson, RD; Гундерлой, ФК; Бедвелл, В. Е. (1967). «Пентафторид хлора. Получение и свойства». Неорганическая химия . 6 (10): 1918. DOI : 10.1021 / ic50056a036 .
- ^ a b Кларк, Джон Д. (1972). Зажигание! Неофициальная история жидкого ракетного топлива (PDF) . Издательство Университета Рутгерса. С. 87–88. ISBN 0-8135-0725-1.
- ^ а б Смит Д.Ф. (1963). «Пентафторид хлора». Наука . 141 (3585): 1039–1040. DOI : 10.1126 / science.141.3585.1039 . PMID 17739492 .
- ^ Šmalc А, Žemva В, Сливник Дж, Lutar К (1981). «О синтезе пентафторида хлора». Журнал химии фтора . 17 (4): 381–383. DOI : 10.1016 / S0022-1139 (00) 81783-2 .
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . п. 834. ISBN 978-0-08-037941-8.
Внешние ссылки [ править ]
- Национальный реестр загрязнителей - информационный бюллетень по фторидам и соединениям
- Информационный бюллетень об опасных веществах в Нью-Джерси
- Страница веб-книги для ClF5