| Криоабляция | |
|---|---|
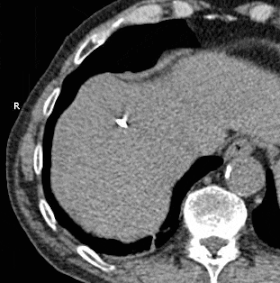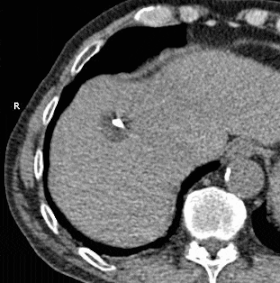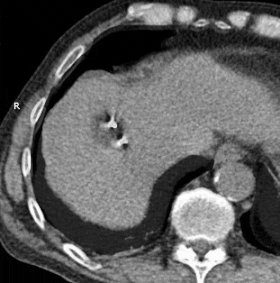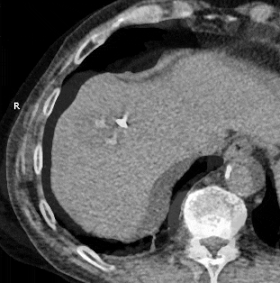 Анимированный GIF, показывающий криоабляцию массы в правой доле печени с помощью двух датчиков. Прошло примерно 30 минут. | |
| МКБ-9-СМ | 37,33 , 37,34 , 60,62 |
| MeSH | D003452 |
Криоабляция - это процесс, при котором для разрушения тканей используется сильный холод . Криоабляция выполняется с использованием полых игл (криозондов), через которые циркулируют охлаждаемые теплопроводные жидкости. Криозонды располагаются рядом с целью таким образом, чтобы процесс замораживания разрушал пораженные ткани. После того, как зонды размещены, прикрепленный блок криогенной заморозки отводит тепло («охлаждает») кончик зонда и, за счет расширения, от окружающих тканей.
Абляция происходит в замороженной ткани по крайней мере с помощью трех механизмов:
- образование кристаллов льда внутри клеток, тем самым разрушая мембраны и, среди прочего, прерывая клеточный метаболизм;
- свертывание крови, тем самым прерывая кровоток к ткани, что, в свою очередь, вызывает ишемию и гибель клеток; и
- индукция апоптоза , так называемого каскада программируемой гибели клеток.
Чаще всего криоабляция применяется для удаления солидных опухолей в легких, печени, груди, почках и простате. Наиболее распространены криоаблация простаты и почек. Хотя иногда криоабляция применяется в криохирургии с помощью лапароскопических или открытых хирургических доступов, чаще всего криоаблация выполняется чрескожно (через кожу и в целевую ткань, содержащую опухоль) медицинским специалистом, например интервенционным радиологом . Термин от крио + абляции .
Простата [ править ]
Криоабляция простаты умеренно эффективна, но, как и любой другой процесс удаления простаты, также может привести к импотенции. Криоаблация простаты применяется у трех категорий пациентов:
- в качестве первичной терапии у пациентов, для которых сексуальная функция менее важна или которые не подходят для радикальной позадилонной простатэктомии (RRP, хирургическое удаление простаты);
- в качестве спасательной терапии у пациентов, которые не прошли брахитерапию (использование имплантированных радиоактивных «семян», помещенных в предстательную железу) или лучевой терапии с использованием внешнего луча (ДЛТ); и
- фокальная терапия небольших дискретных опухолей у молодых пациентов.
Рак костей [ править ]
Криоаблация изучалась как альтернатива радиочастотной абляции при лечении умеренной и сильной боли у людей с метастатическим поражением костей . Зона деструкции ткани, созданная этим методом, может более эффективно контролироваться КТ, чем РЧА, что является потенциальным преимуществом при лечении опухолей, прилегающих к критическим структурам. [1]
Почечный [ править ]
При лечении почечно-клеточного рака результаты криоабляции аналогичны результатам радиочастотной абляции . [2]
Рак груди [ править ]
Криоабляция при раке груди обычно возможна только при небольших опухолях. [3] Часто после криоабляции применяется хирургическое вмешательство. [3] По состоянию на 2014 г. необходимы дополнительные исследования, прежде чем он сможет заменить лампэктомию . [3]
Сердечный [ править ]
Другой тип криоабляции используется для восстановления нормальной электропроводности путем замораживания тканей или сердечных путей, которые мешают нормальному распределению электрических импульсов сердца. Криоабляция используется в двух типах вмешательств для лечения аритмий : (1) процедуры с использованием катетера и (2) хирургические операции.
Катетер - это очень тонкая трубка, которая вводится в вену на ноге пациента и подводится к сердцу, где она передает энергию для лечения аритмии пациента. В хирургических процедурах гибкий зонд используется непосредственно на обнаженном сердце для подачи энергии, которая прерывает аритмию. При охлаждении кончика криоабляционного катетера ( кардиология ) или зонда ( кардиохирургия ) до минусовых температур клетки сердца, ответственные за проведение аритмии, изменяются так, что они больше не проводят электрические импульсы.
Фиброаденома [ править ]
Криоабляция в настоящее время также используется для лечения фиброаденом груди. Фиброаденомы - это доброкачественные опухоли молочной железы, которые встречаются примерно у 10% женщин (в основном в возрасте 15–30 лет). [4]
В этой процедуре, которая была одобрена Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA), в фиброаденому вводится управляемый ультразвуком датчик, а затем используются очень низкие температуры для разрушения аномальных клеток. [5] Со временем клетки реабсорбируются в организме. Процедура может проводиться в кабинете врача под местной анестезией и оставляет очень мало рубцов по сравнению с открытыми хирургическими процедурами. [5]
Катетерные процедуры [ править ]
Могут использоваться различные методы катетерной абляции, которые обычно делятся на две категории: (1) процедуры на основе холода, когда охлаждение тканей используется для лечения аритмии, и (2) процедуры на основе тепла, при которых высокая температура используется для изменения аномальная проводящая ткань в сердце.
Криоабляция [ править ]
Холодные температуры используются при криоабляции для охлаждения или замораживания клеток, которые нарушают сердечный ритм. Катетер отводит тепло от ткани, охлаждая ее до температуры -75 ° C. Это вызывает локальные рубцы, которые перерезают нежелательные проводящие пути.
Это гораздо более новый метод лечения суправентрикулярной тахикардии (СВТ) с непосредственным поражением предсердно-желудочкового (АВ) узла. СВТ с вовлечением АВ-узла часто является противопоказанием к использованию радиочастотной абляции из-за риска повреждения АВ-узла, что вынуждает пациентов получать постоянный кардиостимулятор. При криоабляции участки ткани можно картировать путем ограниченного обратимого замораживания (например, до -10 ° C). Если результат нежелателен, ткань можно нагреть без необратимого повреждения. В противном случае ткань можно удалить навсегда, заморозив ее до более низкой температуры (например, -73 ° C).
Эта терапия произвела революцию в области атриовентрикулярной возвратной тахикардии (AVNRT) и других атриовентрикулярных узловых тахиаритмий. Это позволило людям, которые иначе не были кандидатами на радиочастотную абляцию, получить шанс на лечение своей проблемы. Эта технология была разработана в Монреальском институте сердца в конце 1990-х годов. Терапия была успешно применена в Европе в 2001 году и в США в 2004 году после «Морозного испытания». [6]
В 2004 году эта технология была впервые применена на Среднем Западе США в больнице Майами-Вэлли в Дейтоне, штат Огайо, Марком Кребсом, доктором медицины, FACC, Мэтью Хоскинсом, RN, BSN и Кеном Питерманом, RN, BSN. Этим экспертам по электрофизиологии удалось вылечить первых 12 кандидатов в своем учреждении. [ необходима цитата ]
Криоабляция при AVNRT и других аритмиях действительно имеет некоторые недостатки. Недавнее исследование [7] пришло к выводу, что время процедуры для криоабляции в среднем немного выше, чем для традиционной радиочастотной (тепловой) абляции. Кроме того, с использованием этого метода было зарегистрировано более высокое количество отказов оборудования. Наконец, даже несмотря на то, что краткосрочный успех эквивалентен радиочастотному лечению, криоаблация, по-видимому, имеет значительно более высокую частоту долгосрочных рецидивов.
Тестирование сайта [ править ]
Криотерапия способна вызвать временный электрический блок, охлаждая ткань, которая, как считается, является проводящей аритмию. Это позволяет врачу убедиться, что это правильный сайт, прежде чем отключать его навсегда. Возможность протестировать сайт таким способом называется тестированием сайта или криопечатью .
При удалении ткани около АВ-узла (особого центра проводимости, передающего электрические импульсы от предсердий к желудочкам) существует риск возникновения сердечной блокады, то есть нормальная проводимость от предсердий не может передаваться в желудочки. Замораживание ткани около АВ-узла с меньшей вероятностью спровоцирует необратимую блокаду сердца, чем ее абляция с помощью тепла.
Хирургические процедуры [ править ]
Как и в процедурах с использованием катетера, для лечения аритмий во время операции на сердце могут использоваться методы с использованием температур нагрева или охлаждения. Существуют также методы, при которых в открытом сердце используются надрезы для прерывания аномальной электропроводности ( процедура лабиринта ). Криохирургия предполагает использование методов замораживания для лечения аритмий во время операции.
Врач может порекомендовать использование криохирургии во время операции на сердце в качестве вторичной процедуры для лечения любой аритмии, которая присутствовала или могла появиться во время первичной процедуры открытой груди. Наиболее распространенные операции на сердце, при которых криохирургия может использоваться таким образом, - это восстановление митрального клапана и шунтирование коронарной артерии . Во время процедуры на сердце или вокруг него помещается гибкий криозонд, который подает холодную энергию, которая выводит из строя ткани, ответственные за проведение аритмии.
Сосудистые мальформации [ править ]
Криоабляция недавно была использована для лечения сосудистых мальформаций с низким потоком, таких как венозные мальформации (VM) и фиброзно-жировые сосудистые аномалии (FAVA). Криоабляция оказалась эффективной для лечения этих заболеваний как в качестве основного лечения, так и после склеротерапии . [8]
Криоиммунотерапия [ править ]
Криоиммунотерапия - это онкологическое лечение различных видов рака, сочетающее криоабляцию опухоли с лечением иммунотерапией . [9] Сама по себе криоабляция опухоли in vivo может вызвать иммуностимулирующий, системный противоопухолевый ответ, в результате чего образуется противораковая вакцина - скрытый эффект . [10] Однако криоабляция сама по себе может вызвать недостаточный иммунный ответ, в зависимости от различных факторов, таких как высокая скорость замораживания. Сочетание криотерапии с иммунотерапией усиливает иммуностимулирующий ответ и оказывает синергетическое действие при лечении рака. [11]
История [ править ]
Использование холода для снятия боли и в качестве противовоспалительного средства было известно со времен Гиппократа (460–377 гг. До н.э.). [12] С тех пор появилось множество свидетельств использования льда для снятия боли, в том числе у древних египтян и у Авиценны из Персии (982–1070 гг. Нашей эры). [13]С 1899 года доктор Кэмпбелл Уайт использовал хладагенты для лечения различных состояний, в том числе: красной волчанки, опоясывающего герпеса, шанкроида, невусов, бородавок, варикозных язв на ногах, карбункулов, карцином и эпителиом. Де Кервен успешно использовал углекислый снег для лечения папиллом мочевого пузыря и рака мочевого пузыря в 1917 году. Д-р Ирвинг С. Купер в 1913 году продвинул область криотерапии, разработав зонд с жидким азотом, способный достигать температуры -196 ° C, и используя это для лечения болезни Паркинсона и ранее неоперабельного рака. Криозонд Купера продвинул практику криотерапии, что привело к растущему интересу и практике криотерапии. В 1964 году доктор Кахан успешно применил изобретение зонда с жидким азотом для лечения миомы матки и рака шейки матки. Криотерапия продолжала развиваться с доктором.Компания Amoils разрабатывает зонд для жидкого азота, способный достичь охлаждающего расширения, в 1967 году.[14] [15] [16]
С развитием технологий криозондов в 1960-х годах криотерапия стала широко применяться и практиковаться. С 1960-х годов во многих частях мира лечение рака печени, простаты, груди, костей и других форм рака проводилось криоаблацией. Японский врач доктор Танака начал лечение криоаблацией при метастатическом раке груди в 1968 году. [17] В течение следующих трех десятилетий доктор Танака успешно лечил малый и локализованный, а также запущенный и неоперабельный рак груди с помощью минимально инвазивной криоабляции. Все случаи рака груди доктора Танаки считались неизлечимыми: запущенными, неоперабельными и устойчивыми к лучевой терапии, химиотерапии и эндокринной терапии. [17]В то же время врачи, в том числе доктор Аблин и доктор Гейдж, начали использовать криоабляцию для лечения рака простаты и костей . [18] [19] Доктор Пол Дж. Ван и доктор Питер Л. Фридман изобрели криоабляцию сердца и сердечной аритмии в 1988 году. Их патенты касались катетера криоабляции и криогенного картирования (патенты США 5147355A и 5423807A ).
В 1980-х и 1990-х годах произошел значительный прогресс в области аппаратуры и методов визуализации с появлением CMS Cryoprobe и Accuprobe. [20] КТ , МРТ , криозонды с ультразвуковым контролем стали доступны и улучшили возможности криозондов в лечении. Воодушевленный последними достижениями в области криотерапии, Китай в 1990-х годах начал применять криотерапию для лечения многих онкологических заболеваний. [21] Поскольку преимущества хорошо известны, FDA одобрило лечение рака простаты с помощью криоабляции в 1998 году. [22]
См. Также [ править ]
- Интервенционная радиология
Ссылки [ править ]
- ^ Callstrom, Мэтью R .; Dupuy, Damian E .; Соломон, Стивен Б .; Берес, Роберт А .; Литтруп, Питер Дж .; Дэвис, Киркланд В .; Пас-Фумагалли, Рикардо; Хоффман, Шерил; Этвелл, Томас Д. (2013-03-01). «Чрескожная криоаблация болезненных метастазов в кости под визуальным контролем» . Рак . 119 (5): 1033–41. DOI : 10.1002 / cncr.27793 . ISSN 1097-0142 . PMC 5757505 . PMID 23065947 .
- ^ Эль Диб, R; Тома, штат Нью-Джерси; Капур, А (август 2012 г.). «Криоабляция против радиочастотной абляции для лечения почечно-клеточного рака: мета-анализ исследований серии случаев» . BJU International . 110 (4): 510–16. DOI : 10.1111 / j.1464-410x.2011.10885.x . PMID 22304329 .
- ^ a b c Сабель, MS (июль 2014 г.). «Нехирургическая абляция рака груди: будущие возможности при малых опухолях груди». Клиники хирургической онкологии Северной Америки . 23 (3): 593–608. DOI : 10.1016 / j.soc.2014.03.009 . PMID 24882353 .
- ^ Медицинский словарь
- ^ a b WebMD - Криотерапия уменьшает доброкачественные образования в груди
- ^ "Архивная копия" . Архивировано из оригинала на 2013-12-19 . Проверено 18 декабря 2013 .CS1 maint: заархивированная копия как заголовок ( ссылка )
- ^ Ноябрь 2010 Немецкое исследование CYRANO (Криоабляция в сравнении с радиочастотной энергией для аблации атриовентрикулярной узловой реентрантной тахикардии)
- ^ Гевара, Карлос Дж; Рамасвами, Раджа С. Тивари, Татуля; Дарси, Майкл Д; Ким, Сын К.; Акинванде, Олагуоке; Дасгупта, Нилой (2019). «Криоаблация низкопоточных сосудистых мальформаций» . Диагностическая и интервенционная радиология . Авес Яинджилик ООО НТИ. 25 (3): 225. doi : 10.5152 / dir.2019.18278 - через ProQuest.
- ^ Сидана Абхинав (2014). «Иммунотерапия рака с использованием криоабляции опухолей». Иммунотерапия . 6 (1): 85–93. DOI : 10.2217 / imt.13.151 . PMID 24341887 .
- ^ С улучшением визуализации груди и вмешательств под визуальным контролем появляется интерес к абляционным методам лечения рака груди. Криохирургия вызывает воспаление и оставляет нетронутыми опухолеспецифические антигены, что может вызвать противоопухолевый иммунный ответ. Тарковский Р., Рзаца М. (2005). «Иммунологический ответ на криоабляцию рака груди» . Gland Surg . 3 (2): 88–93. DOI : 10.3978 / j.issn.2227-684X.2014.03.04 . PMC 4115762 . PMID 25083502 .
- ^ Хаен SP, Pereira PL, Салих HR, Rammensee HG, Gouttefangeas C (2011). «Больше, чем просто разрушение опухоли: иммуномодуляция посредством термической абляции рака» . Clin Dev Immunol . 2011 : 1–19. DOI : 10.1155 / 2011/160250 . PMC 3254009 . PMID 22242035 .
- Перейти ↑ Cooper (2001). «История криохирургии» . JR Soc Med . 94 (4): 196–201. DOI : 10.1177 / 014107680109400416 . PMC 1281398 . PMID 11317629 .
- ^ Trescott (2003). «Криоаналгезия в интервенционном лечении боли». Врач боли . 6 (3): 345–60. PMID 16880882 .
- Перейти ↑ Gage AA (1998). «История криохирургии». Semin Surg Oncol . 14 (2): 99–109. DOI : 10.1002 / (sici) 1098-2388 (199803) 14: 2 <99 :: aid-ssu2> 3.0.co; 2-1 . PMID 9492880 .
- ^ Фрейман, Анатолий; Бакалавр, Натаниэль Буганим (2005). «История криотерапии» . Интернет-журнал дерматологии . 11 (2).
- ^ Купер С., Добер RP (2001). «История криохирургии» . JR Soc Med . 94 (4): 196–201. DOI : 10.1177 / 014107680109400416 . PMC 1281398 . PMID 11317629 .
- ^ а б Ричард Дж. Аблин (1998). «Использование криохирургии при раке груди» . Arch Surg . 133 (1): 106. DOI : 10.1001 / archsurg.133.1.106 . PMID 9438770 .
- ^ Marcove RC, Miller TR (1969). «Лечение первичных и метастатических локализованных опухолей костей криохирургией». Surg Clin North Am . 49 (2): 421–30. DOI : 10.1016 / s0039-6109 (16) 38799-0 . PMID 5774987 .
- ^ RJ Ablin; и другие. (1971). «Перспективы криоиммунотерапии при метастазирующем раке простаты». Криобиология . 8 (3): 271–79. DOI : 10.1016 / 0011-2240 (71) 90050-2 . PMID 5570410 .
- ^ Гейслер, Элиэзер; Хеллер, Ори (2012). Управление медицинскими технологиями: теория, практика и кейсы . п. 281. ISBN. 9781461555193.
- ^ Лечение опухолей с помощью криотерапии было впервые изобретено американцами в 1960-х годах. Направленный на продвижение новой технологии, ISC был основан в Австрии в 1972 году. Технология развивалась с каждым днем после более чем 30 лет разработки. В последние годы, в частности, Китай с его более активным экономическим развитием и научно-техническим прогрессом играет ведущую роль в мире как в теоретических исследованиях, так и в клиническом применении криотерапии. Криотерапия как эффективный медицинский метод лечения опухолей применяется во все большем числе медицинских учреждений Китая и достигла выдающейся эффективности в лечении рака. «Китай: новый председатель Международного общества криохирургии (ISC)» . 2015. Архивировано с оригинала.на 2016-10-20 . Проверено 23 октября 2016 .
- ^ "Центр устройств и радиологического здоровья Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США" .