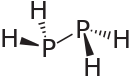| Имена | |||
|---|---|---|---|
| Название ИЮПАК Дифосфан | |||
| Систематическое название ИЮПАК Дифосфан (заместитель) Тетрагидридодифосфор ( P - P ) (добавка) | |||
| Другие имена Дифосфин | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ChemSpider | |||
PubChem CID | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| H 4 P 2 | |||
| Молярная масса | 65,980 г · моль -1 | ||
| Температура плавления | -99 ° С (-146 ° F, 174 К) | ||
| Точка кипения | 63,5 ° C (146,3 ° F, 336,6 K) (экстраполировано, разлагается) | ||
| Родственные соединения | |||
Другие анионы | аммиак гидразин триазан | ||
Другие катионы | дифосфины | ||
Связанные бинарные галогениды фосфора | Тетрафторид дифосфора Тетрахлорид дифосфора Тетрабромид дифосфора Тетраиодид дифосфора | ||
Родственные соединения | фосфаном triphosphane diphosphene diphosphenes | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Дифосфан - неорганическое соединение с химической формулой P 2 H 4 . Эта бесцветная жидкость является одним из нескольких бинарных гидридов фосфора. Это примесь, которая обычно вызывает воспламенение образцов фосфина на воздухе. Более старое название - дифосфин .
Свойства, подготовка, реакции [ править ]
Дифосфан принимает грубую конформацию (как гидразин , менее симметричный, чем показано на изображении) с расстоянием P − P 2,219 ангстрем . Он неосновной, нестабилен при комнатной температуре и самовоспламеняется на воздухе . Он плохо растворяется в воде, но растворяется в органических растворителях. Его 1 H-ЯМР-спектр состоит из 32 линий, являющихся результатом системы расщепления A 2 XX'A ' 2 . [1]
Дифосфан образуется в результате гидролиза монофосфида кальция , который можно описать как Ca 2+ производное P4-
2. В соответствии с оптимизированной процедурой гидролиз 400 г CaP при -30 ° C дает около 20 г продукта, слегка загрязненного фосфином .
Реакция дифосфана с бутиллитием дает множество конденсированных полифосфиновых соединений.
Органические дифосфаны [ править ]
Известны различные органические производные дифосфана. Эти соединения получают восстановительным связыванием, например тетрафенилдифосфин из хлордифенилфосфина :
- 2 ClPPh 2 + 2 Na → Ph 2 P − PPh 2 + 2 NaCl
Метильное соединение P 2 Me 4 получают восстановлением Me 2 P (S) -P (S) Me 2 , которое получают метилированием тиофосфорилхлорида метилмагнийбромидом. [2]
См. Также [ править ]
- Пниктоген гидрид
Ссылки [ править ]
- ^ Marianne Baudler, Клаус Глинка (1993). «Моноциклические и полициклические фосфины». Chem. Ред. 93 (4): 1623–1667. DOI : 10.1021 / cr00020a010 .
- ^ Масло, SA; Чатт, Дж. (1974). «Этиленбис (диметилфосфин)». Неорг. Synth . 15 : 185. DOI : 10.1002 / 9780470132463.ch41 .