| |||
| Имена | |||
|---|---|---|---|
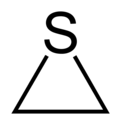
| Предпочтительное название IUPAC Тииран | |||
| Систематическое название ИЮПАК Тиациклопропан | |||
| Другие названия | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| 102379 | |||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.006.359 | ||
| Номер ЕС |
| ||
| 1278 | |||
| КЕГГ | |||
| MeSH | этилен + сульфид | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1992 г. | ||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| C 2 H 4 S | |||
| Молярная масса | 60,11 г · моль -1 | ||
| Появление | Бледно-желтая жидкость | ||
| Плотность | 1,01 г см −3 | ||
| Температура плавления | -109 ° С (-164 ° F, 164 К) | ||
| Точка кипения | 56 ° С; 133 ° F; 329 К | ||
| Давление газа | 28,6 кПа (при 20 ° C) | ||
| Термохимия | |||
Std энтальпия формации (Δ F H ⦵ 298 ) | 51-53 кДж моль -1 | ||
Std энтальпии сгорания (Δ с Н ⦵ 298 ) | -2,0126 МДж моль -1 | ||
| Опасности | |||
| Пиктограммы GHS |   | ||
| Сигнальное слово GHS | Опасность | ||
Положения об опасности GHS | H225 , H301 , H318 , H331 | ||
Меры предосторожности GHS | P210 , P261 , P280 , P301 + 310 , P305 + 351 + 338 , P311 | ||
| NFPA 704 (огненный алмаз) |  3 4 2 | ||
| точка возгорания | 10 ° С (50 ° F, 283 К) | ||
| Родственные соединения | |||
Родственные гетероциклы | Оксид этилена Азиридин Бориран | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Тиран , более известный как сульфид этилена , представляет собой циклическое химическое соединение с формулой C 2 H 4 S. [2] Это наименьший серосодержащий гетероцикл и простейший эписульфид . Как и многие сероорганические соединения, этот вид имеет очень неприятный запах. Тииран также используется для описания любого производного исходного сульфида этилена.
Структура [ править ]
По данным электронной дифракции , расстояния CC и CS в сульфиде этилена составляют 1,473 и 1,811 Å соответственно. Углы CCS и CSC составляют соответственно 66,0 и 48,0 °. [3]
Подготовка и реакции [ править ]
Его можно получить реакцией этиленкарбоната и KSCN . [4] Для этого KSCN сначала плавится в вакууме для удаления воды.
- KSCN + C 2 H 4 O 2 CO → KOCN + C 2 H 4 S + CO 2
Этиленсульфид добавляется к аминам с получением 2-меркаптоэтиламинов [5], которые являются хорошими хелатирующими лигандами.
- С 2 Н 4 S + R 2 NH → R 2 NCH 2 CH 2 SH
Этот процесс часто называют меркаптоэтилированием . [6]
Окисление тиирана периодатом дает эписульфоксид этилена .
Ссылки [ править ]
- ^ a b «тиран (CHEBI: 30977)» . Химические объекты, представляющие биологический интерес (ChEBI) . Великобритания: Европейский институт биоинформатики.
- ^ Уоррен Чу; Дэвид Н. Харпп (1993). «Последние аспекты химии тиранов». Журнал химии серы . 15 (1): 1–39. DOI : 10.1080 / 01961779308050628 .CS1 maint: несколько имен: список авторов ( ссылка )
- ^ Wataru Ando Nami Choi Норихиро Tokitoh (1996). «Тиираны и тиирены: моноциклические». Комплексная гетероциклическая химия II . 1А . С. 173–240. DOI : 10.1016 / B978-008096518-5.00005-8 .CS1 maint: использует параметр авторов ( ссылка )
- ^ Searles, S .; Lutz, EF; Hays, HR; Мортенсен, HE (1962). «Сульфид этилена» . Органический синтез . 42 : 59. DOI : 10,15227 / orgsyn.042.0059 .
- ^ RJ Cremlyn «Введение в химию органосеры» John Wiley and Sons: Chichester (1996). ISBN 0-471-95512-4 .
- ^ Гунар Zelans, Jacquelyn Gervay-Гаага, Ivy Maulie (2010). «Сульфид этилена». Энциклопедия реагентов для органического синтеза . Джон Вили и сыновья. DOI : 10.1002 / 047084289X.re079.pub2 .CS1 maint: использует параметр авторов ( ссылка )