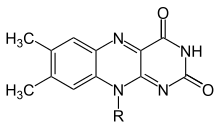
Флавин (от латинского flavus , «желтый») - это общее название группы органических соединений на основе птеридина , образованных трициклическим гетероциклом изоаллоксазином . Биохимический источник - витамин рибофлавин . Флавиновый фрагмент часто присоединяется к аденозиндифосфату с образованием флавинадениндинуклеотида ( FAD ), а в других случаях обнаруживается как флавинмононуклеотид (или FMN ), фосфорилированная форма рибофлавина.. Он находится в одной или другой из этих форм , что флавин присутствует в качестве простетической группы в флавопротеидах .
Флавиновая группа способна подвергаться окислительно-восстановительным реакциям и может принимать либо один электрон в двухступенчатом процессе, либо два электрона сразу. Восстановление осуществляется путем добавления атомов водорода к определенным атомам азота в изоаллоксазиновой кольцевой системе :

В водном растворе флавины окрашиваются в желтый цвет при окислении, приобретая красный цвет в полувосстановленном анионном состоянии или синий в нейтральном ( семихиноновом ) состоянии и бесцветный при полном восстановлении. [1] Окисленная и восстановленная формы находятся в быстром равновесии с семихиноновой ( радикальной ) формой, смещенной против образования радикала: [2]
- Fl ox + Fl красный H 2 ⇌ FlH •
где Fl ox - окисленный флавин, Fl red H 2 - восстановленный флавин (при добавлении двух атомов водорода) и FlH • семихиноновая форма (добавление одного атома водорода).
В форме FADH 2 он является одним из кофакторов, которые могут переносить электроны в цепь переноса электронов .
Фоторедукция [ править ]
Как свободные, так и связанные с белками флавины являются фото-восстанавливаемыми , то есть могут восстанавливаться под действием света по механизму, опосредованному несколькими органическими соединениями, такими как некоторые аминокислоты , карбоновые кислоты и амины . [2] Это свойство флавинов используется различными светочувствительными белками. Например, домен LOV, обнаруженный у многих видов растений, грибов и бактерий, претерпевает обратимое, зависимое от света структурное изменение, которое включает образование связи между остатком цистеина в его пептидной последовательности и связанным FMN. [3]
FAD [ править ]
Флавинадениндинуклеотид представляет собой группу , связанную с многих ферментов , в том числе ферредоксин-НАДФ + -редуктазы , моноаминоксидазы , D-аминокислоты оксидазы , глюкозооксидазы , ксантиноксидазы , и ацил - СоА - дегидрогеназы .
FADH / FADH 2 [ править ]
FADH и FADH 2 - это восстановленные формы FAD. FADH 2 продуцируется как простетическая группа сукцинатдегидрогеназы , фермента, участвующего в цикле лимонной кислоты . При окислительном фосфорилировании две молекулы FADH 2 обычно дают 1,5 АТФ каждая или три вместе взятых.
FMN [ править ]
Флавинмононуклеотид представляет собой простетическую группу, обнаруженную, среди других белков, в НАДН-дегидрогеназе , нитроредуктазе E.coli и старом желтом ферменте .
См. Также [ править ]
- Птеридин
- Птерин
- Деазафлавин (5-деазафлавин)
Ссылки [ править ]
- Перейти ↑ Michaelis L, Schubert MP, Smythe CV (1936). «Потенциометрическое исследование флавинов» . Журнал биологической химии . 116 (2): 587–607.
- ^ a b Мэсси В., Станкович М., Хеммерих П. (январь 1978 г.). «Опосредованное светом восстановление флавопротеинов с флавинами в качестве катализаторов». Биохимия . 17 (1): 1–8. DOI : 10.1021 / bi00594a001 . PMID 618535 .
- ^ Александр MT, Домратчева T, Бонетти C, ван Вильдерен LJ, ван Гронделл R, Groot ML, Hellingwerf KJ, Kennis JT (июль 2009 г.). «Первичные реакции домена LOV2 фототропина изучены с помощью сверхбыстрой спектроскопии в среднем инфракрасном диапазоне и квантовой химии» . Биофизический журнал . 97 (1): 227–37. DOI : 10.1016 / j.bpj.2009.01.066 . PMC 2711383 . PMID 19580760 .
Дальнейшее чтение [ править ]
- Воет Д., Воет Дж. Г. (2004). Биохимия (3-е изд.). Джон Вили и сыновья. ISBN 0-471-39223-5.