Перейти к навигации Перейти к поиску
 | |
 | |
| Идентификаторы | |
|---|---|
3D модель ( JSmol ) | |
| ChemSpider | |
PubChem CID | |
| UNII | |
CompTox Dashboard ( EPA ) | |
| |
| |
| Характеристики | |
| F N O 3 | |
| Молярная масса | 81,002 г · моль -1 |
| Плотность | 2,217 г / л [1] |
| Температура плавления | -175 ° С (-283,0 ° F, 98,1 К) |
| Точка кипения | -46 ° С (-51 ° F, 227 К) |
| Термохимия | |
Std энтальпия формации (Δ F H ⦵ 298 ) | +10,46 кДж / моль |
| Опасности | |
| Основные опасности | Взрывоопасный газ |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
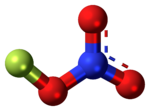
Нитрат фтора - нестабильное производное азотной кислоты с формулой FNO
3. Он чувствителен к ударам. [1] Из-за его нестабильности, его часто производят из нитрата хлора по мере необходимости [ цитата необходима ] .
Синтез и свойства [ править ]
Нитрат фтора образуется, когда газообразный фтор барботируют через азотную кислоту или реагируют с твердым нитратом калия : [2]
- F
2 + HNO
3 → FNO
3 + ВЧ
- F
2 + KNO
3 → FNO
3 + KF
Он разлагается в воде с образованием кислорода газа, дифторидом кислорода , фтористоводородной кислотой и азотной кислотой. [1]
Ссылки [ править ]
- ^ a b c Ерш, Отто; Квасник, Вальтер (1935). «Фторирование азотной кислоты. Нитроксифторид NO 3 F». Angewandte Chemie . 48 : 238–240. DOI : 10.1002 / ange.19350481604 .
- ^ Йост, Дон М .; Бирбауэр, Алан. «Реакция фтора с азотной кислотой и твердым нитратом калия с образованием NO 3 F». Коммуникация. Cite journal requires
|journal=(help)
- Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8.
| HNO 3 | Он | ||||||||||||||||
| LiNO 3 | Быть (NO 3 ) 2 | B (НЕТ3)- 4 | RONO 2 | НЕТ- 3 NH 4 NO 3 | HOONO 2 | FNO 3 | Ne | ||||||||||
| NaNO 3 | Mg (NO 3 ) 2 | Al (NO 3 ) 3 | Si | п | S | ClONO 2 | Ar | ||||||||||
| KNO 3 | Ca (NO 3 ) 2 | СБН (№ 3 ) 3 | Ti (NO 3 ) 4 | VO (NO 3 ) 3 | Cr (NO 3 ) 3 | Mn (NO 3 ) 2 | Fe (NO 3 ) 2 Fe (NO 3 ) 3 | Co (NO 3 ) 2 Co (NO 3 ) 3 | Ni (NO 3 ) 2 | CuNO 3 Cu (NO 3 ) 2 | Zn (NO 3 ) 2 | Ga (NO 3 ) 3 | Ge | В качестве | Se | Br | Kr |
| RbNO 3 | Sr (NO 3 ) 2 | Д (НЕТ 3 ) 3 | Zr (NO 3 ) 4 | Nb | Пн | Tc | Ru (NO 3 ) 3 | Rh (NO 3 ) 3 | Pd (NO 3 ) 2 Pd (NO 3 ) 4 | AgNO 3 Ag (NO 3 ) 2 | Cd (NO 3 ) 2 | В (NO 3 ) 3 | Sn | Сб (NO 3 ) 3 | Te | INO 3 | Xe (NO 3 ) 2 |
| CsNO 3 | Ba (NO 3 ) 2 | Hf (NO 3 ) 4 | Та | W | Re | Операционные системы | Ir | Pt (NO 3 ) 2 Pt (NO 3 ) 4 | Au (NO 3 ) 3 | Hg 2 (NO 3 ) 2 Hg (NO 3 ) 2 | TlNO 3 Tl (NO 3 ) 3 | Pb (NO 3 ) 2 | Би (NO 3 ) 3 BiO (NO 3 ) | Po (NO 3 ) 4 | В | Rn | |
| Пт № 3 | Ра (NO 3 ) 2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ц | Og | |
| ↓ | |||||||||||||||||
| Ла (NO 3 ) 3 | Ce (NO 3 ) 3 Ce (NO 3 ) 4 | Pr (NO 3 ) 3 | Nd (NO 3 ) 3 | PM (NO 3 ) 3 | См (NO 3 ) 3 | Eu (NO 3 ) 3 | Б-г (NO 3 ) 3 | Tb (NO 3 ) 3 | Dy (NO 3 ) 3 | Хо (нет 3 ) 3 | Er (NO 3 ) 3 | Тм (№ 3 ) 3 | Yb (NO 3 ) 3 | Лу (NO 3 ) 3 | |||
| Ac (NO 3 ) 3 | Чт (NO 3 ) 4 | PaO 2 (NO 3 ) 3 | UO 2 (NO 3 ) 2 | Np (NO 3 ) 4 | Pu (NO 3 ) 4 | Am (NO 3 ) 3 | См (NO 3 ) 3 | Bk | Cf | Es | FM | Мкр | Нет | Lr | |||
| Этот материал, связанный с неорганическими соединениями, является незавершенным . Вы можете помочь Википедии, расширив ее . |