| Стрептококковая инфекция группы B | |
|---|---|
| Другие имена | Стрептококковая инфекция группы B |
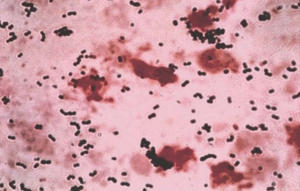 | |
| Streptococcus agalactiae - окраска по Граму | |
| Специальность | Педиатрия |
Группа B стрептококковой инфекции , также известный как группы B стрептококковой болезни или просто группы B стрептококк , [1] является инфекция , вызванная бактерией стрептококки группы в ( S. agalactiae ) (также известный как группы В стрептококк или GBS). Инфекция GBS может вызвать серьезное заболевание, а иногда и смерть, особенно у новорожденных, пожилых людей и людей с ослабленной иммунной системой .
В качестве других вирулентных бактерий, ГБС таит в себе важный ряд факторов вирулентности , [2] , наиболее важными из них являются капсульный полисахарид (богаты сиаловой кислоты ), а также порообразующего токсина , β- гемолизин . [3] [4] Капсула GBS, вероятно, является ключевым фактором вирулентности, потому что она помогает GBS ускользать от защитных механизмов хозяина, мешающих фагоцитарному уничтожению GBS фагоцитами человека . [5] [3] β-гемолизин GBS считается почти идентичным пигменту GBS ( гранадаен ). [6] [7] [8] [9]
СГБ был признан патогеном крупного рогатого скота Эдмондом Нокаром и Моллеро в конце 1880-х годов. Это может привести к бычьего мастит ( воспаление в вымени ) в молочных коров. Название вида «agalactiae», что означает «без молока», намекает на это. [10]
Его значение как патогена для человека было впервые описано в 1938 году, когда Фрай сообщил о трех смертельных случаях послеродовых инфекций, вызванных СГБ. [11] В начале 1960-х годов СГБ был признан основной причиной инфекций у новорожденных. [12]
В целом, GBS представляет собой безвредную комменсальную бактерию, являющуюся частью микробиоты человека, колонизирующей желудочно-кишечные и мочеполовые тракты до 30% здоровых взрослых людей ( бессимптомные носители ). [13] [14] [5]
Идентификация лаборатории [ править ]
Как уже упоминалось, S. agalactiae - это грамположительный кокк со склонностью к образованию цепочек, бета-гемолитический, каталазонегативный и факультативный анаэроб. GBS легко растет на чашках с кровяным агаром в виде микробных колоний, окруженных узкой зоной β- гемолиза . GBS характеризуется наличием в клеточной стенке антигена группы B по классификации Lancefield (группа Lancefield ), который может быть обнаружен непосредственно у интактных бактерий с помощью тестов латексной агглютинации. [15] [16] Тест CAMPтакже является еще одним важным тестом для выявления GBS. Фактор САМР действует синергетически со стафилококковым β-гемолизином, вызывая усиленный гемолиз эритроцитов овцы или крупного рогатого скота . [15]
GBS также способен гидролизовать гиппурат , и этот тест также может использоваться для идентификации GBS. Гемолитические штаммы GBS продуцируют оранжево-кирпично-красный неизопреноидный полиеновый пигмент (орнитинрхамнододекаен) ( гранадаен ) при культивировании на среде гранада, что позволяет его легко идентифицировать. [17]
Идентификация GBS также может быть легко проведена с использованием современных методов, таких как масс-спектрометрия с лазерной десорбцией и времяпролетной ионизацией с использованием матрицы ( MALDI-TOF ) . [18] [19]
Кроме того, колонии GBS могут быть предварительно идентифицированы после их появления в среде хромогенного агара. [16] [20] [21] Тем не менее, GBS-подобные колонии, которые развиваются в хромогенных средах, должны быть подтверждены как GBS с помощью дополнительных надежных тестов (например, агглютинация латекса или тест CAMP), чтобы избежать потенциальной неправильной идентификации. [16] Краткое описание лабораторных методов идентификации GBS приведено в ссылке 18. [16]
Колонизация против инфекции [ править ]
СГБ обнаруживается в желудочно-кишечном и мочеполовом трактах человека и является нормальным компонентом кишечной и вагинальной микробиоты у некоторых женщин. [22] В различных исследованиях уровень вагинальной колонизации GBS колеблется от 4 до 36%, при этом в большинстве исследований сообщается о показателях более 20%. Колонизация влагалища или прямой кишки может быть прерывистой, преходящей или постоянной. [22] Эти различия в сообщаемой распространенности бессимптомной (без симптомов болезни) колонизации могут быть связаны с различными используемыми методами обнаружения и различиями в изученных популяциях. [23] [24] [20]
Хотя GBS является бессимптомным и безвредным колонизатором желудочно-кишечного тракта человека у 30% здоровых взрослых людей, включая беременных женщин [5] [23], эта условно-патогенная безвредная бактерия в некоторых случаях может вызывать тяжелые инвазивные инфекции. [14]
Беременность [ править ]
Хотя колонизация GBS протекает бессимптомно и, как правило, не вызывает проблем, иногда она может вызвать серьезные заболевания у матери и ребенка во время беременности и после родов. Инфекции GBS у матери могут вызывать хориоамнионит (внутриамниотическую инфекцию или тяжелую инфекцию плацентарных тканей), нечасто, послеродовые инфекции (после рождения), и это было связано с недоношенностью и гибелью плода. [25] Инфекции мочевыводящих путей, связанные с СГБ, могут вызывать роды у беременных женщин и вызывать преждевременные роды ( преждевременные роды ) и выкидыш . [5] [26]
Новорожденные [ править ]
В западном мире СГБ (при отсутствии эффективных мер профилактики) является основной причиной бактериальных инфекций у новорожденных, таких как сепсис , пневмония и менингит , которые могут привести к смерти или долгосрочным последствиям . [5] [27]
Инфекции GBS у новорожденных подразделяются на два клинических типа: болезнь с ранним началом (GBS-EOD) и болезнь с поздним началом (GBS-LOD). GBS-EOD проявляется у новорожденного от 0 до 7 дней жизни, в большинстве случаев EOD проявляется в течение 24 часов с момента рождения. GBS-LOD начинается от 7 до 90 дней после рождения. [5] [20]
Наиболее частыми клиническими синдромами GBS-EOD являются сепсис без видимой локализации, пневмония и, реже, менингит. Бактериемия без очага встречается в 80-85%, пневмония - в 10-15%, менингит - в 5-10% случаев. Первоначальные клинические признаки являются респираторными симптомами более чем в 80% случаев. Новорожденные с менингитом часто имеют начальную клиническую картину, идентичную таковой у новорожденных без менингеального поражения. Чтобы исключить менингит, часто необходимо исследование спинномозговой жидкости . [5] [28] [29]
Колонизация GBS во время родов является основным фактором риска развития GBS-EOD. GBS-EOD приобретается вертикально ( вертикальная передача ), в результате воздействия GBS на плод или ребенка из влагалища колонизированной женщины либо внутриутробно (из-за восходящей инфекции), либо во время родов, после разрыва плодных оболочек. Младенцы также могут быть инфицированы во время прохождения через родовые пути, тем не менее, новорожденные, которые приобретают GBS через этот путь, могут стать только колонизированными, и у этих колонизированных младенцев обычно не развивается GBS-EOD. [ необходима цитата ]
Примерно 50% новорожденных от матерей, колонизированных GBS, также являются колонизированными GBS, и (без мер профилактики) у 1-2% этих новорожденных разовьется GBS-EOD. [30]
Хотя материнская колонизация GBS является ключевым фактором для GBS-EOD, другие факторы также увеличивают риск. Вот эти факторы: [5] [20]
- Начало родов до 37 недель беременности ( преждевременные роды )
- Длительный разрыв плодных оболочек (большая продолжительность разрыва мембран) (≥18 ч до родов)
- GBS бактериурии во время беременности
- Внутриродовая (во время родов) лихорадка (> 38 ° C,> 100,4 ° F)
- Амниотические инфекции (хориоамнионит)
- Молодой возраст матери
- Материнская ВИЧ-инфекция [31]
Тем не менее, большинство детей, у которых развивается GBS-EOD, рождаются от колонизированных матерей без каких-либо из этих факторов риска. [20] Тяжелая вагинальная колонизация GBS также связана с более высоким риском GBS-EOD. Женщины, у которых был один из этих факторов риска, но которые не были колонизированы GBS во время родов, имеют низкий риск GBS-EOD по сравнению с женщинами, которые были колонизированы пренатально, но не имели ни одного из вышеупомянутых факторов риска. [30]
Наличие низких уровней антикапсулярных антител против GBS у матери также имеет большое значение для развития GBS-EOD. [32] [33] Из-за этого предыдущий брат или сестра с GBS-EOD также является важным фактором риска развития инфекции при последующих родах, что, вероятно, отражает отсутствие защитных антител у матери.[20]
В целом, показатели летальности от GBS-EOD снизились с 50%, наблюдавшихся в исследованиях 1970-х годов, до 2–10% в последние годы, главным образом в результате улучшений в терапии и лечении. Смертельные неонатальные инфекции, вызванные СГБ, чаще встречаются среди недоношенных детей.[5] [20] [34]
GBS-LOD поражает младенцев в возрасте от 7 дней до 3 месяцев и имеет более низкий уровень летальности (1-6%), чем GBS-EOD. Клинические синдромы GBS-LOD - это бактериемия без очага (65%), менингит (25%), целлюлит , остеоартрит и пневмония. Сообщается, что недоношенность является основным фактором риска. Каждая неделя уменьшения гестации увеличивает риск развития GBS-LOD в 1,34 раза. [35]
GBS-LOD не передается посредством вертикальной передачи во время доставки; он может быть передан позже от матери с грудным молоком или из источников окружающей среды и населения. GBS-LOD обычно проявляет неспецифические признаки, и диагноз следует ставить путем посева крови у новорожденных с лихорадкой. Неонатальный менингит, вызванный S.agalactiae , не сопровождается характерным признаком менингита взрослых - ригидностью шеи; скорее, он проявляется неспецифическими симптомами, такими как лихорадка, рвота и раздражительность, и, следовательно, может привести к позднему диагнозу. Потеря слуха и психические нарушения могут быть долгосрочными последствиями менингита, вызванного СГБ. [5] [27]
Профилактика неонатальной инфекции [ править ]
В настоящее время единственным надежным способом предотвращения GBS-EOD является время родов профилактика антибиотиками (IAP) - введение внутривенных (IV) антибиотиков во время родов. Доказано, что внутривенное введение пенициллина или ампициллина в начале родов, а затем снова каждые четыре часа до родов женщинам, колонизировавшим GBS, очень эффективно предотвращает вертикальную передачу GBS от матери к ребенку и GBS-EOD (пенициллин G, 5 миллионов единиц Начальная доза внутривенно, затем 3 миллиона единиц [22] каждые 4 часа до родов или ампициллин, 2 г начальная доза внутривенно, затем 1 г внутривенно каждые 4 часа до родов). [5] [20] [22]
Женщины с аллергией на пенициллин без анафилаксии ( ангионевротический отек , респираторный дистресс или крапивница ) после введения пенициллина или цефалоспорина (низкий риск анафилаксии) могли получать цефазолин (начальная доза 2 г внутривенно, затем 1 г внутривенно каждые 8 часов до доставка) вместо пенициллина или ампициллина. [20] Клиндамицин (900 мг внутривенно каждые 8 часов до родов), эритромицин сегодня не рекомендуются из-за высокой доли устойчивости GBS к эритромицину (до 44,8%), [20] [22]
Ни пероральные, ни внутримышечные антибиотики не эффективны для снижения риска GBS-EOD. [22]
Тестирование чувствительности к антибиотикам изолятов СГБ имеет решающее значение для надлежащего выбора антибиотиков для ВБД у женщин с аллергией на пенициллин, поскольку среди изолятов СГБ растет устойчивость к клиндамицину, наиболее часто используемому агенту (у женщин с аллергией на пенициллин). Соответствующие методики тестирования важны, потому что устойчивость к клиндамицину (устойчивость к противомикробным препаратам ) может возникать у некоторых штаммов GBS, которые оказываются чувствительными ( чувствительность к антибиотикам ) в определенных тестах на чувствительность. [20]
Для женщин, которые подвергаются риску анафилаксии после воздействия пенициллина, в лабораторных условиях должно быть четко указано наличие аллергии на пенициллин, чтобы гарантировать, что лаборатория осведомлена о необходимости тестирования изолятов GBS на чувствительность к клиндамицину. Ванкомицин (20 мг / кг каждые 8 часов до родов) [22] используется для предотвращения GBS-EOD у младенцев, рожденных от матерей с аллергией на пенициллин. [20] [22]
Если соответствующий IAP у женщин с колонией GBS начинается как минимум за 2 часа до родов, риск неонатальной инфекции также каким-то образом снижается. [36] [37] [38]
Истинная аллергия на пенициллин встречается редко, частота анафилаксии составляет от одного до пяти эпизодов на 10 000 случаев терапии пенициллином. [39] Пенициллин, назначенный женщине, не страдающей аллергией на β-лактам, имеет риск анафилаксии от 0,04 до 4 на 100 000 человек. Материнская анафилаксия, связанная с GBS IAP, имеет место, но любая заболеваемость, связанная с анафилаксией, в значительной степени компенсируется снижением частоты GBS-EOD. [20]
Считается, что IAP связаны с появлением резистентных штаммов бактерий и с увеличением частоты инфекций с ранним началом, вызванных другими патогенами, в основном грамотрицательными бактериями, такими как Escherichia coli . Тем не менее, в большинстве исследований не было обнаружено увеличения частоты сепсиса с ранним началом, не связанного с СГБ, связанного с широким использованием IAP.[20] [40] [41] [42]
Были изучены другие стратегии предотвращения GBS-EOD, и было предложено очищение влагалища во время родов хлоргексидином, чтобы помочь предотвратить GBS-EOD, тем не менее, не было представлено доказательств эффективности этого подхода. [20] [22] [43] [44]
Определение кандидатов для получения IAP [ править ]
Для отбора кандидатов-женщин в МАП используются два способа: метод отбора на основе культуры и подход, основанный на оценке риска. [45] Подход к скринингу на основе посевов позволяет выявить кандидатов с использованием посевов из влагалища и прямой кишки, полученных между 35 и 37 неделями беременности (или 36-37 [22] ), и всем женщинам, колонизировавшим GBS, назначают IAP. Стратегия, основанная на оценке риска, определяет кандидатов на получение IAP с учетом вышеупомянутых факторов риска, которые, как известно, увеличивают вероятность GBS-EOD, без учета того, является ли мать носителем GBS или нет. [5] [20] [46]
IAP также рекомендуется женщинам с факторами риска во время родов, если их статус носителя GBS неизвестен во время родов, а также женщинам с бактериурией GBS во время беременности, а также женщинам, у которых ранее был ребенок с GBS-EOD. Подход, основанный на оценке риска, в целом менее эффективен, чем подход, основанный на культуре [47], потому что в большинстве случаев GBS-EOD развивается среди новорожденных, рожденных от матерей без факторов риска. [20] [30] [48]
ВБД не требуется женщинам, перенесшим плановое кесарево сечение при отсутствии родов и с неповрежденными плодными оболочками, независимо от носительства СГБ. [20] [22]
Регулярный скрининг беременных женщин проводится в большинстве развитых стран, таких как США, Франция, Испания, Бельгия, Канада и Австралия, и данные показали снижение заболеваемости GBS-EOD после введения основанных на скрининге мер для предотвращения GBS- EOD. [24] [48] [49]
Стратегия, основанная на оценке риска, пропагандируется, среди других стран, в Великобритании, Нидерландах, Новой Зеландии и Аргентине. [24]
Вопрос рентабельности обеих стратегий определения кандидатов на IAP менее ясен, и некоторые исследования показали, что тестирование женщин с низким риском, плюс IAP, назначаемое женщинам с высоким риском, и тем, у кого установлено наличие GBS, обходится дороже. - эффективнее, чем нынешняя практика Великобритании. [50] Другие оценки также показали, что подход, основанный на культуре, более рентабелен, чем подход, основанный на оценке риска, для предотвращения GBS-EOD. [51] [52]
Также было предложено тестирование беременных женщин для выявления носителей СГБ, а проведение IAP для носителей СГБ и женщин из группы высокого риска значительно более рентабельно, чем использование подхода, основанного на факторах риска. В одном из исследований была подсчитана ожидаемая чистая выгода для правительства Великобритании от такого подхода в размере около 37 миллионов фунтов стерлингов в год по сравнению с текущим подходом RCOG . [50] [51]
Сообщалось, что IAP не предотвращает всех случаев GBS-EOD; его эффективность оценивается в 80%. Стратегия профилактики, основанная на оценке риска, не предотвращает около 33% случаев без факторов риска. [53]
До 90% случаев GBS-EOD можно было бы предотвратить, если бы IAP предлагался всем носителям GBS, выявленным в результате всеобщего скрининга на поздних сроках беременности, а также матерям из групп повышенного риска. [54]
Если перед родами вводится недостаточное количество внутривенных антибиотиков, ребенку могут быть назначены антибиотики сразу после рождения, хотя данные неубедительны в отношении того, является ли эта практика эффективной или нет. [20] [55] [56] [57]
Домашние роды и водные роды [ править ]
Домашние роды становятся все более популярными в Великобритании. Рекомендации по профилактике инфекций, вызываемых СГБ, у новорожденных такие же, как при домашних родах, так и при родах в больнице. Около 25% женщин, рожающих дома, вероятно, несут СГБ во влагалище во время родов, не зная об этом, и может быть трудно правильно следовать рекомендациям IAP и справляться с риском тяжелой аллергической реакции на антибиотики вне стационара. . [58]
Руководства RCOG и ACOG предполагают, что роды в бассейне не противопоказаны носителям GBS, которым был предложен соответствующий IAP, если нет других противопоказаний к погружению в воду [22] [59]
Проверка на колонизацию [ править ]
Примерно 10–30% женщин колонизируют СГБ во время беременности. Тем не менее во время беременности колонизация может быть временной, прерывистой или постоянной. [20] Поскольку статус колонизации GBS у женщин может измениться во время беременности, только посевы, проведенные за ≤5 недель до родов, достаточно точно предсказывают статус носителя GBS при родах. [60] Напротив, если пренатальный посев проводится более чем за 5 недель до родов, это ненадежно для точного прогнозирования статуса носителя GBS при родах. По этой причине CDC рекомендует тестирование на колонизацию GBS у беременных женщин на сроке 35–37 недель беременности. [20] [61] Важно отметить, что ACOGтеперь рекомендует проводить универсальный скрининг СГБ между 36 и 37 неделями беременности. Эта новая рекомендация предусматривает 5-недельное окно для достоверных результатов посева, которое включает роды, которые произошли до гестационного возраста не менее 41 недели. [22]
Клинические образцы, рекомендуемые для посева GBS, представляют собой мазки, взятые из нижней части влагалища и прямой кишки через наружный анальный сфинктер . Образец следует собирать с помощью мазка из нижней части влагалища (вагинального входа), а затем из прямой кишки (т. Е. Путем введения мазка через анальный сфинктер), используя тот же мазок или два разных мазка. Цервикальные, перианальные, периректальные или промежностные образцы не принимаются, и для взятия образцов не следует использовать зеркало . [20] Образцы могут быть взяты медицинскими работниками или самой матерью с соответствующими инструкциями. [62] [63] [64]
Следуя рекомендациям CDC, эти тампоны следует помещать в непитательную транспортную среду. По возможности образцы следует охладить и как можно скорее отправить в лабораторию. [20] Соответствующие транспортные системы коммерчески доступны, и в этих транспортных средах GBS может оставаться жизнеспособным в течение нескольких дней при комнатной температуре. Однако выздоровление GBS замедляется в течение одного-четырех дней, особенно при повышенных температурах, что может привести к ложноотрицательным результатам. [20] [65]
Методы культуры [ править ]
Образцы (вагинальные, ректальные или вагиноректальные мазки) должны быть внесены в селективный обогащенный бульон ( бульон Тодда Хьюитта с селективными антибиотиками, обогащенная культура). Это включает выращивание образцов в обогащенной среде для повышения жизнеспособности GBS и одновременного нарушения роста других естественных бактерий. После инкубации (18–24 часа, 35–37 ° C) обогащенный бульон субкультивируют на чашки с кровяным агаром, и GBS-подобные колонии идентифицируются с помощью теста CAMP или с использованием латексной агглютинации с антисывороткой GBS. [20] [66] В Великобритании этот метод описан в Стандартах Великобритании для микробиологических исследований Министерства здравоохранения Великобритании [67]
После инкубации обогащающий бульон также можно пересеять на агар со средой гранады, где GBS растет в виде розовато-красных колоний [16] [17] [66] [68] [69], или на хромогенный агар, где GBS растет в виде окрашенных колоний. [20] Тем не менее, GBS-подобные колонии, которые развиваются в хромогенной среде, должны быть подтверждены как GBS с помощью дополнительных надежных тестов, чтобы избежать неправильной идентификации. [16]
Также возможен посев непосредственно из вагинальных и ректальных мазков или вагиноректальных мазков в чашку с подходящей культуральной средой (кровяной агар, среда гранада или хромогенная среда). Однако этот метод (минуя этап селективного обогащения бульона) может привести к некоторым ложноотрицательным результатам, и этот подход следует применять только в дополнение, а не вместо инокуляции в селективный бульон. [20]
Сегодня в Великобритании обнаружение колонизации GBS с использованием метода обогащающего бульона не предлагается в большинстве лабораторий, обслуживающих NHS. Однако реализация этого теста кажется жизнеспособным вариантом. В настоящее время посев на GBS (с использованием обогащенной питательной среды) на сроке 35–37 недель для определения группы женщин, подверженных риску, представляется наиболее рентабельной стратегией. [51] [52]
Благотворительная организация Группы B Strep поддержка опубликовала список больниц в Великобритании , которые предлагают обнаружение GBS с использованием методы обогащения бульонной культуры (обогащение культуральной среды, ECM). [70] Этот тест также доступен в частном порядке по цене от 35 фунтов стерлингов за тест за набор для домашнего тестирования, и его предлагают частные клиники. [70] Тест также доступен в частном порядке для почтовой службы Великобритании. [71] [72]
Тестирование на месте [ править ]
Ни один из текущих тестов на основе культуры не является достаточно точным и достаточно быстрым, чтобы его рекомендовали для выявления GBS после начала родов. Для посева образцов тампона требуется время для роста бактерий, а это означает, что его нельзя использовать в качестве теста в месте оказания медицинской помощи во время родов . [ необходима цитата ]
Быстро были разработаны альтернативные методы обнаружения GBS в клинических образцах (например, вагиноректальные мазки), такие как методы, основанные на тестах амплификации нуклеиновых кислот , такие как тесты полимеразной цепной реакции (ПЦР), и зонды гибридизации ДНК . Эти тесты также можно использовать для обнаружения GBS непосредственно из бульонной среды после стадии обогащения, избегая пересева инкубированного обогащающего бульона на подходящую чашку с агаром. [16] [20] [73]
Тестирование женщин на колонизацию СГБ с помощью вагинальных или ректальных мазков на 35–37 неделе беременности и их культивирование в обогащенной среде не так быстро, как тест ПЦР, который проверяет, есть ли у беременной женщины СГБ при родах. ПЦР-тесты позволят начать IAP при поступлении в родильное отделение тем женщинам, для которых неизвестно, являются ли они носителями СГБ. [20] ПЦР-тест на носительство GBS в будущем может быть достаточно точным, чтобы определять IAP. Однако технология ПЦР для обнаружения GBS должна быть улучшена и упрощена, чтобы сделать метод рентабельным и полностью полезным в качестве теста на месте . Эти тесты по-прежнему не могут заменить дородовой посев для точного выявления GBS. [20] [22] [74]Тем не менее, тестирование в месте оказания медицинской помощи может использоваться для рожениц с неизвестным статусом СГБ и без факторов риска для подтверждения использования IAP. [22]
Упущенные возможности предотвращения [ править ]
Важными факторами для успешной профилактики GBS-EOD с использованием IAP и универсального подхода к скринингу являются: [ необходима ссылка ]
- Охватите большинство беременных женщин для дородовых обследований
- Правильный сбор образцов
- Использование соответствующей процедуры для обнаружения GBS
- Администрирование правильного IAP для операторов GBS
Большинство случаев GBS-EOD встречается у доношенных детей, рожденных от матерей, которые не прошли скрининг на колонизацию GBS, и у недоношенных детей, рожденных от матерей, которые не проходили скрининг, хотя некоторые ложноотрицательные результаты, наблюдаемые в скрининговых тестах GBS, могут быть связаны с ограничениями теста. и к приобретению GBS между моментом проверки и доставки. Эти данные показывают, что в некоторых условиях все еще необходимы улучшения в методах сбора и обработки образцов для выявления GBS. Ложноотрицательный скрининговый тест, а также невозможность получить IAP у женщин, родивших недоношенных с неизвестным статусом колонизации GBS, и назначение несоответствующих агентов IAP женщинам с аллергией на пенициллин составляют большинство упущенных возможностей для предотвращения случаев GBS-EOD. [ необходима цитата ]
Инфекции GBS-EOD, обнаруженные у младенцев, матери которых были проверены как отрицательные по культуре GBS, вызывают особую тревогу и могут быть вызваны неправильным сбором образцов, задержкой в обработке образцов, неправильными лабораторными методами, недавним использованием антибиотиков или колонизацией GBS после скрининга. было проведено. [48] [75] [76] [77] [78]
Эпидемиология [ править ]
В 2000–2001 гг. Сообщенная общая частота инфицирования GBS среди новорожденных в Великобритании составляла 0,72 на 1000 живорождений, 0,47 на 1000 для GBS-EOD и 0,25 на 1000 для GBS-LOD. Наблюдались очень заметные колебания: заболеваемость в Шотландии составила 0,42 на 1000 живорождений, а в Северной Ирландии - 0,9 на 1000 живорождений.[79] [80]
Тем не менее, это может быть серьезной недооценкой реальной заболеваемости GBS-инфекцией у новорожденных. Правдоподобным объяснением этого является то, что у значительного числа младенцев с вероятным GBS-EOD были отрицательные посевы в результате предыдущего лечения матери антибиотиками, которое подавляет рост GBS в крови и культурах спинномозговой жидкости, но не маскирует клинические симптомы. [81] [82]
Данные, собранные проспективно для новорожденных, которым потребовалось обследование на сепсис в первые 72 часа жизни в Великобритании, показали, что комбинированная частота определенной и вероятной инфекции GBS-EOD составляет 3,6 на 1000 живорождений. [83] Другое исследование эпидемиологии инвазивных инфекций СГБ в Англии и Уэльсе сообщило о росте заболеваемости СГБ-EOD в период с 2000 по 2010 год с 0,28 до 0,41 на 1000 живорождений. Показатели GBS-LOD также увеличились в период с 1991 по 2010 год с 0,11 до 0,29 на 1000 живорождений в Англии и Уэльсе. [84]
В прошлом заболеваемость GBS-EOD колебалась от 0,7 до 3,7 на тысячу живорождений в США [5] и от 0,2 до 3,25 на тысячу в Европе. [24] В 2008 году, после широкого использования дородового скрининга и антибиотикопрофилактики во время родов , Центры по контролю и профилактике заболеваний в США сообщили о частоте 0,28 случая GBS-EOD на тысячу живорождений в США. [85] С 2006 по 2015 год заболеваемость GBS EOD снизилась до 0,37–0,23 на тысячу живорождений в США. [86] Напротив, заболеваемость GBS-LOD в США осталась неизменной и составила 0,26-0,31 на 1000 живорождений. [86] [87]
В Испании заболеваемость СГБ-вертикальным сепсисом снизилась на 73,6%, с 1,25 на 1000 живорождений в 1996 году до 0,33 на 1000 в 2008 году. [88] В районе Барселоны с 2004 по 2010 год заболеваемость СГБ-EOD составляла 0,29 на человека. тысяч живых новорожденных, без существенных различий по годам. Летальность составила 8,16%. [48] [89]
Во Франции с 2001 г. также сообщалось о быстром снижении заболеваемости неонатальными инфекциями СГБ после широкого использования IAP, с 0,7 до 0,2 на 1000 рождений в период с 1997 по 2006 гг. [90]
С 2012 года частота неонатальной инфекции GBS оценивается в 0,53 на 1000 рождений в Европейском регионе, 0,67 в Америке и 0,15 в Австралазии. В странах, сообщивших об отсутствии использования IAP, заболеваемость GBS-EOD была в 2,2 раза выше, чем в странах, сообщивших об использовании IAP. [34] [80]
Было подсчитано, что инфекции GBS являются причиной не менее 409 000 случаев заболевания матерей / плода / младенцев и 147 000 мертворождений и младенческих смертей во всем мире ежегодно. [91]
Ниже приведены оценки шансов, что ребенок заразится неонатальной инфекцией, вызываемой СГБ, если не будут приняты профилактические меры и отсутствуют другие факторы риска: [92]
- Одна из 1000, где женщина не является носителем СГБ.
- Одна из 400 женщин с СГБ во время беременности
- Одно из 300 случаев, когда женщина носит СГБ при родах
- Один из 100 случаев, когда у женщины был предыдущий ребенок, инфицированный СГБ
Если женщине-носителю СГБ назначают ВБП во время родов, риск для ребенка значительно снижается:
- Один из 8000 случаев, когда мать носит СГБ во время беременности;
- Один из 6000, когда мать носит GBS при родах; и
- Один из 2200 случаев, когда у матери ранее был ребенок, инфицированный СГБ.
Рекомендации [ править ]
Соединенное Королевство [ править ]
Королевский колледж акушеров и гинекологов (RCOG) [ править ]
Королевский колледж акушеров и гинекологов (RCOG) выпустили своего зеленый Top Указание № 36 «Профилактика раннего начала неонатальных стрептококков группы заболеваний» в 2003 году руководство четко указано: «Рутинное бактериологическое обследование всех беременных женщин для дородовой GBS перевозки не рекомендуется, и вагинальные мазки не следует брать во время беременности, если для этого нет клинических показаний ». Но, «следует предложить антибиотикопрофилактику во время родов, если при текущей беременности в вагинальном мазке обнаружен СГБ». [ необходима цитата ]
Тем не менее, в этом руководстве используются данные о минимальной заболеваемости из исследования, проведенного в 2000–2001 гг. [93], поэтому оно могло не только недооценивать истинную заболеваемость СГБ, но и недооценивать риски заражения СГБ для младенцев. Инфекция GBS у младенцев увеличилась в Англии, Уэльсе и Северной Ирландии с 2003 г. (когда было введено руководство). Добровольно зарегистрированные случаи из Отчета об инфекционных заболеваниях / Агентства по охране здоровья показывают 0,48 случая на 1000 живорождений в 2003 году, а в 2009 году этот показатель увеличился до 0,64 на 1000 живорождений. [94]
В 2007 году RCOG опубликовала результаты своего аудита, чтобы оценить практику акушерских отделений Великобритании в соответствии с их рекомендациями. [95] Аудит начался со сравнения международных рекомендаций по профилактике GBS-EOD: подчеркивая тот факт, что, в отличие от руководящих принципов Великобритании и Новой Зеландии, большинство других стран рекомендовали выявлять женщин на ВБД, предлагая эффективные тесты всем беременным. женщины. В ходе аудита были изучены протоколы больниц против инфицирования GBS новорожденных. Из 161 британского подразделения, представившего свой протокол, четыре подразделения даже не имели протокола для GBS, из них 35% не упомянули руководство RCOG 2003 года, и только у меньшинства подразделений были протоколы, полностью соответствующие руководству. . [ необходима цитата ]
Дальнейшее британское исследование, опубликованное в 2010 году, рассматривало возможности предотвращения GBS-EOD после введения руководства RCOG. Они обнаружили, что в 48 случаях СГБ в период с 2004 по 2007 год (0,52 на 1000 живорождений) только 19% матерей, у которых присутствовали факторы риска, получали адекватный IAP. Исследователи заявили: «Если бы все женщины с факторами риска получали профилактику, можно было бы предотвратить 23 случая (48%)». [53]
Руководство RCOG от 2003 г. было пересмотрено в июле 2012 г., но существенных изменений внесено не было. Наиболее заметным изменением является уточнение процедуры, когда у женщины-носителя GBS есть PROM, и разъяснение, что пероральные антибиотики не рекомендуются во время родов против инфекции GBS у ребенка. [ необходима цитата ]
В обзоре также было рассмотрено распространенное заблуждение относительно чистки влагалища, согласно которому нет доказательств того, что эта процедура может уменьшить инфекцию GBS у ребенка. Новые доказательства и рекомендации в этой области были рассмотрены RCOG в 2014 году, и было решено, что пересмотр руководства будет отложен на более поздний срок, а тем временем версия, доступная на веб-сайте, будет оставаться в силе до замены. [ необходима цитата ]
Опубликован второй и заключительный аудиторский отчет GBS (Аудит текущей практики предотвращения EOD GBS в Великобритании). В результате аудита RCOG рекомендовала обновить национальные рекомендации по предотвращению заражения GBS у новорожденных. [96]
В Великобритании RCOG по- прежнему не рекомендует бактериологический скрининг беременных на предмет дородового носительства СГБ в своих пересмотренных новых рекомендациях. [59] Тем не менее, утверждается, что если носительство GBS обнаруживается случайно или намеренно, женщинам следует предложить IAP. И чтобы всем беременным женщинам была предоставлена соответствующая информационная брошюра о СГБ и беременности (опубликована в декабре 2017 года). [97]Вместо этого к женщинам обращаются с учетом риска родов. IAP назначают женщинам, у которых в моче или вагинальных / ректальных мазках, взятых во время беременности, был обнаружен СГБ, а также женщинам, у которых ранее был ребенок с СГБ. Немедленное индукцию родов и ВБД следует предлагать всем женщинам с предродовым разрывом плодных оболочек на 37 неделе беременности и более, женщинам, у которых разрыв плодных оболочек превышает 18 часов, и тем, у кого во время родов наблюдается высокая температура.
Женщинам, страдающим гипертермией в родах, следует предлагать антибиотики широкого спектра действия, включая антибиотик, подходящий для предотвращения EOD-GBS. [59]
В Великобритании также было предложено следующее: «Для женщин, которые, как известно, носят СГБ, когда не ожидается, что внутривенные антибиотики можно вводить как минимум за 4 часа до родов, - внутримышечная инъекция 4,8 МЕ (2,9 г) пенициллина. G примерно на 35 неделе беременности может быть полезен в дополнение к внутривенным антибиотикам, вводимым с начала родов или разрыву плодных оболочек до родов, чтобы попытаться искоренить носительство GBS до родов ».[98] Однако эта рекомендация НЕ ПОДДЕРЖИВАЕТСЯ ни одним из настоящих руководств. [20] [22] [59]
Рекомендации NICE [ править ]
Национальный институт здравоохранения и качества ухода Великобритании (NICE) не рекомендует рутинное тестирование на СГБ, заявляя: «Беременным женщинам не следует предлагать рутинный дородовой скрининг на стрептококк группы B, поскольку доказательства его клинической и экономической эффективности остаются неопределенными». [99]
Тем не менее, руководство NICE «Инфекция новорожденных: антибиотики для профилактики и лечения» гласит: «Внутриродовая антибиотикопрофилактика должна быть предложена, если колонизация стрептококками группы B, бактериурия или инфекция выявляются при текущей беременности». [100]
Национальный отборочный комитет [ править ]
Великобритания Национального Скрининг Комитет текущей позиции политики «S на GBS является:.«Скрининг не следует предлагать все беременные женщина Этой политика была пересмотрена в 2012 году, и , несмотря на получение 212 ответов, из которых 93% ратуют скрининг, НСК решило не рекомендуют антенатальный скрининг. [101]
Это решение подверглось резкой критике со стороны благотворительной организации Group B Strep Support за игнорирование как пожеланий общественности, так и растущих показателей заболеваемости GBS в Великобритании. [102]
В мае 2006 года Национальный отборочный комитет Великобритании запустил пакет онлайн-обучения GBS. Этот учебный пакет был разработан для повышения осведомленности специалистов здравоохранения о СГБ. Учебный пакет, разработанный Библиотекой специалистов по женскому здоровью (часть Национальной библиотеки здравоохранения), основан на действующих в Великобритании руководящих принципах, опубликованных RCOG, и разделен на три раздела - дородовой, родовой и послеродовой. В каждом разделе есть возможность получить доступ к введению в GBS, различным клиническим сценариям, серии вопросов викторины для проверки знаний и разделу часто задаваемых вопросов. [ необходима цитата ]
Соединенные Штаты [ править ]
Рекомендации по IAP для предотвращения перинатального заболевания GBS были выпущены CDC в 1996 году. В этих рекомендациях рекомендуется использовать один из двух методов профилактики: подход, основанный на оценке риска, или подход скрининга на основе культуры. [45] CDC выпустил обновленные инструкции в 2002 году; в этих рекомендациях рекомендуется универсальный скрининг всех беременных женщин на сроках 35–37 недель на основе посевов для оптимизации выявления женщин, которые должны получать IAP. CDC также рекомендовал, чтобы женщины с неизвестным статусом колонизации GBS во время родов контролировались в соответствии с наличием факторов риска во время родов. Благодаря этой стратегии в США значительно снизилась заболеваемость GBS-EOD. [103]
CDC снова выпустил обновленные руководства в 2010 году, однако основы профилактики в рекомендациях CDC 2010 года остались неизменными. [20] Основными дополнениями к руководящим принципам 2010 г. были следующие: [ необходима цитата ]
- Расширенные возможности лабораторного обнаружения GBS включают использование пигментированных сред и ПЦР-анализов.
- Пересмотренный порог подсчета колоний был установлен для лабораторий, чтобы регистрировать GBS в моче беременных женщин.
- Пересмотренные алгоритмы скрининга GBS и использования IAP для женщин с угрозой преждевременных родов включают один алгоритм для преждевременных родов и один для преждевременного преждевременного разрыва плодных оболочек.
- Рекомендации по препаратам IAP представлены в формате алгоритма, чтобы способствовать использованию наиболее подходящего антибиотика у женщин с аллергией на пенициллин.
- В дозирование пенициллина было внесено небольшое изменение, чтобы облегчить внедрение в учреждениях с различными упакованными продуктами пенициллина.
- Сфера применения алгоритма неонатального ведения была расширена и теперь распространяется на всех новорожденных.
- Рекомендации по ведению зависят от клинической картины новорожденного и других факторов риска, таких как материнский хориоамнионит, адекватность ВБД, если показано для матери, гестационный возраст и продолжительность разрыва мембраны.
- В алгоритм были внесены изменения, чтобы уменьшить количество ненужных оценок у хорошо выглядящих новорожденных с относительно низким риском GBS-EOD.
В 2018 году задача по пересмотру и обновлению рекомендаций по профилактике GBS была передана из CDC в ACOG ( Американский колледж акушеров и гинекологов ) (ACOG) и в Американскую академию педиатрии . [ необходима цитата ]
Комитет ACOG выпустил обновленный документ о профилактике стрептококковых заболеваний с ранним началом у новорожденных группы B в 2019 году. [22] Руководство ACOG заменило рекомендации 2010 года, опубликованные CDC. [104]
Этот документ не вносит важных изменений в рекомендации CDC. Ключевыми мерами, необходимыми для предотвращения раннего начала заболевания GBS у новорожденных, по-прежнему являются универсальный пренатальный скрининг с помощью посева GBS из мазков, взятых из нижней части влагалища и прямой кишки, правильный сбор и микробиологическая обработка образцов, а также правильное внедрение антибиотикопрофилактики во время родов. Также важно отметить, что ACOG рекомендовал проводить универсальный скрининг СГБ на сроках от 36 до 37 недель беременности. Эта новая рекомендация предусматривает 5-недельное окно [60] для достоверных результатов посева, которое включает роды, которые происходят до гестационного возраста не менее 41 недели.
В 2019 году Американская академия педиатрии (AAP) опубликовала новый клинический отчет «Ведение младенцев с риском неонатального заболевания, связанного с СГБ». [105] Клинический отчет AAP заменил рекомендации 2010 г., опубликованные CDC.
Другие правила [ править ]
Национальные руководства в большинстве развитых стран рекомендуют использовать всеобщий скрининг беременных женщин на поздних сроках беременности для выявления носительства GBS и использования IAP у всех колонизированных матерей. например, Канада, [106] Испания, [107] Швейцария, [108] Германия, [109] Польша, [110] Чехия, [111] Франция, [112] Норвегия и Бельгия. [113]
В отличие от этого руководства, основанные на факторах риска, были выпущены в Нидерландах [114], Новой Зеландии, Аргентине [115] и Квинсленде.[116] Тем не менее, Королевский колледж акушеров и гинекологов Австралии и Новой Зеландии не рекомендует однозначно одну из обеих стратегий профилактики - ни подход, основанный на оценке риска, ни культуральный подход для выявления беременных женщин на ВБД, и позволяет практикующим врачам выбирать в соответствии с юрисдикционные правила. [117]
Взрослые [ править ]
СГБ также является важным инфекционным агентом, способным вызывать инвазивные инфекции у взрослых. Серьезные опасные для жизни инвазивные инфекции GBS все чаще распознаются у пожилых людей и у людей, страдающих такими заболеваниями, как диабет, цирроз и рак. Инфекции GBS у взрослых включают инфекцию мочевыводящих путей, инфекцию кожи и мягких тканей (инфекцию кожи и кожных структур ), бактериемию без очага, остеомиелит, менингит и эндокардит . [14] Инфекция GBS у взрослых может быть серьезной, а смертность среди взрослых выше, чем среди новорожденных. [118]Как правило, пенициллин - это антибиотик выбора для лечения инфекций, вызываемых СГБ. Эритромицин или клиндамицин не следует использовать для лечения пациентов с аллергией на пенициллин, если только не подтверждена чувствительность инфекционного изолята GBS к этим агентам. Может использоваться гентамицин плюс пенициллин (для синергии с антибиотиками ) у пациентов с опасными для жизни инфекциями, вызываемыми СГБ. [119] [120] [121]
Синдром токсического шока (СТШ) - это острое мультисистемное опасное для жизни заболевание, приводящее к полиорганной недостаточности. Тяжесть этого заболевания часто требует немедленной медицинской помощи. СТШ вызывается в первую очередь некоторыми штаммами Staphylococcus aureus и Streptococcus pyogenes, которые продуцируют экзотоксины. Тем не менее, инвазивная инфекция GBS может осложняться, хотя и довольно редко, стрептококковым токсическим шоковым синдромом (STLS) [122].
Общество и культура [ править ]
Июль был объявлен Месяцем осведомленности о стрептококках группы B [123], когда информация о стрептококках группы B распространяется среди семей и медицинских работников, преимущественно в Великобритании и США. В Великобритании этим занимается Служба поддержки стрептококка группы B [124].
Вакцина [ править ]
Хотя введение национальных руководств по скринингу беременных женщин на носительство GBS и использование IAP значительно снизило бремя болезни GBS-EOD, оно не повлияло на предотвращение GBS-LOD у младенцев или инфекций GBS у взрослых. [125] По этой причине, если бы эффективная вакцина против СГБ была доступна, она была бы эффективным средством борьбы не только с СГБ у младенцев, но и с инфекциями у взрослых. [ необходима цитата ]
Существует ряд проблем с назначением антибиотиков роженицам. Такие риски воздействия антибиотиков включали тяжелые аллергические реакции и трудности при проверке беременных женщин на СГБ. Если беременным женщинам можно сделать вакцину против СГБ, это потенциально могло бы предотвратить большинство случаев СГБ без необходимости в антибиотиках или скрининге. Вакцинация считается идеальным решением для предотвращения не только заболеваний с ранним и поздним началом, но и инфекций СГБ у взрослых из группы риска. [126]
Всемирная организация здравоохранения определила разработку вакцин против СГБ для иммунизации матерей в качестве приоритетной задачи из-за большого количества неудовлетворенных потребностей. [127] Было подсчитано, что такая вакцина потенциально может предотвратить 231 000 случаев СГБ у младенцев и матерей. [128]
Еще в 1976 г. [32] было показано, что низкие уровни материнских антител против капсульного полисахарида GBS коррелируют с чувствительностью к GBS-EOD и GBS-LOD. Специфические материнские антитела, переданные от матери новорожденному, смогли обеспечить защиту младенцев от инфекции GBS. [129] капсульный полисахарид из GBS, что является важным фактором вирулентности, также является отличным кандидат для разработки эффективной вакцины. [130] [129] [131] [132]
Вакцины на основе белка GBS также находятся в стадии разработки. [133] [134] [135]
В настоящее время лицензирование вакцин против СГБ затруднено из-за сложности проведения клинических испытаний на людях из-за низкой частоты неонатальных заболеваний, связанных с СГБ. [24] [131] [136] Тем не менее, несмотря на то, что исследования и клинические испытания по разработке эффективной вакцины для предотвращения инфекций GBS продолжаются, по состоянию на 2019 г. вакцины нет. [133] [137]
Нечеловеческие инфекции [ править ]
GBS был обнаружен у многих млекопитающих и других животных, таких как верблюды, собаки, кошки, тюлени, дельфины и крокодилы. [138]
Крупный рогатый скот [ править ]
У крупного рогатого скота GBS вызывает мастит, инфекцию вымени. Это может вызвать острую лихорадку или подострое хроническое заболевание. И то, и другое приводит к уменьшению производства молока (отсюда и название: agalactiae, что означает «без молока»). Мастит, связанный с СГБ, может иметь важное влияние на количество и качество производимого молока, а также связан с повышенным количеством соматических клеток и общим количеством бактерий в молоке. [139] Вспышки в стадах являются обычным явлением, и, поскольку это имеет большое значение для молочной промышленности, во многих странах были приняты программы по снижению воздействия GBS [140]
Рыба [ править ]
GBS также является важным патогеном для множества видов рыб, приводя к серьезным экономическим потерям для многих видов рыб во всем мире. СГБ вызывает серьезные эпидемии у разводимой рыбы, вызывая сепсис, внешние и внутренние кровотечения. Инфицирование GBS было зарегистрировано от диких рыб и рыб, содержащихся в неволе, и было вовлечено в эпизоотии во многих странах. [141] [142] Вакцины для защиты рыб от инфекций GBS находятся в стадии разработки. [143] [144]
Ссылки [ править ]
- ^ "Группа B Strep" . nhs.uk . 7 февраля 2018 . Проверено 8 декабря 2019 .
- ^ Maisey НС, Доран К.С., Nizet В (2009). «Последние достижения в понимании молекулярных основ вирулентности Streptococcus группы B» . Обзоры экспертов в области молекулярной медицины . 10 : e27. DOI : 10.1017 / S1462399408000811 . PMC 2676346 . PMID 18803886 .
- ^ a b Раджагопал Л. (2009). «Понимание регуляции факторов вирулентности стрептококков группы B» . Будущая микробиология . 4 (2): 201–221. DOI : 10.2217 / 17460913.4.2.201 . PMC 2691590 . PMID 19257847 .
- ^ Леклерк SY, Sullivan MJ, Ipe DS, Смит JP, Криппс AW, Ulett GC (2016). «Патогенез инфекции мочевыводящих путей Streptococcus зависит от штамма бактерий и β-гемолизина / цитолизина, который опосредует цитотоксичность, синтез цитокинов, воспаление и вирулентность» . Научные отчеты . 6 : 29000. Bibcode : 2016NatSR ... 629000L . DOI : 10.1038 / srep29000 . PMC 4935997 . PMID 27383371 .
- ^ Б с д е е г ч я J к л м Эдвардса МС, Nizet В (2011). Стрептококковые инфекции группы B. Инфекционные болезни плода и новорожденного (7-е изд.). Эльзевир. С. 419–469. ISBN 978-0-443-06839-3.
- ^ Уидби С, Харрелл М.И., бернсайдовского К, Нго л, Becraft А.К., Ийер Л.М., Аравиндом л, Хитти Дж, Вальдорфская КМ, Раджагопал L (2013). «Гемолитический пигмент Streptococcus группы B позволяет бактериям проникать через плаценту человека» . Журнал экспериментальной медицины . 210 (6): 1265–1281. DOI : 10,1084 / jem.20122753 . PMC 3674703 . PMID 23712433 .
- ^ Роса-Фрайл М, Dramsi S, Spellerberg В (2014). «Стрептококковый гемолизин и пигмент группы B, сказка о близнецах» (PDF) . Обзоры микробиологии FEMS . 38 (5): 932–946. DOI : 10.1111 / 1574-6976.12071 . PMC 4315905 . PMID 24617549 .
- ^ Whidbey C, Vornhagen J, Gendrin C, Boldenow E, Samson JM, Doering K, Ngo L, Ezekwe EA Jr, Gundlach JH, Elovitz MA, Liggitt D, Duncan JA, Adams Waldorf KM, Rajagopal L (2015). «Стрептококковый липидный токсин вызывает мембранную проницаемость и пироптоз, что приводит к повреждению плода» . EMBO Молекулярная медицина . 7 (4): 488–505. DOI : 10.15252 / emmm.201404883 . PMC 4403049 . PMID 25750210 .
- ^ Кристофер-Микаэль Уидби (2015). Характеристика гемолизина Streptococcus группы B и его роли во внутриутробной инфекции (PDF) . Вашингтонский университет.
- ^ Keefe GP. (1997). «Streptococcus agalactiae мастит: обзор» . Канадский ветеринарный журнал . 38 (7): 199–204. PMC 1576741 . PMID 9220132 .
- ^ Фрай РМ. (1938). «Смертельные инфекции гемолитическим стрептококком группы В.». Ланцет . 231 (5969): 199–201. DOI : 10.1016 / S0140-6736 (00) 93202-1 .
- ^ Айкхофф TC; Klein JO; Кэтлин Дейли А; Дэвид Ингалл; Финляндия М. (1964). «Неонатальный сепсис и другие инфекции, вызванные бета-гемолитическими стрептококками группы B». Медицинский журнал Новой Англии . 271 (24): 1221–1228. DOI : 10.1056 / NEJM196412102712401 . PMID 14234266 .
- ^ "Стрептококковая инфекция группы B" . MedicineNet.com . Проверено 10 января +2016 .
- ^ a b c Эдвардс MS, Бейкер CJ (2010). Streptococcus agalactiae (стрептококки группы В). Mandell GL, Bennett JE, Dolin R (eds) Принципы и практика инфекционных заболеваний. Том 2 (7-е изд.). Эльзевир. с. Глава 202. ISBN 978-0-443-06839-3.
- ^ а б Тилле П. (2014). Диагностическая микробиология Бейли и Скотта (13-е изд.). Эльзевир. ISBN 978-0-323-08330-0.
- ^ Б с д е е г Роза-Fraile М., Spellerberg B. (2017). «Надежное обнаружение стрептококков группы B в клинической лаборатории» (PDF) . Журнал клинической микробиологии . 55 (9): 2590–2598. DOI : 10.1128 / JCM.00582-17 . PMC 5648696 . PMID 28659318 . Проверено 23 ноября 2019 года .
- ^ a b Роса-Фрайле М, Родригес-Грейнджер Дж, Куэто-Лопес М, Сампедро А, Биль Гай Э, Аро М, Андреу А (1999). «Использование среды Гранады для выявления колонизации стрептококками группы B у беременных» . Журнал клинической микробиологии . 37 (8): 2674–2677. DOI : 10.1128 / JCM.37.8.2674-2677.1999 . PMC 85311 . PMID 10405420 .
- ^ Binghuai л, Яньли S, Shuchen Z, Z Fengxia, Dong L, Yanchao С (2014). «Использование масс-спектрометрии MALDI-TOF для быстрой идентификации Streptococcus группы B на агаре chromID Strepto B» . Международный журнал инфекционных болезней . 27 : 44–48. DOI : 10.1016 / j.ijid.2014.06.023 . PMID 25220051 .
- ^ К KN, Корнуэлл E, Дэниел R, Goonesekera S, Jauneikaite E, Chalker V, Le Doare K. (2019). «Оценка времяпролетной масс-спектрометрии с лазерной десорбцией и ионизацией с использованием матрицы (MALDI-TOF MS) для идентификации Streptococcus группы B» . BMC Research Notes . 12 (1): 85. DOI : 10,1186 / s13104-019-4119-1 . PMC 6376729 . PMID 30764872 . CS1 maint: несколько имен: список авторов ( ссылка )
- ^ Б с д е е г ч я J к л м п о р Q R сек т у V ш х у г аа аЬ ас объявлений к.э. аф Verani JR, L McGee, Schrag SJ (2010). «Профилактика перинатального стрептококкового заболевания группы B: пересмотренное руководство CDC» (PDF) . MMWR Recomm. Rep . 59 ((RR-10)): 1–32. CS1 maint: multiple names: authors list (link)
- ^ Эль Айла Н.А., Стихийность я, Claeys G, Saerens В, Кулз Р, Verstraelen Н, Теммерман М, Верхельст Р, Vaneechoutte М (2010). «Сравнение различных методов отбора проб и различных методов культивирования для выявления носительства стрептококка группы B у беременных» . BMC Инфекционные болезни . 10 : 285. DOI : 10,1186 / 1471-2334-10-285 . PMC 2956727 . PMID 20920213 . CS1 maint: multiple names: authors list (link)
- ^ a b c d e f g h i j k l m n o p q Американский колледж акушеров и гинекологов (ACOG). (2019). «Профилактика стрептококковой инфекции с ранним началом у новорожденных, Заключение Комитета ACOG, номер 782» . Акушерство и гинекология . 134 (1): e19-40. DOI : 10,1097 / AOG.0000000000003334 . PMID 31241599 . S2CID 195659363 .
- ^ a b Barcaite E, Bartusevicius A, Tameliene R, Kliucinskas M, Maleckiene L, Nadisauskiene R (2008). «Распространенность колонизации материнской группы B стрептококками в европейских странах». Acta Obstetricia et Gynecologica Scandinavica . 87 (3): 260–271. DOI : 10.1080 / 00016340801908759 . PMID 18307064 . S2CID 25897076 .
- ^ a b c d e Родригес-Грейнджер Дж., Альваргонзалес Дж. К., Берарди А., Бернер Р., Кунце М., Хуфнагель М., Мелин П., Дечева А., Орефичи Дж., Пойярт К., Телфорд Дж., Эфстратиу А., Киллиан М., Кризова П., Baldassarri L, Spellerberg B, Puertas A, Rosa-Fraile M (2012). «Еще раз о профилактике неонатальных заболеваний, вызванных стрептококками группы B. Европейский проект DEVANI» . Европейский журнал клинической микробиологии и инфекционных заболеваний . 31 (9): 2097–2114. DOI : 10.1007 / s10096-012-1559-0 . PMID 22314410 . S2CID 15588906 .
- ^ Muller AE, Oostvogel PM, Steegers Е.А., Dörr PJ. (2016). «Заболеваемость, связанная с материнскими стрептококковыми инфекциями группы B». Acta Obstetricia et Gynecologica Scandinavica . 85 (9): 1027–37. DOI : 10.1080 / 00016340600780508 . PMID 16929406 . S2CID 11745321 . CS1 maint: multiple names: authors list (link)
- ^ Cunningham, F, Leveno KJ, Bloom SL, Spong CY, Даша JS, Хоффман BL, BM Casey, Шеффилд JS (2013). «Аборт». Акушерство Уильямса . Макгроу-Хилл. п. 5.
- ^ a b Либстер Р., Эдвардс К.М., Левент Ф, Эдвардс М.С., Ренч М.А., Кастаньини Л.А., Купер Т., Спаркс Р.С., Бейкер С.Дж., Шах PE (2012). «Отдаленные исходы стрептококкового менингита группы B» (PDF) . Педиатрия . 130 (1): e8–15. DOI : 10.1542 / peds.2011-3453 . PMID 22689869 . S2CID 1013682 .
- ^ Полин Р.А. (2012). «Ведение новорожденных с подозрением или доказанным ранним бактериальным сепсисом» (PDF) . Педиатрия . 129 (5): 1006–1015. DOI : 10.1542 / peds.2012-0541 . PMID 22547779 . С2КИД 230591 .
- ^ Мартинес Е, Mintegi S, Вилар В, Мартинес МДж, Лопес А, Catediano Е, Гомес В (2015). «Распространенность и предикторы бактериального менингита у младенцев с лихорадкой без источника». Журнал детских инфекционных болезней . 34 (5): 494–498. DOI : 10.1097 / inf.0000000000000629 . PMID 25461476 . S2CID 43717212 .
- ^ a b c Бойер KM, Gotoff SP (1985). «Стратегии химиопрофилактики раннего начала инфекций GBS1». Стратегии химиопрофилактики инфекций с ранним началом GBS . Антибиотики и химиотерапия. 35 . С. 267–280. DOI : 10.1159 / 000410380 . ISBN 978-3-8055-3953-1. PMID 3931544 .
- ^ Dauby N, Chamekh М, Мелин Р, Slogrove А, Goetghebuer Т (2016). «Повышенный риск инвазивной инфекции стрептококками группы B у ВИЧ-инфицированных, но неинфицированных младенцев: обзор доказательств и возможных механизмов» . Границы иммунологии . 16 : 505. DOI : 10.3389 / fimmu.2016.00505 . PMC 5110531 . PMID 27899925 .
- ^ a b Бейкер CJ, Каспер DL (1976). «Корреляция материнской недостаточности антител с восприимчивостью к неонатальной инфекции Streptococcus группы B». Медицинский журнал Новой Англии . 294 (14): 753–756. DOI : 10.1056 / nejm197604012941404 . PMID 768760 .
- ^ Бейкер CJ, Эдвардс МС, Kasper DL (1981). «Роль антител к полисахариду нативного типа III Streptococcus группы B в детской инфекции». Педиатрия . 68 (4): 544–549. PMID 7033911 .
- ^ а б Эдмонд К.М., Корцалиоудаки С., Скотт С., Шраг С.Дж., Заиди А.К., Кузенс С., Хит П.Т. (2012). «Стрептококковая инфекция группы B у детей младше 3 месяцев: систематический обзор и метаанализ» (PDF) . Ланцет . 379 (9815): 547–556. DOI : 10.1016 / s0140-6736 (11) 61651-6 . PMID 22226047 . S2CID 15438484 .
- ^ Lin FY, Вайсман LE, Troendle J, K Adams (2003). «Недоношенность является основным фактором риска для позднего начала стрептококковой болезни группы B» (PDF) . Журнал инфекционных болезней . 188 (2): 267–271. DOI : 10,1086 / 376457 . PMID 12854082 .
- ^ Лин, F; Бреннер, РА; Джонсон, Ю. Р.; Азими, PH; Philips Jb, 3-й; Regan, JA; Кларк, П; Weisman, LE; и другие. (2001). «Эффективность химиопрофилактики во время родов с учетом риска для предотвращения раннего начала неонатальной стрептококковой болезни группы B». Американский журнал акушерства и гинекологии . 184 (6): 1204–10. DOI : 10.1067 / mob.2001.113875 . PMID 11349189 .
- ^ Де Куэто, М; Санчес, MJ; Сампедро, А; Miranda, JA; Herruzo, AJ; Роза-Фрайле, М. (1998). «Время приема ампициллина в родах и профилактика вертикальной передачи стрептококков группы B». Акушерство и гинекология . 91 (1): 112–4. DOI : 10.1016 / S0029-7844 (97) 00587-5 . PMID 9464732 . S2CID 22858678 .
- Перейти ↑ Berardi A, Rossi C, Biasini A, Minniti S, Venturelli C, Ferrari F, Facchinetti F (2011). «Эффективность химиопрофилактики в родах продолжительностью менее 4 часов». Журнал материнско-фетальной и неонатальной медицины . 24 (4): 619–625. DOI : 10.3109 / 14767058.2010.511347 . PMID 20828241 . S2CID 6697604 .
- ^ Бхаттачарья С. (2010). «Факты об аллергии на пенициллин: обзор» . Журнал передовых фармацевтических технологий и исследований . 1 (1): 11–17. PMC 3255391 . PMID 22247826 .
- ^ Балтимор RS, Huie С.М., Кроткий СО, Schuchat A, О'Брайен KL (2001). «Ранний неонатальный сепсис в эпоху профилактики стрептококков группы B». Педиатрия . 108 (5): 1094–1098. DOI : 10.1542 / peds.108.5.1094 . PMID 11694686 .
- ^ Суткин G, Крон MA, Heine RP, Сладкие RL (2005). «Антибиотикопрофилактика и неонатальный сепсис, вызванный стрептококками не группы B». Акушерство и гинекология . 105 (3): 581–586. DOI : 10.1097 / 01.aog.0000153492.30757.2f . PMID 15738028 . S2CID 22019440 .
- ^ Schrag SJ, Hadler JL, Арнольд KE, Martell-Клири P, Рейнгольд A, Schuchat A (2006). «Факторы риска инвазивных инфекций Escherichia coli с ранним началом в эпоху широкого применения антибиотиков во время родов». Педиатрия . 118 (2): 560–566. DOI : 10.1542 / peds.2005-3083 . PMID 16882809 . S2CID 34908773 .
- ^ Катленд, Клэр L; Мадхи, Шабир А; Зелл, Элизабет Р.; Куванда, Локадия; Лак, Мартин; Грум, Мишель; Горвиц, Рэйчел; Тигпен, Майкл С; и другие. (2009). «Хлоргексидиновые салфетки для тела матери, влагалища и новорожденных при сепсисе и вертикальной передаче патогенных бактерий в Южной Африке: рандомизированное контролируемое исследование». Ланцет . 374 (9705): 1909–16. DOI : 10.1016 / S0140-6736 (09) 61339-8 . PMID 19846212 . S2CID 23418670 .
- ^ Олссон, А; Шах, VS; Стаде, Британская Колумбия (14 декабря 2014 г.). «Вагинальный хлоргексидин во время родов для предотвращения раннего начала неонатальной стрептококковой инфекции группы B». Кокрановская база данных систематических обзоров . 12 (12): CD003520. DOI : 10.1002 / 14651858.CD003520.pub3 . PMID 25504106 .
- ^ а б CDC (1996). «Профилактика перинатального стрептококкового заболевания группы B: перспективы общественного здравоохранения» . MMWR . 45-RR7: 1–24.
- ^ Clifford V, Garland SM, Grimwood K (2011). «Профилактика неонатальной болезни, вызванной стрептококками группы B в 21 веке». Журнал педиатрии и детского здоровья . 48 (9): 808–815. DOI : 10.1111 / j.1440-1754.2011.02203.x . PMID 22151082 .
- ^ Шраг SJ, Зелл ER, Линфилд R, Roome A, Арнольд KE, Крейг AS, Харрисон LH, Рейнгольд A, Стефонек K, Смит G, Гэмбл M, Schuchat A; Группа активного наблюдения за ядром бактерий. (2002). «Популяционное сравнение стратегий профилактики стрептококковой инфекции группы B с ранним началом у новорожденных». Медицинский журнал Новой Англии . 347 (4): 233–239. DOI : 10.1056 / nejmoa020205 . PMID 12140298 . CS1 maint: multiple names: authors list (link)
- ^ a b c d Хименес М., Санфелиу I, Сьерра М, Допико E, Хункоса Т, Андреу А, Лайт J, Гуарда С, Санчес Ф, Бош Дж., Статья на испанском языке. (2015). "Evolución de la sepsis neonatal precoz por Streptococcus agalactiae en el área de Barcelona (2004-2010). Аналитический анализ фаллос дель cumplimiento дель протокола профилактики. Ранний стрептококковый сепсис новорожденных в районе Барселоны (2004-2010)" . Анализ упущенных возможностей для предотвращения » (PDF) . Enfermedades Infecciosas y Microbiologia Clinica . 33 (7): 446–450. DOI : 10.1016 / j.eimc.2014.10.015 . PMID 25541009 . Архивировано из оригинал (PDF) 23 февраля 2016 года . Проверено 15 января 2016 .CS1 maint: multiple names: authors list (link)
- ^ Phares CR, Lynfield R, Фарли MM, Mohle-Boetani J, Harrison LH, Petit S, Craig AS, Schaffner W, Zansky SM, Gershman K, Stefonek KR, Albanese BA, Zell ER, Schuchat A, Schrag SJ; Активная сеть программы эпиднадзора за основными бактериальными инфекциями / возникающими инфекциями. (2008). «Эпидемиология инвазивной стрептококковой болезни группы B в США, 1999-2005» . JAMA . 299 (17): 2056–2065. DOI : 10,1001 / jama.299.17.2056 . PMID 18460666 . CS1 maint: multiple names: authors list (link)
- ^ а б Колборн, Т; Ассебург, К; Bojke, L; Philips, Z; Claxton, K; Ades, AE; Гилберт, RE (2007). «Пренатальный скрининг и стратегии лечения для предотвращения стрептококков группы B и других бактериальных инфекций в раннем младенчестве: рентабельность и ожидаемая ценность анализа информации» . Оценка технологий здравоохранения . 11 (29): 1–226, iii. DOI : 10,3310 / hta11290 . PMID 17651659 .
- ^ a b c Colbourn, T. E; Asseburg, C .; Bojke, L .; Philips, Z .; Велтон, Н. Дж; Claxton, K .; Ades, AE; Гилберт, Р. Э (2007). «Стратегии профилактики стрептококков группы B и других бактериальных инфекций в раннем младенчестве: экономическая эффективность и ценность информационного анализа» . BMJ . 335 (7621): 655. DOI : 10.1136 / bmj.39325.681806.AD . PMC 1995477 . PMID 17848402 .
- ^ a b Каамбва Б., Брайан С., Грей Дж., Милнер П., Дэниелс Дж., Хан К.С., Робертс Т.Э. (2010). «Экономическая эффективность экспресс-тестов и других существующих стратегий для скрининга и лечения стрептококков группы B с ранним началом во время родов» . BJOG: Международный журнал акушерства и гинекологии . 117 (13): 1616–1627. DOI : 10.1111 / j.1471-0528.2010.02752.x . PMID 21078057 . S2CID 25561127 .
- ^ a b Верньяно S, Эмблтон N, Коллинсон A, Менсон E, Бедфорд Рассел A, Хит P (2010). «Упущенные возможности для предотвращения заражения стрептококком группы B». Архивы болезней детства - фетальное и неонатальное издание . 95 (1): F72–73. DOI : 10.1136 / adc.2009.160333 . PMID 19439431 . S2CID 38297857 .
- ^ Steer, PJ; Пламб, Дж. (2011). «Миф: стрептококковая инфекция группы B во время беременности: постижение и победа». Семинары по медицине плода и неонатологии . 16 (5): 254–8. DOI : 10.1016 / j.siny.2011.03.005 . PMID 21493170 .
- ^ Siegel JD, Подушка NB (1996). «Профилактика стрептококковой инфекции группы B с ранним началом: еще один взгляд на однократную дозу пенициллина при рождении». Акушерство и гинекология . 87 (5 Pt 1): 692–698. DOI : 10.1016 / 0029-7844 (96) 00004-X . PMID 8677068 . S2CID 40716699 .
- ^ Velaphi S, Siegel JD, Вендель GD Jr, Подушка N, Ид WM, Sanchez PJ (2003). «Ранняя стрептококковая инфекция группы B после комбинированной стратегии химиопрофилактики стрептококков группы B у матери и новорожденного». Педиатрия . 111 (3): 541–547. DOI : 10.1542 / peds.111.3.541 . PMID 12612234 .
- ^ Woodgate PG, Flenady V, Steer PA (2004). «Внутримышечный пенициллин для профилактики раннего начала стрептококковой инфекции группы B у новорожденных». Кокрановская база данных систематических обзоров (3): CD003667. DOI : 10.1002 / 14651858.CD003667.pub2 . PMID 15266494 .
- ^ ПОДДЕРЖКА СТРЕЛКИ ГРУППЫ B. "Часто задаваемые вопросы35. Вынашивание СГБ и домашних родов?" . Проверено 25 ноября 2019 года .
- ^ а б в г Хьюз Р.Г., Броклхерст П., Стир П.Дж., Хит П., Стенсон Б.М. от имени Королевского колледжа акушеров и гинекологов. (2017). «Профилактика стрептококковой инфекции группы B с ранним началом у новорожденных. Зеленое руководство № 36. Сентябрь 2017 г.» . BJOG: Международный журнал акушерства и гинекологии . 124 (12): e280 – e305. DOI : 10.1111 / 1471-0528.14821 . PMID 28901693 . CS1 maint: multiple names: authors list (link)
- ^ a b Янси М.К., Шухат А., Браун Л.К., Вентура В.Л., Маркенсон Г.Р. (1996). «Точность поздних антенатальных скрининговых культур в прогнозировании колонизации генитальными стрептококками группы B при родах». Акушерство и гинекология . 88 (5): 811–815. DOI : 10.1016 / 0029-7844 (96) 00320-1 . PMID 8885919 . CS1 maint: multiple names: authors list (link)
- ^ Валькенбург-ван ден Берг AW, Houtman-Roelofsen RL, Oostvogel PM, Dekker FW, Dorr PJ, Sprij AJ (2010). «Сроки скрининга на стрептококки группы B у беременных: систематический обзор». Гинекологическое и акушерское обследование . 69 (3): 174–183. DOI : 10.1159 / 000265942 . PMID 20016190 . S2CID 26709882 .
- ^ Цена D, E Shaw, Howard M, J Zazulak, Уотерс H, Kaczorowski J (2006). «Самостоятельный отбор образцов на стрептококк группы B у женщин на 35–37 неделях беременности является точным и приемлемым: рандомизированное перекрестное исследование». Журнал акушерства и гинекологии Канады . 28 (12): 1083–8. DOI : 10.1016 / s1701-2163 (16) 32337-4 . PMID 17169231 .
- Перейти ↑ Hicks P, Diaz-Perez MJ (2009). «Самостоятельный сбор образцов стрептококков группы B во время беременности» . Журнал Американского совета семейной медицины . 22 (2): 136–140. DOI : 10.3122 / jabfm.2009.02.080011 . PMID 19264936 .
- ^ Арья А; Cryan B; О'Салливан К; Грин Р.А.; Хиггинс-младший. (2008). «Самостоятельный сбор мазков с гениталий и мазков, собранных медицинским работником для определения распространенности стрептококка группы B: сравнение предпочтений пациентов и их эффективности». Европейский журнал акушерства, гинекологии и репродуктивной биологии . 139 (1): 32–45. DOI : 10.1016 / j.ejogrb.2007.12.005 . PMID 18255214 .
- ^ Роса-Фрайле М, Камачо-Муньос Е, Родригес-Грейнджер Дж, Liebana-Мартос С (2005). «Хранение образцов в транспортной среде и обнаружение стрептококков группы B путем посева» . Журнал клинической микробиологии . 43 (2): 928–930. DOI : 10.1128 / jcm.43.2.928-930.2005 . PMC 548104 . PMID 15695709 .
- ^ a b Кэри РБ. «Стрептококки группы B: цепи и изменения, новые рекомендации по предотвращению раннего начала GBS» (PDF) . Проверено 11 января +2016 .
- ^ UK Gov. "SMI B 58: обнаружение носительства стрептококков группы B. Обновлено 2018" . Проверено 28 ноября 2019 .
- ^ Гил, EG; Родригес, МС; Bartolomé, R; Бержано, B; Каберо, L; Андреу, А (1999). «Оценка чашки с агаром Гранады для выявления вагинальных и ректальных стрептококков группы B у беременных» . Журнал клинической микробиологии . 37 (8): 2648–2651. DOI : 10.1128 / JCM.37.8.2648-2651.1999 . PMC 85303 . PMID 10405415 .
- ^ Claeys, G .; Verschraegen, G .; Теммерман, М. (2001). «Модифицированная среда агара Гранады для обнаружения носительства стрептококков группы B у беременных» . Клиническая микробиология и инфекция . 7 (1): 22–24. DOI : 10,1046 / j.1469-0691.2001.00156.x . PMID 11284939 .
- ^ a b Где я могу пройти тест ECM ?. «Тестирование ECM» . Группа Стрептококковой Поддержка B . Проверено 28 ноября 2019 .
- ^ «Скрининговый тест на стрептококк группы B» . Medisave UK Ltd . Проверено 28 ноября 2019 .
- ^ «Тестирование на стрептококк группы B» . Лаборатория врачей . Проверено 28 ноября 2019 .
- ^ Бучан BW, Faron ML, Фуллер D, Davis TE, Мейн D, Ledeboer Н.А. (2015). «Многоцентровая клиническая оценка анализа LB Xpert GBS для обнаружения стрептококков группы B в образцах пренатального скрининга» . Журнал клинической микробиологии . 53 (2): 443–448. DOI : 10.1128 / jcm.02598-14 . PMC 4298547 . PMID 25411176 .
- ^ Дэниэлс Дж, Грей Дж, Паттисон Х, Робертс Т, Эдвардс Е, Милнер П, Спайсер Л, Кинг Е, Хиллз РК, Грей Р, Бакли Л, Мэджилл Л, Эллиман Н., Каамбва Б, Брайан С, Ховард Р, Томпсон П, Хан К.С. (2009). «Экспресс-тестирование на стрептококк группы B во время родов: исследование точности теста с оценкой приемлемости и экономической эффективности» (PDF) . Оценка технологий здравоохранения . 13 (42): 1–154, iii – iv. DOI : 10,3310 / hta13420 . PMID 19778493 . Архивировано из оригинального (PDF) 23 февраля 2016 года.
- ^ Мелин П. (2011). «Стрептококковая инфекция группы В новорожденных: от патогенеза к стратегиям профилактики» . Клиническая микробиология и инфекция . 17 (9): 1294–1303. DOI : 10.1111 / j.1469-0691.2011.03576.x . PMID 21672083 .
- ^ Берарди А., Лугли Л., Барончиани Д., Росси С., Чичча М., Крети Р., Гамбини Л., Мариани С., Папа I, Тридапалли Е., Вагнарелли Ф, Феррари Ф; Рабочая группа по профилактике GBS в Эмилии-Романье. (2010). «Заболевание Streptococcus группы B с ранним началом в Эмилии-Романье: обзор после внедрения подхода, основанного на скрининге». Журнал детских инфекционных болезней . 29 (2): 115–121. DOI : 10,1097 / inf.0b013e3181b83cd9 . PMID 19915512 . S2CID 31548613 . CS1 maint: multiple names: authors list (link)
- ^ Schrag SJ, Verani JR (2013). «Интранатальная антибиотикопрофилактика для профилактики перинатального стрептококкового заболевания группы B: опыт США и последствия для потенциальной вакцины против стрептококка группы B» . Вакцина . 31С : D20–26. DOI : 10.1016 / j.vaccine.2012.11.056 . PMID 23219695 .
- ^ Pulver LS, Hopfenbeck MM, Young PC, Стоддард GJ, Korgenski K, J Daly, Байингтон CL (2009). «Продолжение стрептококковых инфекций группы B с ранним началом в эпоху внутриродовой профилактики» . Журнал перинатологии . 29 (1): 0–25. DOI : 10.1038 / jp.2008.115 . PMID 18704032 .
- ^ Хит П.Т., Бальфур Г., Вайснер А.М., Эфстратиу А., Ламаньи Т.Л., Тайге Х., О'Коннелл Л.А., Кафферки М., Верландер Н.К., Николл А., Маккартни А.С. PHLS Group B Streptococcus Working Group. (2004). «Стрептококковая инфекция группы B у детей младше 90 дней в Великобритании и Ирландии». Ланцет . 363 (9405): 292–294. DOI : 10.1016 / s0140-6736 (03) 15389-5 . PMID 14751704 . S2CID 22371160 . CS1 maint: multiple names: authors list (link)
- ^ а б Доар К., Хит ПТ (2013). «Обзор глобальной эпидемиологии СГБ». Вакцина . 31 Дополнение 4: D7–12. DOI : 10.1016 / j.vaccine.2013.01.009 . PMID 23973349 .
- ^ Бригцен А.К .; Якобсен А.Ф .; Деди Л .; Мелби К.К.; Fugelseth D .; Уайтлоу А. (2015). «Колонизация матери стрептококками группы B связана с увеличением числа младенцев, переводимых в отделение интенсивной терапии новорожденных». Неонатология . 108 (3): 157–163. DOI : 10.1159 / 000434716 . PMID 26182960 . S2CID 24711146 .
- ^ Карбонелл-Estrany X, Фигерас-Aloy J, Salcedo-Abizanda S, де ла Роса-Фрайле M, Castrillo Study Group (2008). «Вероятный стрептококковый неонатальный сепсис группы B с ранним началом: серьезное клиническое состояние, связанное с внутриутробной инфекцией». Архивы болезней детства - фетальное и неонатальное издание . 93 (2): F85–89. DOI : 10.1136 / adc.2007.119958 . PMID 17704105 . S2CID 10300571 .
- ^ Удачи, Сюзанна; Торни, Майкл; д'Агапейев, Катрина; Питт, Элисон; Хит, Пол; Breathnach, Aoadhan; Рассел, Элисон Бедфорд (2003). «Предполагаемое раннее начало стрептококковой болезни новорожденных группы B». Ланцет . 361 (9373): 1953–1954. DOI : 10.1016 / S0140-6736 (03) 13553-2 . PMID 12801740 . S2CID 33025300 .
- ^ Lamagni TL, Keshishian С, Efstratiou А, Ги R, Хендерсон KL, Бругтон К, Е Шеридан (2013). «Новые тенденции в эпидемиологии инвазивной стрептококковой болезни группы B в Англии и Уэльсе, 1991–2010 годы» . Клинические инфекционные болезни . 57 (5): 682–688. DOI : 10.1093 / CID / cit337 . PMID 23845950 .
- ^ CDC. «Стрептококк группы B (GBS) - Клинический обзор» . Проверено 10 января +2016 .
- ^ a b Nanduri SA, Petit S, Smelser C, Apostol M, Alden NB, Harrison LH, Lynfield R, Vagnone PS, Burzlaff K, Spina NL, Dufort EM, Schaffner W, Thomas AR, Farley MM, Jain JH, Pondo T. , МакГи Л., Билл Б.В., Шраг С.Дж. (2019). «Эпидемиология инвазивного стрептококкового заболевания группы B с ранним и поздним началом в США, 2006–2015 годы: многогосударственный лабораторный и популяционный эпиднадзор» . JAMA Pediatrics . 173 (3): 224–33. DOI : 10,1001 / jamapediatrics.2018.4826 . PMC 6439883 . PMID 30640366 . CS1 maint: multiple names: authors list (link)
- ^ Бейкер CJ. (2013). «Спектр перинатального стрептококкового заболевания группы В». Вакцина . 31с : D3–6. DOI : 10.1016 / j.vaccine.2013.02.030 . PMID 23973344 .
- ^ Lopez Састр J, Fernandez Colomer B, Кото Cotallo Gil D, члены "Grupo де Hospitales Кастрилльо" (2009). «Неонатальный сепсис вертикальной передачи. Эпидемиологическое исследование от„Grupo де Hospitales Кастрилльо “ ». Раннее человеческое развитие . 85 (10): S100. DOI : 10.1016 / j.earlhumdev.2009.08.049 .CS1 maint: multiple names: authors list (link)
- ^ Андреу А, Санфелиу I, Виньяс Л., Барранко М, Бош Дж, Допико Е, Гуарда С, Джункоса Т, Лайт J, Матас Л, Санчес Ф, Сьерр М; Grupo de Microbiólogos pare el Esduio de las Infecciones de Transmissión Vertical, Societat Catalana de Malalties Infeccioses i Microbiologia Clínica, статья на испанском языке. (2003). "Declive de la incidencia de la sepsis perinatal por estreptococo del grupo B (Barcelona 1994-2001). Relación con las políticas profilácticas Снижение заболеваемости перинатальным стрептококком группы B (Барселона, 1994-2002). Связь с политикой больничной профилактики" (PDF) . Enfermedades Infecciosas y Microbiologia Clinica . 21 (4): 174–179. DOI : 10.1157 / 13045447 . Архивировано из оригинал (PDF) от 23 февраля 2016 г.CS1 maint: multiple names: authors list (link)
- ^ Albouy-Llaty, Марион; Надо, Седрик; Декомб, Эммануэль; Пьер, Фабрис; Мигеот, Вирджиния (2011). «Улучшение перинатального скрининга стрептококков группы B с помощью индикаторов процесса». Журнал оценки в клинической практике . 18 (4): 727–733. DOI : 10.1111 / j.1365-2753.2011.01658.x . PMID 21414110 .
- ^ Сил AC, Бьянки-Джассир F, Рассел NJ, Коли-Линч M, Танн CJ, Холл J, Мадрид L, Бленкоу H, Cousens S, Бейкер CJ, Бартлетт L, Катленд C, Gravett MG, Heath PT, Ip M, Ле Доар К., Мадхи С.А., Рубенс К.Э., Саха С.К., Шраг С.Дж., Собанджо-Тер Меулен А., Векеманс Дж., Лаун Дж. Э. (2017). «Оценка бремени стрептококковой инфекции группы B во всем мире для беременных женщин, мертворожденных и детей» . Клинические инфекционные болезни . 65 (приложение 2) (приложение 2): S200-209. DOI : 10,1093 / CID / cix664 . PMC 5849940 . PMID 29117332 . CS1 maint: multiple names: authors list (link)
- ^ Benitz WE, Гулд JB, Друзин ML (1999). «Факторы риска для стрептококкового сепсиса группы B с ранним началом: оценка отношения шансов путем критического обзора литературы» . Педиатрия . 103 (6): e77. DOI : 10.1542 / peds.103.6.e77 . PMID 10353974 .
- ^ Хит, Пол Т; Бальфур, Гейл; Weisner, Abbie M; Эфстратиу, Андрулла; Lamagni, Theresa L; Тиге, Хелен; О'Коннелл, Лиам А.Ф.; Кафферки, Мэри; и другие. (2004). «Стрептококковая инфекция группы B у детей младше 90 дней в Великобритании и Ирландии». Ланцет . 363 (9405): 292–294. DOI : 10.1016 / S0140-6736 (03) 15389-5 . PMID 14751704 . S2CID 22371160 .
- ^ Отчет об охране здоровья Vol. 5 № 46 - 18 ноября 2011 г. ·. «Пиогенная и непиогенная стрептококковая бактериемия, Англия, Уэльс и Северная Ирландия: 2010» . Отчет по охране здоровья . Архивировано из оригинального 14 июля 2014 года . Проверено 11 января +2016 .
- Перейти ↑ Cromwell D, Joffe T, van der Meulen J, Dhillon C, Hughes R, Murphy D (2007). Профилактика стрептококковой инфекции группы B с ранним началом у новорожденных в акушерских отделениях Великобритании (PDF) . Королевский колледж акушеров и гинекологов и Лондонская школа гигиены и тропической медицины. ISBN 978-1-904752-37-0. Проверено 11 января +2016 .
- ^ RCOG. «Аудит существующей практики профилактики стрептококковой инфекции группы B с ранним началом у новорожденных в Великобритании» (PDF) . Дата обращения 2 февраля 2016 .
- ^ GBS Support UK & RCOG (декабрь 2017 г.). «Стрептококк группы B (GBS) у беременных и новорожденных» (PDF) . Архивировано из оригинального (PDF) 22 декабря 2017 года . Проверено 25 ноября 2019 года .
- ^ Справочный сайт по домашним родам. «Стрептококковая инфекция группы B и домашние роды» . Проверено 11 января +2016 .
- ^ Скрининг на инфекции. 1.8.9 Стрептококк группы B. «Дородовая помощь при неосложненной беременности. Рекомендации NICE [CG62]: март 2008 г.» . Национальный институт здравоохранения и медицинского обслуживания NICE . Проверено 27 ноября 2019 года .
- ^ Рекомендации NICE [CG149], август 2012 г. «Неонатальная инфекция: антибиотики для профилактики и лечения. 1.3 Антибиотики во время родов» . Национальный институт здоровья и ухода NICE . Проверено 27 ноября 2019 года .
- ^ Национальный комитет Великобритании по отбору. «Текущий NSC Великобритании от Национального комитета Великобритании по отбору (UK NSC)» . Дата обращения 19 ноября 2019 .
- ^ «Ведущий ребенок благотворительности опустошенного решения не вводить спасательный скрининг беременных women.2012» . campaign-archive2.com . Проверено 30 ноября 2019 года .
- ^ Центры по контролю и профилактике заболеваний - CDC, MMWR (2002). «Пересмотренное руководство по профилактике перинатальных стрептококковых заболеваний группы B от CDC. 2002» . Еженедельный отчет о заболеваемости и смертности . 51-RR11: 1–22 . Проверено 11 января +2016 .
- ^ CDC. «Рекомендации по профилактике. Обновление рекомендаций 2019 г.» . Проверено 26 ноября 2019 .
- ^ Пуополо К.М., Линфилд Р., Каммингс Дж. Дж.; КОМИТЕТ ПО ПЛОДУ И НОВОРОЖДЕННЫМ; КОМИТЕТ ПО ИНФЕКЦИОННЫМ ЗАБОЛЕВАНИЯМ. (2019). «Ведение младенцев с риском стрептококковой инфекции группы B» (PDF) . Педиатрия . 144 (2): e20191881. DOI : 10.1542 / peds.2019-1881 . PMID 31285392 . S2CID 195843897 . Проверено 25 ноября 2019 года . CS1 maint: multiple names: authors list (link)
- ^ Деньги D, Аллен В.М. (2018). "№ 298 - Профилактика неонатальной инфекции при стрептококках группы B d'apparition précoce". Журнал акушерства и гинекологии Канады . 40 (8): e675 – e686. DOI : 10.1016 / j.jogc.2018.05.033 . PMID 30103892 .
- ^ Alos Кортес СО, Андреу Доминго А, Аррибас Мир л, Cabero Roura л, КУЭТО Лопес М, Лопес Састр J, Мелчор Маркос JC, Пуэртас Прито А, де ла Росу Фрайле М, Сальсед Abizanda S, Санчес Луна М, Санчес Перес МДж , Торрехон Кардосо Р. (2012). "Prevención de la infoccion perinatal por estreptococo del grupo B. Recomendaciones españolas revisadas 2012" (PDF) . Revista Espanola de Quimioterapia . 25 (1): 79–88. PMID 22488547 . Проверено 25 ноября 2019 года . CS1 maint: multiple names: authors list (link)
- ^ Surbek D.Kommission für Qualitätssicherung дер SGGG / gynécologie Свисс (2007). "Prophylaxe der frühen Neugeborenensepsis durch Streptokokken der Gruppe B - Профилактика раннего неонатального сепсиса с помощью GBS" . Gynäkologisch-geburtshilfliche Rundschau . 47 (2): 103–104. DOI : 10.1159 / 000100342 . PMID 17440274 . S2CID 77887846 .
- ^ Leitlinien дер Gesellschaft für Neonatologie унд Pädiatrische Intensivmedizin (ГИЯЭ) Deutschen Gesellschaft für Gynäkologie унд Geburtshilfe, Deutschen Gesellschaft für Pädiatrische Infektiologie (DGPI), унд Германское общество Perinatale Medizin (ДУПЖ). «Профилактика Neugeborensepsis - frühe Form - durch Streptokokken der Gruppe B - Профилактика неонатального сепсиса - ранняя форма - GBS» (PDF) . Проверено 30 ноября 2019 года . CS1 maint: multiple names: authors list (link)
- ^ Kotarski Дж, Heczko РВ, Лаутербах Р, Т Niemiec, Leszczyńska- Gorzelak В (2008). «Rekomendacje polskiego towarzystwa ginekologicznego dotyczące wykrywania nosicielstwa paciorkowców grupy B (GBS) u kobiet w ciąży i zapobiegania zakażeniombor u noworodków - Рекомендации Польского гинекологического общества для выявления носителей инфекции у беременных женщин и женщин-гинекологов». Ginekol Pol . 79 : 221–223.
- ^ А. Мехурова; В. Унцайтиг; Я. Машата; П. Швиховец (2013). «Диагностика и лечение стрептококка скупины Б в тeхотенции за породу - допущенный поступок --- Диагностика и лечение СГБ во время беременности и родов - Рекомендации» (PDF) . Клин Микробиол Инфекц Лек . 12 : 11–14.
- Перейти ↑ Agence Nationale d'Accreditation et d'Evaluation en Santé (2001). "Anténatale Prevention du Risktieux Bactérien néonatal précoce.2001" (PDF) . Проверено 25 ноября 2019 года .
- ^ Бельгийский совет здравоохранения. «Профилактика перинатальных стрептококковых инфекций группы В. Рекомендации. 2003» (PDF) . Проверено 25 ноября 2019 года .
- ^ Nederlandse Vereniging voor Obstetrie en Gynaecologie. "2008. ПРОФИЛАКТИКА НЕОНАТАЛЕ ГРУПП-Б-СТРЕПТОКОККЕНЗИЕКТЕ (GBS-ZIEKTE) Версия 2.0" (PDF) . Проверено 25 ноября 2019 года .
- ^ Министерио де Салуд де ла Насьон. Dirección Nacional de Salud Materno Infantil. Аргентина, на испанском языке. «Рекомендации по профилактике, диагностике и лечению инфекций новорожденных от Estreptococo β Hemolítico del Grupo B (EGB). Рекомендации по профилактике, диагностике и лечению ранней неонатальной инфекции, вызванной Streptococcus β гемолитической группой B (GBS)» (PDF) . Проверено 29 ноября 2019 .
- ^ Материнство Квинсленда; Клинические рекомендации для новорожденных. «Раннее начало стрептококковой болезни группы B» (PDF) . Проверено 29 ноября 2019 .
- ^ Королевский колледж акушеров и гинекологов Австралии и Новой Зеландии. РАНЦКОГ. «Streptococcus (GBS) при беременности: скрининг и ведение. Июль 2019 г.» » (PDF) . Проверено 25 ноября 2019 года .
- ^ Раабе В.Н., Шейн А.Л. (2019). Стрептококк группы В (Streptococcus agalactiae) . Спектр микробиологии . 7 . С. 228–238. DOI : 10.1128 / microbiolspec.GPP3-0007-2018 . ISBN 9781683670124. PMC 6432937 . PMID 30900541 .
- ^ Фарли MM. (2001). «Стрептококковая болезнь группы B у небеременных взрослых» (PDF) . Клинические инфекционные болезни . 33 (4): 556–561. DOI : 10.1086 / 322696 . PMID 11462195 .
- ^ Эдвардс MS ,. Бейкер CJ. (2005). «Стрептококковые инфекции группы B у пожилых людей» (PDF) . Клинические инфекционные болезни . 41 (6): 839–847. DOI : 10.1086 / 432804 . PMID 16107984 .
- ^ Скофф TH, Фарли MM, Пети S, Крейг А.С., Шаффнер W, Гершман K, Харрисон LH, Линфилд R, Мохле-Боэтани J, Зански S, Альбанезе BA, Стефонек K, Зелл ER, Джексон D, Томпсон T, Шраг SJ (2009). «Увеличение бремени инвазивной стрептококковой инфекции группы B у небеременных взрослых, 1990–2007 годы» (PDF) . Клинические инфекционные болезни . 49 (1): 85–92. DOI : 10.1086 / 599369 . PMID 19480572 .
- ^ Аль Ахрасс Ф, Абдалла Л, Бергер С, Ханна Р, Рейнольдс Н, Томпсон С, Халлит Р, Шливерт PM. (2013). «Streptococcus agalactiae токсический шок-подобный синдром: два клинических случая и обзор литературы» . Медицина . 92 (1): 10–14. DOI : 10.1097 / MD.0b013e31827dea11 . PMC 5370747 . PMID 23263717 . CS1 maint: multiple names: authors list (link)
- ^ Поддержка Strep группы B (GBSS). «На главную» Примите участие »Кампания» Месяц осведомленности о стрептококках группы B Месяц осведомленности о стрептококках группы B " . Проверено 25 ноября 2019 года .
- ^ "Добро пожаловать" .
- ^ Джордан Х.Т., Фарли М.М., Крейг А., Моле-Боэтани Дж., Харрисон Л.Х., Пети С., Линфилд Р., Томас А., Зански С., Гершман К., Альбанезе Б.А., Шаффнер В., Шраг С.Дж.; Активный эпиднадзор за основными бактериями (ABCs) / Сеть программ по возникающим инфекциям, CDC (2008). «Возвращаясь к необходимости вакцинопрофилактики позднего неонатального стрептококкового заболевания группы B: многоступенчатый популяционный анализ» . Журнал детских инфекционных болезней . 27 (12): 1057–1064. DOI : 10.1097 / inf.0b013e318180b3b9 . PMID 18989238 . S2CID 1533957 . CS1 maint: multiple names: authors list (link)
- ^ Эдвардс MS, Ренч MA, Rinaudo CD, Fabbrini M, Tuscano G, Buffi G, Bartolini E, Bonacci S, Baker CJ, Margarit I (2016). «Иммунные ответы на инвазивную стрептококковую болезнь группы B у взрослых» . Возникающие инфекционные заболевания . 22 (11): 1877–1883. DOI : 10.3201 / eid2211.160914 . PMC 5088039 . PMID 27767008 .
- ^ «Техническая дорожная карта исследований и разработок вакцины GBS и предпочтительные характеристики продуктов ВОЗ» . Всемирная организация здравоохранения . Проверено 30 ноября 2019 года .
- ^ «Инфекция Streptococcus группы B ежегодно вызывает около 150 000 предотвратимых мертворождений и младенческих смертей» . Всемирная организация здравоохранения . 6 ноября 2017 . Проверено 30 ноября 2019 года .
- ^ a b Бейкер CJ, Кэри VJ, Rench MA, Edwards MS, Hillier SH, Kasper DL, Platt R (2014). «Материнские антитела при родах защищают новорожденных от стрептококковой инфекции группы B с ранним началом» (PDF) . Журнал инфекционных болезней . 209 (5): 781–788. DOI : 10.1093 / infdis / jit549 . PMC 3923540 . PMID 24133184 .
- ^ Родригес-Грейнджер J, Альваргонзалес JC, Берарди A, Бернер R, Кунце M, Hufnagel M, Melin P, Decheva A, Orefici G, Poyart C, Telford J, Efstratiou A, Killian M, Krizova P, Baldassarri L, Spellerberg B , Пуэртас А, Роза-Фрайле М (2012). «Еще раз о профилактике неонатальных заболеваний, вызванных стрептококками группы B. Европейский проект DEVANI» . Европейский журнал клинической микробиологии и инфекционных заболеваний . 31 (9): 2097–2114. DOI : 10.1007 / s10096-012-1559-0 . PMID 22314410 . S2CID 15588906 .
- ^ а б Эдвардс MS, Гоник Б (2013). «Предотвращение широкого спектра перинатальной заболеваемости и смертности с помощью вакцинации против стрептококков группы B». Вакцина . 31С : D66–71. DOI : 10.1016 / j.vaccine.2012.11.046 . PMID 23200934 .
- ^ Мадхи, Шабир А; Катленд, Клэр Л; Хосе, Лиза; Коэн, Антонет; Говендер, Ниреша; Виттке, Фредерик; Олугбоси, Морунфолу; Меулен, Аджоке Собанджо-тер; Бейкер, Шеррил; Скучный, Питер М; Нарасимхан, Вас; Слобод, Карен (2016). «Безопасность и иммуногенность исследуемой материнской трехвалентной вакцины против стрептококка группы B у здоровых женщин и их младенцев: рандомизированное испытание фазы 1b / 2». Ланцетные инфекционные болезни . 16 (8): 923–934. DOI : 10.1016 / S1473-3099 (16) 00152-3 . ISSN 1473-3099 . PMID 27139805 .
- ^ a b Хит PT. (2016). «Статус исследования вакцины и разработки вакцин для GBS» . Вакцина . 34 (26): 2876–2879. DOI : 10.1016 / j.vaccine.2015.12.072 . PMID 26988258 .
- ↑ Song JY, Lim JH, Lim S, Yong Z, Seo HS (2018). «Прогресс в направлении вакцины против стрептококка группы B» . Человеческие вакцины и иммунотерапевтические препараты . 14 (11): 2669–2681. DOI : 10.1080 / 21645515.2018.1493326 . PMC 6314413 . PMID 29995578 . CS1 maint: multiple names: authors list (link)
- ^ Риа, Франческо; Гупалова, Т .; Леонтьева, Г .; Крамская, Т .; Грабовская, К .; Бормотова, Е .; Коржевский, Д .; Суворов, А. (2018). «Разработка экспериментальной вакцины GBS для иммунизации слизистых оболочек» . PLOS ONE . 13 (5): e0196564. Bibcode : 2018PLoSO..1396564G . DOI : 10.1371 / journal.pone.0196564 . ISSN 1932-6203 . PMC 5935385 . PMID 29727446 .
- ^ Nuccitelli А, Ринаудо компакт - диск, Maione D (2015). «Вакцина против стрептококка группы B: современное состояние» . Терапевтические достижения в вакцинах . 3 (3): 76–90. DOI : 10.1177 / 2051013615579869 . PMC 4530403 . PMID 26288735 .
- ^ Дэвис HG, Каррерас-Абад C, Le Doare K, Heath PT. (2019). «Стрептококк группы B: испытания и невзгоды» (PDF) . Журнал детских инфекционных болезней . 38 (6S Дополнение 1.) (6S Дополнение 1): S72-76. DOI : 10.1097 / INF.0000000000002328 . PMID 31205250 . CS1 maint: multiple names: authors list (link)
- ^ Деланных СМ, Crumlish М, Фонтэн МС, Поллок Дж, Фостер G, Dagleish М.П., Тернбуллы ДФ, Zadoks РН (2013). «Штаммы Human Streptococcus agalactiae у водных млекопитающих и рыб» . BMC Microbiology . 13 : 41. DOI : 10,1186 / 1471-2180-13-41 . PMC 3585737 . PMID 23419028 .
- ^ Ruegg PL (2017). «100-летний обзор: выявление, лечение и профилактика мастита» . Журнал молочной науки . 100 (12): 10381–10397. DOI : 10.3168 / jds.2017-13023 . PMID 29153171 . Проверено 29 ноября 2019 .
- ^ Киф GP (1997). «Streptococcus agalactiae мастит: обзор» . Может. Вет. Дж . 38 : 429–37. PMC 1576741 . PMID 9220132 .
- ^ Evans JJ, Klesius PH, Pasnik DJ, Bohnsack JF (2009). «Изолят Streptococcus agalactiae человека в нильской тилапии (Oreochromis niloticus)» . Возникающие инфекционные заболевания . 15 (5): 774–776. DOI : 10.3201 / eid1505.080222 . PMC 2687030 . PMID 19402966 .
- Перейти ↑ Liu G, Zhang W, Lu C (2013). «Сравнительный геномный анализ Streptococcus» . BMC Genomics . 14 : 775. DOI : 10.1186 / 1471-2164-14-775 . PMC 3831827 . PMID 24215651 .
- ^ Ли LP, Ван Р, Лян WW1, Хуанг Т1, Хуан И2, Ло Ф.Г., Лэй А.Й., Чен М., Ган X (2015). «Разработка живой ослабленной вакцины Streptococcus agalactiae от тилапии путем непрерывного пассажа in vitro». Иммунология рыб и моллюсков . 45 (2): 955–963. DOI : 10.1016 / j.fsi.2015.06.014 . PMID 26087276 . CS1 maint: multiple names: authors list (link)
- ↑ Zhang D, Gao Y, Li Q, Ke X, Liu Z, Lu M, Shi C. (2019). «Эффективная живая аттенуированная вакцина против инфекции Streptococcus agalactiae в выращиваемой нильской тилапии (Oreochromis niloticus)». Иммунология рыб и моллюсков . S1050-4648: 31087–3. DOI : 10.1016 / j.fsi.2019.11.044 . PMID 31751658 . CS1 maint: multiple names: authors list (link)
Внешние ссылки [ править ]
- Британская ассоциация стрептококков группы B
- CDC — Стрептококковая инфекция группы B (GBS)
| Классификация | D
|
|---|---|
| Внешние ресурсы |
|