Пентакарбонилгидридомарганец
 | |
 | |
| Имена | |
|---|---|
| Другие имена Пентакарбонилманганат водорода (-I) (7Cl); Марганец, пентакарбонилгидро- (8Cl); Пентакарбонил гидридомарганца; Гидридопентакарбонилмарганец; Пентакарбонилгидрид марганца; Пентакарбонилгидромарганец; Пентакарбонилмагидрид | |
| Идентификаторы | |
| |
3D модель ( JSmol ) | |
| ChemSpider | |
PubChem CID | |
| |
| |
| Характеристики | |
| HMn (CO) 5 | |
| Молярная масса | 195,99799 г / моль |
| Появление | При комнатной температуре он жидкий и бесцветный. Ниже его точки плавления он может быть сублимирован в вакууме. [1] |
| Кислотность (p K a ) | 7.1 |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
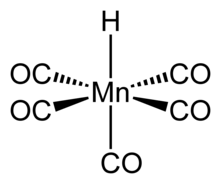
Пентакарбонилгидридомарганец представляет собой металлоорганическое соединение с формулой HMn (CO) 5 . Это соединение является одним из наиболее стабильных гидридов переходных металлов «первого ряда» .
Подготовка
Впервые об этом было сообщено в 1931 году. [2] Из нескольких способов получения этого соединения [3] - протонирование пентакарбонил-манганат-аниона. Последний образуется при восстановлении декакарбонила диманганца , (Mn (CO) 5 ) 2 . Реакция показана ниже.
- LiHB (C 2 H 5 ) 3 ( супергидрид ) + ½ Mn 2 (CO) 10 → Li [Mn (CO) 5 ] + ½ H 2 + (C 2 H 5 ) 3 B
- Li [Mn (CO) 5 ] + CF 3 SO 3 H → HMn (CO) 5 + Li+
CF 3 SO 3-
Соли [Mn (CO) 5 ]-
может быть выделен в виде кристаллического PPN+
(μ-nitrido-бис- (triphenylphosphorus)) соль, которая плавно протонированная с помощью CF 3 SO 3 H . [3]
- PPN [Mn (CO) 5 ] + CF 3 SO 3 H → HMn (CO) 5 + PPN+
CF 3 SO 3-
Это соединение также может быть образовано реакцией раствора пентакарбонил (триметилсилил) марганца с водой. [4] Реакция показана ниже.
- 2 (CO) 5 MnSiMe 3 + H 2 O → HMn (CO) 5 + Me 3 SiOSiMe 3
Структура и свойства
Соединение имеет октаэдрическую симметрию [5], а его молекулярная точечная группа - C 4v . [6] H-Мп длина связи составляет 1,44 ± 0,03 Å. [6] Исследование дифракции электронов в газовой фазе подтверждает эти данные.
Структура HMn (CO) 5 изучено многими методами , включая дифракции рентгеновских лучей , дифракции нейтронов и дифракции электронов . [6] HMn (CO) 5 может быть связан со структурой гексакарбонильного комплекса, такого как Mn (CO).+
6, и поэтому обладает следующими аналогичными свойствами. [7] Занятые молекулярные орбитали наверху - это орбитали 2 t 2g . Они характеризуются как металлические 3d π орбитали. Поскольку разрыхляющие 2π-орбитали взаимодействуют с карбонильными группами (или в данном случае H-
) орбиталь t 2g стабилизируется по сравнению с орбиталью 3d π , что, в свою очередь, вызовет изменения в сигма- и пи-взаимодействиях.
Основные реакции
РК из HMn (CO) 5 в воде составляет 7,1. [8] Таким образом , по кислотности он сравним с сероводородом , обычной неорганической кислотой.
Обычной реакцией с участием разновидностей HMn (CO) 5 является замещение лигандов CO органофосфинами , что происходит как термически, так и фотохимически. [9] Таким образом, следующие производные образуют MnH (CO) 3 P 2 , MnH (CO) 2 P 3 и MnH (CO) P 4 , (где P = P (OEt) 3 , PPh (OEt) 2 , PPh 2 OEt, PPh (OiPr) 2 ).
Соединение HMn (CO) 5 можно использовать для восстановления олефинов и других органических соединений, а также галогенидов металлов. [3]
Это соединение можно метилировать диазометаном . [1]
- HMn (CO) 5 + CH 2 N 2 → Mn (CO) 5 CH 3 + N 2
Примечания
- ^ а б Элей, ДД; Сосны, Герман; Вайс, П.Б. Достижения в области катализа . 32. 385. ISBN 978-0-12-007832-5
- ^ Hieber, W. Leutert, F. Naturwissenschaften . 1931. 360.
- ^ a b c Хантер, Алан Д.; Бьянкони, Ларри Дж; DiMuzio, Стивен Дж; Брахо, Дайан Л. Синтез и взаимосвязь между структурой и свойством в химии η6-арена) Cr (CO) 3: от управляемых экспериментов до открытий. J. Chem. Educ. 75. 1998. 891. DOI : 10.1021 / ed075p891
- ^ Финн, MG Пентакарбонил (триметилсилил) марганец. Энциклопедия реагентов для органического синтеза . DOI : 10.1002 / 047084289X.rp022s
- ^ Лю, Сянь-мэй; Ван, Чао-янь; Цянь-шу; Се; Yaoming; Кинг, Р. Брюс; Шефер, Генри Ф., III. Одноядерные и биядерные карбонилгидриды марганца. Dalton Trans. , 2009, 3774-3785, DOI : 10.1039 / b822913a
- ^ a b c Куколич С.Г. Микроволновый спектр и молекулярная структура пентакарбонилгидрида марганца. 33. 1994. 1217-1219.
- ^ Фенске, Ричард. Электронная структура и связь в пентакарбонилгалогенидах и гидриде марганца. Неорганическая химия . 9. 1970. 1053-1060.
- ^ Моррис, Роберт Х. (2016-08-10). "Кислотная сила Бренстеда – Лоури металлогидридных и дигидрогенных комплексов". Химические обзоры . 116 (15): 8588–8654. DOI : 10.1021 / acs.chemrev.5b00695 . hdl : 1807/78047 . ISSN 0009-2665 . PMID 26963836 .
- ^ Альбертин, Габриэле. Катионные молекулярно-водородные комплексы Mn (I). Металлоорганические соединения. 16. 1997. 4959-4969.
- Карбонильные комплексы
- Органические соединения марганца
- Гидриды металлов