Гидросилилирование
Гидросилилирование , также называемое каталитическим гидросилированием , описывает добавление связей Si-H через ненасыщенные связи . [1] Обычно реакция проводится каталитически, и обычно субстратами являются ненасыщенные органические соединения . Алкены и алкины дают алкил- и винилсиланы ; альдегиды и кетоны дают простые силиловые эфиры. Гидросилилирование называют «наиболее важным применением платины в гомогенном катализе». [2]
Объем и механизм
Гидросилилирование алкенов представляет собой коммерчески важный метод получения кремнийорганических соединений . Процесс механически аналогичен гидрированию алкенов. Фактически, подобные катализаторы иногда используются для двух каталитических процессов.
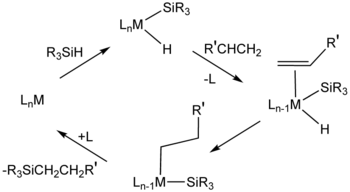
Преобладающий механизм, называемый механизмом Чока-Харрода , предполагает промежуточный комплекс металла, который содержит гидрид , силильный лиганд (R 3 Si) и алкеновый субстрат. Окислительное присоединение происходит за счет взаимодействия сигма-комплекса , в котором связь Si-H не полностью разорвана.
Гидросилилирование алкенов обычно происходит через антимарковниковское присоединение , т. Е. Кремний размещается у концевого атома углерода при гидросилилировании концевого алкена [1]. Существуют вариации механизма Чалка-Харрода. В некоторых случаях происходит внедрение алкена в связь M-Si с последующим восстановительным отщеплением, что противоположно последовательности в механизме Чалка-Харрода. В некоторых случаях гидросилилирование приводит к виниловым или аллильным силанам в результате отщепления бета-гидрида . [3]
Алкины также подвергаются гидросилилированию, например, добавлению триэтилсилана к дифенилацетилену : [4]
- Et 3 SiH + PhC≡CPh → Et 3 Si (Ph) C = CH (Ph)
Асимметричное гидросилилирование
Используя хиральные фосфины в качестве спектральных лигандов , были разработаны катализаторы для каталитического асимметричного гидросилирования. Хорошо изученной реакцией является добавление трихлорсилана к стиролу с образованием 1-фенил-1- (трихлорсилил) этана:
- Cl 3 SiH + PhCH = CH 2 → (Ph) (CH 3 ) CHSiCl 3
Почти идеальная энантиоселективность (ее) может быть достигнута с использованием палладиевых катализаторов, поддерживаемых бинафтилзамещенными монофосфиновыми лигандами. [5]
Гидросилилирование поверхности
Кремниевые пластины можно протравить в плавиковой кислоте (HF), чтобы удалить естественный оксид и сформировать поверхность кремния с концевыми водородными группами . Поверхности с концевыми водородными группами подвергаются гидросилированию ненасыщенными соединениями (такими как концевые алкены и алкины) с образованием стабильного монослоя на поверхности. Например:
- Si- H + H 2 C = CH (CH 2 ) 7 CH 3 → Si-CH 2 CH H - (CH 2 ) 7 CH 3
Реакция гидросилилирования может быть инициирована УФ-светом при комнатной температуре или нагреванием (типичная температура реакции 120-200 ° C) в условиях отсутствия влаги и кислорода. [6] Полученный монослой, который является стабильным и инертным, препятствует окислению основного кремниевого слоя, что актуально для различных приложений устройств. [7]
Катализаторы
До введения Шпейером платиновых катализаторов гидросилилирование не практиковалось широко. Процесс, катализируемый пероксидом, был описан в академической литературе в 1947 году [8], но введение катализатора Шпейера ( H 2 PtCl 6 ) было большим прорывом.
Позже был введен катализатор Карстедта . Это липофильный комплекс, растворимый в органических субстратах, представляющих промышленный интерес. [9] Комплексы и соединения, катализирующие гидрирование, часто являются эффективными катализаторами гидросилилирования, например катализатор Уилкинсона .
использованная литература
- ^ a b «Гидросилилирование - всесторонний обзор последних достижений» Б. Марчинец (редактор), «Достижения в науке о кремнии», Springer Science, 2009. doi : 10.1007 / 978-1-4020-8172-9
- ^ Реннер, H .; Schlamp, G .; Kleinwächter, I .; Drost, E .; Lüschow, HM; Tews, P .; Panster, P .; Diehl, M .; Lang, J .; Kreuzer, T .; Knödler, A .; Starz, KA; Dermann, K .; Rothaut, J .; Дризельман, Р. (2002). «Металлы и соединения платиновой группы». Энциклопедия промышленной химии Ульмана . Вайли. DOI : 10.1002 / 14356007.a21_075 .
- ^ Troegel, D .; Сторер, Дж. (2011). "Последние достижения и актуальные проблемы гидросилилирования олефинов, катализируемого поздними переходными металлами, с промышленной точки зрения". Coord. Chem. Ред . 255 : 1440–1459. DOI : 10.1016 / j.ccr.2010.12.025 .
- ^ Джеймс Л. Фрай, Рональд Дж. Рахайм-младший, Роберт Е. Малецка-младший «Триэтилсилан», Энциклопедия реагентов для органического синтеза , John Wiley & Sons , 2007. doi : 10.1002 / 047084289X.rt226.pub2
- ^ Hayashi, T .; Ямасаки, К. (2007). «Формирование связи C – E посредством асимметричного гидросилилирования алкенов». В Крэбтри, Роберт Х .; Д. Майкл П. Мингос (ред.). Комплексная металлоорганическая химия III . Амстердам: Эльзевир. DOI : 10.1016 / B0-08-045047-4 / 00140-0 . ISBN 978-0-08-045047-6.
- ^ "Фотореактивность ненасыщенных соединений с кремнием с концевыми водородными группами (111)", RL Cicero, MR Linford, CED Chidsey, Langmuir 16, 5688-5695 (2000)
- ^ Прямое электрическое обнаружение гибридизации ДНК на ДНК-модифицированных кремниевых поверхностях, W.Cai, J. Peck, D. van der Weide и RJ Hamers, Biosensors and Bioelectronics 19, 1013-1019 (2004)
- ^ Sommer, L .; Pietrusza, E .; Уитмор, Ф. "Добавление трихлорсилана к 1-октену, катализируемое пероксидом". Варенье. Chem. Soc . 69 (1): 188. DOI : 10.1021 / ja01193a508 .
- ^ С. Elschenbroich, Organometallics (2006) Wiley и Sons-VCH: Weinheim. ISBN 978-3-527-29390-2
дальнейшее чтение
Книги
- Прикладной гомогенный катализ металлоорганическими соединениями: подробный справочник: приложения, разработки. Бой Корнилс; WA Herrmann. Издатель: Weinheim; Нью-Йорк: Wiley-VCH, 2000.
- Подробное руководство по гидросилилированию. Богдан Марцинец. Издательство: Оксфорд [ua]: Pergamon Press, 1992.
- Комплексы родия как катализаторы гидросилилирования. Н.К. Скворцов. // Родий Экспресс. 1994. № 4 (май). С. 3 - 36 (англ.). [1] ISSN 0869-7876
Статьи
- «Алкильные монослои на кремнии, полученные из 1-алкенов и кремния с концевыми водородными группами», MR Linford, P. Fenter, PM Eisenberger и CED Chidsey, J. Am. Chem. Soc. 117, 3145-3155 (1995).
- «Синтез и характеристика ДНК-модифицированных поверхностей Si (111)», T. Strother, W. CAi, X. Zhao, RJ Hamers и LM Smith, J. Am. Chem. Soc. 122, 1205-1209 (2000).
- "Т. Стротер, Р. Дж. Хамерс и Л. М. Смит," Химия поверхности ковалентного прикрепления ДНК к поверхности кремния (100) ". Langmuir, 2002, 18, 788-796.
- «Ковалентно модифицированные поверхности кремния и алмаза: устойчивость к неспецифической адсорбции белка и оптимизация для биочувствительности», TL Lasseter, BH Clare, NL Abbott и RJ Hamers. Варенье. Chem. Soc. 2004, 126, 10220-10221.
- Кремний
- Наука о поверхности