 | |
| Имена | |
|---|---|
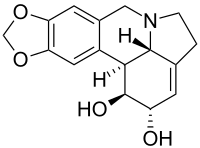
| Название ИЮПАК 1,2,4,5,12b, 12c-Гексагидро-7 H - [1,3] диоксоло [4,5-j] пирроло [3,2,1- де ] фенантридин-1,2-диол | |
| Другие имена Галантидин, Амариллин, Нарциссин, Ликорин, Беламарин | |
| Идентификаторы | |
3D модель ( JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100,006,822 |
PubChem CID | |
| UNII | |
Панель управления CompTox ( EPA ) | |
| |
| |
| Характеристики | |
| C 16 H 17 N O 4 | |
| Молярная масса | 287,315 г · моль -1 |
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Ликорин - токсичный кристаллический алкалоид, обнаруженный в различных видах Amaryllidaceae , таких как культивируемая кустовая лилия ( Clivia miniata ), лилии-сюрпризы ( Lycoris ) и нарциссы ( Нарцисс ). Он может быть очень ядовитым или даже смертельным при проглатывании в определенных количествах. [1] Тем не менее, он иногда используется в лечебных целях, поэтому некоторые группы могут собирать очень популярную Clivia miniata .
Источник [ править ]
Ликорин содержится в различных видах Amaryllidaceae, включая цветы и луковицы нарциссов, подснежника ( Galanthus ) или лилии паука ( Lycoris ). Ликорин - самый частый алкалоид Amaryllidaceae . [2]
Самая ранняя диверсификация Amaryllidaceae, скорее всего, произошла в Северной Африке и на Пиренейском полуострове, и этот ликорин является одним из старейших в биосинтетическом пути алкалоидов Amaryllidaceae. [3]
Механизм действия [ править ]
В настоящее время очень мало известно о механизме действия ликорина. Существуют предварительные идеи о том, как метаболизируется ликорин, благодаря исследованию, проведенному на собаках породы бигль . [4]
Ликорин ингибирует синтез белка , [5] и может ингибировать аскорбиновую кислоту биосинтез , хотя исследования последнего противоречивы и неубедительны. В настоящее время он представляет определенный интерес для изучения некоторых дрожжей , основного организма, на котором тестируется ликорин. [6]
Известно, что ликорин слабо ингибирует ацетилхолинэстеразу (АХЭ) и биосинтез аскорбиновой кислоты. [7] Было обнаружено, что IC50 ликорина варьирует между различными видами, в которых он может быть найден, но общий вывод из экспериментов с ликорином заключался в том, что он оказывает некоторое влияние на ингибирование AChE. [8]
Ликорин проявляет цитостатические эффекты, воздействуя на актиновый цитоскелет, а не индуцируя апоптоз в раковых клетках, хотя было обнаружено, что ликорин вызывает апоптоз на разных стадиях клеточного цикла. [9]
Биосинтез [ править ]
Один из возможных вариантов синтеза ликорина может происходить из O-метилнорбелладина , который можно увидеть на изображении справа.
Токсичность [ править ]
Отравление ликорином обычно происходит при попадании в организм луковиц нарциссов. Луковицы нарциссов иногда путают с луком , что приводит к случайному отравлению. [10]
В исследовании дозировки, используемой на собаках породы гончая, первые признаки тошноты наблюдались уже при дозе 0,5 мг / кг и возникали в течение 2,5 часов. Эффективная доза, вызывающая рвоту у собак, составляла 2,0 мг / кг и действовала не более 2,5 часов после введения. [11]
Симптомы [ править ]
Симптомами отравления ликорином являются тошнота , [12] рвота , диарея и судороги . [13]
Текущее исследование [ править ]
Было замечено, что ликорин обладает многообещающими биологическими и фармакологическими свойствами, такими как антибактериальные, противовирусные или противовоспалительные эффекты, а также может иметь противораковые свойства. [14] Он продемонстрировал различные ингибирующие свойства по отношению к множеству линий раковых клеток, включая лимфому, карциному, множественную миелому, меланому, лейкоз, немелкоклеточный рак легкого человека A549, рак пищевода OE21 человека и другие. [15]
Ликорин имеет много производных, используемых для противораковых исследований, таких как гидрохлорид ликорина (ЛГ), который является новым средством против рака яичников, и данные показали, что ЛГ эффективно ингибирует митотическую пролиферацию клеток Hey1B с очень низкой токсичностью. Этот препарат может быть использован для эффективной терапии рака яичников в будущем. [16]
Ссылки [ править ]
- ^ "T3DB: Ликорин" . www.t3db.ca . Проверено 12 ноября 2018 .
- ^ Ян, Сандра; Зайверт, Беттина; Кретцинг, Саша; Авраам, Гету; Регенталь, Ральф; Карст, Уве (2012). «Метаболические исследования амариллидных алкалоидов галантамина и ликорина на основе электрохимического моделирования в дополнение к моделям in vivo и in vitro» . Analytica Chimica Acta . 756 (756): 60–72. DOI : 10.1016 / j.aca.2012.10.042 . PMID 23176740 . Проверено 25 апреля 2017 года .
- ^ Берков, Страхил; Мартинес-Фрэнсис, Ванесса; Bastida, Jaume; Кодина, Карлес; Риос, Секундо (2014). «Эволюция биосинтеза алкалоидов в роде Нарцисс» . Фитохимия . 99 (99): 95–106. DOI : 10.1016 / j.phytochem.2013.11.002 . PMID 24461780 .
- ^ Кретцинг, Саша; Авраам, Гету; Зайверт, Беттина; Унгемах, Фриц Руперт; Кругель, Юте; Регенталь, Ральф (2011). «Дозозависимые рвотные эффекты амариллидного алкалоида ликорина у гончих собак» . Токсикон . 57 (57): 117–124. DOI : 10.1016 / j.toxicon.2010.10.012 . PMID 21055413 . Проверено 25 апреля 2017 года .
- ^ Vrijsen R, Ванден Берге Д.А., Vlietinck А.Ю., Boeyé А (1986). «Ликорин: ингибитор терминации эукариот?». J. Biol. Chem . 261 (2): 505–7. PMID 3001065 .
- ^ Garuccio I, Arrigoni O (1989). «[Различная чувствительность дрожжей к ликорину]». Болл. Soc. Ital. Биол. Спер. (на итальянском). 65 (6): 501–8. PMID 2611011 .
- ^ Ян, Сандра; Зайверт, Беттина; Кретцинг, Саша; Авраам, Гету; Регенталь, Ральф; Карст, Уве (2012). «Метаболические исследования амариллидных алкалоидов галантамина и ликорина на основе электрохимического моделирования в дополнение к моделям in vivo и in vitro» . Analytica Chimica Acta . 756 (756): 60–72. DOI : 10.1016 / j.aca.2012.10.042 . PMID 23176740 . Проверено 25 апреля 2017 года .
- ^ Елисей, Иллинойс; Эльгораши, Э. Хусейн, AA; Duncan, G .; Элофф, Дж. Н. (2013). «Эффекты ингибирования ацетлихолинэстеразы луковицы Ammocharis coranica (Amaryllidaceae) и его активного компонента ликорина» . Южноафриканский журнал ботаники (85): 44–47 . Проверено 25 апреля 2017 года .
- ^ Ван, Пэн; Юань, Хуэй-Хуэй; Чжан, Сюэ; Ли, Юнь-Пин; Шан, Лу-Цин; Инь, Чжэн (21 февраля 2014 г.). «Новые производные ликорина в качестве противораковых агентов: синтез и биологическая оценка in vitro» . Молекулы . 19 (2): 2469–2480. DOI : 10,3390 / молекулы19022469 . PMC 6271160 . PMID 24566315 . Проверено 25 апреля 2017 года .
- ↑ Зрачки заболели после того, как лампочку положили в суп , BBC News , 3 мая 2009 г.
- ^ Кретцинг, Саша; Авраам, Гету; Зайверт, Беттина; Унгемах, Фриц Руперт; Кругель, Юте; Регенталь, Ральф (2011). «Дозозависимые рвотные эффекты амариллидного алкалоида ликорина у гончих собак» . Токсикон . 57 (57): 117–124. DOI : 10.1016 / j.toxicon.2010.10.012 . PMID 21055413 . Проверено 25 апреля 2017 года .
- ^ Кретцинг, Саша; Авраам, Гету; Зайверт, Беттина; Унгемах, Фриц Руперт; Кругель, Юте; Регенталь, Ральф (2011). «Дозозависимые рвотные эффекты амариллидного алкалоида ликорина у гончих собак» . Токсикон . 57 (57): 117–124. DOI : 10.1016 / j.toxicon.2010.10.012 . PMID 21055413 . Проверено 25 апреля 2017 года .
- ^ Ликорин , определение на mercksource.com
- ^ Ян, Сандра; Зайверт, Беттина; Кретцинг, Саша; Авраам, Гету; Регенталь, Ральф; Карст, Уве (2012). «Метаболические исследования амариллидных алкалоидов галантамина и ликорина на основе электрохимического моделирования в дополнение к моделям in vivo и in vitro» . Analytica Chimica Acta . 756 (756): 60–72. DOI : 10.1016 / j.aca.2012.10.042 . PMID 23176740 . Проверено 25 апреля 2017 года .
- ^ Ван, Пэн; Юань, Хуэй-Хуэй; Чжан, Сюэ; Ли, Юнь-Пин; Шан, Лу-Цин; Инь, Чжэн (21 февраля 2014 г.). «Новые производные ликорина в качестве противораковых агентов: синтез и биологическая оценка in vitro» . Молекулы . 19 (2): 2469–2480. DOI : 10,3390 / молекулы19022469 . PMC 6271160 . PMID 24566315 . Проверено 25 апреля 2017 года .
- ^ Цао, Чжифэй; Ю, Ди; Фу, Шилонг; Чжан, Гаочуань; Пан, Янян; Бао, Мэймэй; Ту, Цзянь; Шан, Бинсюэ; Го, Пэнда; Ян, Пинг; Чжоу, Quansheng (2013). «Ликорина гидрохлорид избирательно подавляет пролиферацию клеток рака яичников человека и неоваскуляризацию опухоли с очень низкой токсичностью» . Письма токсикологии . 218 (2): 174–185. DOI : 10.1016 / j.toxlet.2013.01.018 . PMID 23376478 . Проверено 25 апреля 2017 года .
Внешние ссылки [ править ]
- Хилл, РК; Джоуль, JA; Лёффлер, LJ (1962). «Стереоселективный синтез d, l-α- и β-ликоранов». Журнал Американского химического общества . 84 (24): 4951–4956. DOI : 10.1021 / ja00883a064 .
- Вольфганг Оппольцер; Алан С. Спайви и Кристиан Г. Боше (1994). «Супрафациальность термической циклизации N-4-алкенилгидроксиламина: синтезы (±) -α-ликорана и (+) - тиантина» (PDF) . Варенье. Chem. Soc . 116 (7): 3139–3140. DOI : 10.1021 / ja00086a060 . Архивировано из оригинального (PDF) на 2011-06-14 . Проверено 4 ноября 2009 .