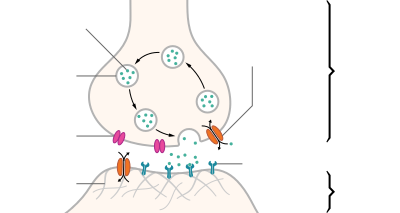
| Структура типичного химического синапса |
|---|
Нейротрансмиттеры - это химические мессенджеры, которые передают сигнал от нейрона через синапс к целевой клетке, которая может быть другим нейроном, мышечной клеткой или клеткой железы . Нейротрансмиттеры - это химические вещества, созданные нейроном специально для передачи сообщения . [1]
Нейротрансмиттеры высвобождаются из синаптических пузырьков в синапсах в синаптическую щель , где они принимаются рецепторами нейротрансмиттеров на клетке-мишени. Многие нейротрансмиттеры синтезируются из простых и многочисленных предшественников, таких как аминокислоты , которые легко доступны и требуют лишь небольшого количества этапов биосинтеза для преобразования. Нейротрансмиттеры необходимы для функционирования сложных нервных систем. Точное количество уникальных нейромедиаторов в организме человека неизвестно, но идентифицировано более 200. [2] [3] [4]
Механизм [ править ]
Нейротрансмиттеры хранятся в синаптических пузырьках , сгруппированных рядом с клеточной мембраной на конце аксона пресинаптического нейрона. Нейротрансмиттеры высвобождаются и диффундируют через синаптическую щель , где они связываются со специфическими рецепторами на мембране постсинаптического нейрона. [5] Связывание нейротрансмиттеров может влиять на постсинаптический нейрон возбуждающим или тормозящим образом, деполяризуя или реполяризуя его соответственно.
Большинство нейротрансмиттеров размером с одну аминокислоту; однако некоторые нейротрансмиттеры могут быть размером с более крупные белки или пептиды . Высвобожденный нейротрансмиттер обычно доступен в синаптической щели в течение короткого времени, прежде чем он метаболизируется ферментами, втягивается обратно в пресинаптический нейрон посредством обратного захвата или связывается с постсинаптическим рецептором . Тем не менее кратковременного воздействия на рецептор нейромедиатора обычно достаточно для того, чтобы вызвать постсинаптический ответ посредством синаптической передачи .
Обычно нейротрансмиттер высвобождается на пресинаптическом окончании в ответ на пороговый потенциал действия или градиентный электрический потенциал в пресинаптическом нейроне. Однако «исходный» выброс низкого уровня также происходит без электростимуляции.
Открытие [ править ]
До начала 20 века ученые предполагали, что большая часть синаптических коммуникаций в головном мозге была электрической. Однако при гистологическом исследовании Рамона-и-Кахала был обнаружен промежуток от 20 до 40 нм между нейронами, известный сегодня как синаптическая щель . Наличие такого разрыва предполагало, что связь осуществляется через химические мессенджеры, пересекающие синаптическую щель, и в 1921 году немецкий фармаколог Отто Левиподтвердили, что нейроны могут общаться, выделяя химические вещества. С помощью серии экспериментов с блуждающими нервами лягушек Лоуи смог вручную замедлить сердцебиение лягушек, контролируя количество физиологического раствора вокруг блуждающего нерва. По завершении этого эксперимента Лоуи утверждал, что симпатическая регуляция сердечной функции может быть опосредована изменениями в химических концентрациях. Кроме того, Отто Лоуи приписывают открытие ацетилхолина (ACh) - первого известного нейромедиатора. [6]
Идентификация [ править ]
Существует четыре основных критерия определения нейромедиаторов:
- Химическое вещество должно быть синтезировано в нейроне или иным образом в нем присутствовать.
- Когда нейрон активен, химическое вещество должно выделяться и вызывать реакцию у некоторых мишеней.
- Такой же ответ должен быть получен, когда химическое вещество экспериментально помещается на мишень.
- Должен существовать механизм для удаления химического вещества с места его активации после того, как его работа будет завершена.
Однако с учетом достижений фармакологии , генетики и химической нейроанатомии термин «нейромедиатор» можно применять к химическим веществам, которые:
- Передают сообщения между нейронами посредством воздействия на постсинаптическую мембрану.
- Имеют незначительное влияние или не влияют на напряжение на мембране, но имеют общую несущую функцию, такую как изменение структуры синапса.
- Общайтесь, отправляя сообщения в обратном направлении, которые влияют на освобождение или обратный захват передатчиков.
Анатомическая локализация нейротрансмиттеров обычно определяется с помощью иммуноцитохимических методов, которые определяют местоположение либо самих медиаторных веществ, либо ферментов, участвующих в их синтезе. Иммуноцитохимические методы также показали, что многие передатчики, особенно нейропептиды , локализованы совместно, то есть нейрон может высвобождать более одного передатчика со своего синаптического конца . [7] Различные методы и эксперименты, такие как окрашивание , стимуляция и сбор, могут использоваться для идентификации нейромедиаторов в центральной нервной системе . [8]
Типы [ править ]
Есть много разных способов классификации нейромедиаторов. Разделения их на аминокислоты , пептиды и моноамины достаточно для некоторых целей классификации. [9]
Основные нейротрансмиттеры:
- Аминокислоты : глутамат , [10] аспартат , D-серин , гамма-аминомасляная кислота (ГАМК), [nb 1] глицин.
- Газопередатчики : оксид азота (NO), оксид углерода (CO), сероводород (H 2 S).
- Моноамины : дофамин (DA), норэпинефрин (норадреналин; NE, NA), адреналин (адреналин), гистамин , серотонин (SER, 5-HT)
- Следовые амины : фенэтиламин , N- метилфенэтиламин , тирамин , 3-йодтиронамин , октопамин , триптамин и др.
- Пептиды : окситоцин , соматостатин , субстанция P , транскрипт , регулируемый кокаином и амфетамином , опиоидные пептиды [11]
- Пурины : аденозинтрифосфат (АТФ), аденозин
- Катехоламины : дофамин , норэпинефрин (норадреналин), адреналин (адреналин)
- Прочие: ацетилхолин (АХ), анандамид и др.
Кроме того, было обнаружено более 50 нейроактивных пептидов , и регулярно открываются новые. [ необходима цитата ] Многие из них выпускаются совместно с низкомолекулярным трансмиттером. Тем не менее, в некоторых случаях пептид является первичным передатчиком в синапсе. Бета-эндорфин является относительно известным примером пептидного нейромедиатора, поскольку он участвует в высокоспецифичных взаимодействиях с опиоидными рецепторами в центральной нервной системе .
Отдельные ионы (такие как синаптически высвобождаемый цинк ) также считаются нейротрансмиттерами некоторыми [12], а также некоторые газообразные молекулы, такие как оксид азота (NO), монооксид углерода (CO) и сероводород (H 2 S). [13] Газы производятся в нервной цитоплазме и немедленно диффундируют через клеточную мембрану во внеклеточную жидкость и в соседние клетки, чтобы стимулировать производство вторичных мессенджеров. Нейромедиаторы растворимых газов трудно изучать, поскольку они действуют быстро и сразу же разрушаются, существуя всего несколько секунд.
Наиболее распространенным передатчиком является глутамат , который возбуждает более 90% синапсов человеческого мозга. [10] Следующей по распространенности является гамма-аминомасляная кислота, или ГАМК, которая ингибирует более 90% синапсов, не использующих глутамат. Хотя другие передатчики используются в меньшем количестве синапсов, они могут иметь очень важное функциональное значение: подавляющее большинство психоактивных препаратов оказывают свое действие, изменяя действие некоторых систем нейротрансмиттеров, часто действуя через передатчики, отличные от глутамата или ГАМК. Наркотики, вызывающие привыкание, такие как кокаин и амфетамины, оказывают свое действие в первую очередь на дофаминовую систему. Опиатные препараты, вызывающие привыкание, проявляют свое действие в первую очередь как функциональные аналоги опиоидных пептидов., которые, в свою очередь, регулируют уровень дофамина.
Список нейротрансмиттеров, пептидов и газообразных сигнальных молекул [ править ]
|
Действия [ редактировать ]
Нейроны образуют сложные сети, через которые проходят нервные импульсы - потенциалы действия. Каждый нейрон имеет до 15 000 связей с соседними нейронами.
Нейроны не соприкасаются друг с другом (кроме случая электрического синапса через щелевой переход); вместо этого нейроны взаимодействуют в точках контакта, называемых синапсами: соединение внутри двух нервных клеток, состоящее из миниатюрной щели, внутри которой импульсы переносятся нейротрансмиттером. Нейрон передает свою информацию посредством нервного импульса, называемого потенциалом действия. Когда потенциал действия достигает предсинаптической терминальной кнопки синапса, он может стимулировать высвобождение нейротрансмиттеров. Эти нейротрансмиттеры высвобождаются в синаптическую щель, чтобы связываться с рецепторами постсинаптической мембраны и влиять на другую клетку либо ингибирующим, либо возбуждающим образом. Следующий нейрон может быть связан со многими другими нейронами, и если общее количество возбуждающих влияний минус тормозные влияния достаточно велико, он также будет "огонь ». Иными словами, он создаст новый потенциал действия на бугре аксона, высвобождая нейротрансмиттеры и передавая информацию еще одному соседнему нейрону.
Возбуждающее и сдерживающее [ править ]
Нейромедиатор может влиять на функцию нейрона посредством значительного числа механизмов. Однако в своем прямом воздействии на электрическую возбудимость нейрона нейротрансмиттер действует только одним из двух способов: возбуждающим или тормозящим. Нейромедиатор влияет на трансмембранный ионный поток, увеличивая (возбуждая) или уменьшая (подавляя) вероятность того, что клетка, с которой он вступает в контакт, будет производить потенциал действия. Таким образом, несмотря на большое разнообразие синапсов, все они передают сообщения только этих двух типов, и они обозначены как таковые. Синапсы типа I обладают возбуждающим действием, а синапсы типа II - тормозящими.. Каждый тип имеет различный внешний вид и располагается в разных частях нейронов, находящихся под его влиянием. [17]
Синапсы типа I (возбуждающие) обычно располагаются на стержнях или шипах дендритов, тогда как синапсы типа II (тормозящие) обычно располагаются на теле клетки. Кроме того, синапсы типа I имеют круглые синаптические пузырьки, тогда как пузырьки синапсов типа II уплощены. Материал на пресинаптических и постсинаптических мембранах более плотный в синапсе I типа, чем в синапсе II типа, а синаптическая щель I типа шире. Наконец, активная зона в синапсе I типа больше, чем в синапсе II типа.
Различное расположение синапсов типа I и типа II делит нейрон на две зоны: дендритное дерево возбуждения и тело тормозящей клетки. С тормозной точки зрения, возбуждение проходит через дендриты и распространяется на бугорок аксона, чтобы запустить потенциал действия.. Если сообщение должно быть остановлено, лучше всего остановить его, применив ингибирование к телу клетки, близко к бугорку аксона, где возникает потенциал действия. Другой способ концептуализировать возбуждающе-тормозное взаимодействие - представить себе возбуждение, преодолевающее торможение. Если тело клетки обычно находится в подавленном состоянии, единственный способ создать потенциал действия на бугорке аксона - это уменьшить подавление тела клетки. В этой стратегии «откройте ворота» возбуждающее сообщение похоже на скаковую лошадь, готовую бежать по трассе, но сначала необходимо удалить препятствующие стартовые ворота. [18]
Примеры важных действий нейротрансмиттеров [ править ]
Как объяснялось выше, единственное прямое действие нейротрансмиттера - это активация рецептора. Следовательно, эффекты нейротрансмиттерной системы зависят от соединений нейронов, которые используют передатчик, и химических свойств рецепторов, с которыми передатчик связывается.
Вот несколько примеров важных действий нейротрансмиттеров:
- Глутамат используется в подавляющем большинстве быстрых возбуждающих синапсов головного и спинного мозга. Он также используется в большинстве синапсов, которые являются «модифицируемыми», т. Е. Способными увеличиваться или уменьшаться в силе. Считается , что модифицируемые синапсы являются основными элементами памяти в мозгу. Чрезмерное высвобождение глутамата может чрезмерно стимулировать мозг и приводить к эксайтотоксичности, вызывая гибель клеток, приводящую к судорогам или инсультам. [19] Эксайтотоксичность участвует в некоторых хронических заболеваний , в том числе ишемического инсульта , эпилепсии , бокового амиотрофического склероза , болезни Альцгеймера , болезни Хантингтона , иБолезнь Паркинсона . [20]
- ГАМК используется в подавляющем большинстве быстрых тормозных синапсов практически в каждой части мозга. Многие седативные / транквилизирующие препараты действуют, усиливая действие ГАМК. [21] Соответственно, глицин является тормозящим передатчиком в спинном мозге .
- Ацетилхолин был первым нейромедиатором, обнаруженным в периферической и центральной нервной системах. Он активирует скелетные мышцы соматической нервной системы и может возбуждать или подавлять внутренние органы вегетативной системы. [8] Он известен как передатчик в нервно-мышечном соединении, соединяющем двигательные нервы с мышцами. Паралитический яд со стрелами кураре действует, блокируя передачу в этих синапсах. Ацетилхолин также действует во многих областях мозга, но с использованием различных типов рецепторов , включая никотиновые и мускариновые рецепторы. [22]
- Дофамин выполняет ряд важных функций в головном мозге; это включает в себя регулирование двигательного поведения, удовольствия, связанные с мотивацией, а также эмоциональное возбуждение. Он играет решающую роль в системе вознаграждения ; Болезнь Паркинсона связана с низким уровнем дофамина, а шизофрения связана с высоким уровнем дофамина. [23]
- Серотонин - нейромедиатор моноаминов . Большая часть вырабатывается и обнаруживается в кишечнике (примерно 90%), а остальная часть - в нейронах центральной нервной системы . Он регулирует аппетит, сон, память и обучение, температуру, настроение, поведение, сокращение мышц, а также функции сердечно-сосудистой и эндокринной систем . Предполагается, что он играет роль в депрессии, поскольку у некоторых пациентов с депрессией наблюдаются более низкие концентрации метаболитов серотонина в спинномозговой жидкости и ткани мозга. [24]
- Норэпинефрин, который синтезируется в центральной нервной системе и симпатических нервах, модулирует реакции вегетативной нервной системы, режим сна, концентрацию внимания и бдительность. Он синтезируется из тирозина .
- Адреналин, который также синтезируется из тирозина, высвобождается в надпочечниках и стволе мозга. Он играет роль во сне, в способности человека быть бдительным и сохранять его, а также в реакции « бей или беги» .
- Гистамин работает с центральной нервной системой (ЦНС), в частности с гипоталамусом ( туберомаммиллярное ядро ) и тучными клетками ЦНС .
Системы нейротрансмиттеров головного мозга [ редактировать ]
Нейроны, экспрессирующие определенные типы нейротрансмиттеров, иногда образуют отдельные системы, активация которых влияет на большие объемы мозга, что называется объемной передачей . Основные системы нейротрансмиттеров включают , среди прочего, систему норадреналина (норадреналина), систему дофамина, систему серотонина и холинергическую систему. Следовые амины оказывают модулирующее действие на нейротрансмиссию в моноаминовых путях (т. Е. В путях дофамина, норэпинефрина и серотонина) по всему мозгу посредством передачи сигналов через рецептор 1, связанный со следами аминов . [25] [26] Ниже приводится краткое сравнение этих систем:
| Система | Происхождение и проекции пути | Регулируемые когнитивные процессы и поведение |
|---|---|---|
| Норадреналиновая система [27] [28] [29] [30] [31] [32] | Норадренергические пути :
|
|
| Дофаминовая система [29] [30] [31] [33] [34] [35] | Дофаминергические пути :
|
|
| Гистаминовая система [30] [31] [36] | Гистаминергические пути :
|
|
| Система серотонина [27] [29] [30] [31] [37] [38] [39] | Серотонинергические пути : Хвостовые ядра (CN):
Ростральные ядра (RN):
|
|
| Ацетилхолиновая система [27] [29] [30] [31] [40] | Холинергические пути : Холинергические ядра переднего мозга (FCN):
Холинергические
|
|
Эффекты наркотиков [ править ]
Понимание воздействия лекарств на нейротрансмиттеры составляет значительную часть исследовательских инициатив в области нейробиологии . Большинство нейробиологов, занимающихся этой областью исследований, считают, что такие усилия могут способствовать дальнейшему углублению нашего понимания цепей, ответственных за различные неврологические заболевания и расстройства, а также способов эффективного лечения, а когда-нибудь, возможно, предотвращения или лечения таких заболеваний. [41] [ требуется медицинская ссылка ]
Наркотики могут влиять на поведение, изменяя активность нейромедиаторов. Например, лекарства могут снижать скорость синтеза нейротрансмиттеров, воздействуя на синтетический фермент (ы) этого нейротрансмиттера. Когда синтез нейротрансмиттеров блокируется, количество нейромедиаторов, доступных для высвобождения, становится значительно ниже, что приводит к снижению активности нейромедиатора. Некоторые препараты блокируют или стимулируют высвобождение определенных нейромедиаторов. В качестве альтернативы, лекарства могут предотвратить накопление нейротрансмиттеров в синаптических везикулах, вызывая утечку мембран синаптических везикул. Лекарства, которые препятствуют связыванию нейромедиатора с его рецептором, называются антагонистами рецепторов.. Например, препараты, используемые для лечения пациентов с шизофренией, такие как галоперидол, хлорпромазин и клозапин, являются антагонистами рецепторов дофамина в головном мозге. Другие препараты действуют путем связывания с рецептором и имитируют нормальный нейромедиатор. Такие препараты называют агонистами рецепторов . Примером агониста рецептора является морфин , опиат, имитирующий эффекты эндогенного нейромедиатора β-эндорфина.чтобы облегчить боль. Другие препараты препятствуют дезактивации нейромедиатора после его высвобождения, тем самым продлевая действие нейромедиатора. Это может быть достигнуто путем блокирования повторного захвата или ингибирования ферментов деградации. Наконец, лекарства могут также предотвращать возникновение потенциала действия, блокируя нейронную активность в центральной и периферической нервной системе . Такие препараты, как тетродотоксин, блокирующие нервную активность, обычно смертельны.
Лекарства, нацеленные на нейромедиатор основных систем, влияют на всю систему, что может объяснить сложность действия некоторых лекарств. Кокаин , например, блокирует повторный захват дофамина обратно в пресинаптический нейрон, оставляя молекулы нейротрансмиттера в синаптической щели на длительный период времени. Поскольку дофамин дольше остается в синапсе, нейромедиатор продолжает связываться с рецепторами постсинаптического нейрона, вызывая приятную эмоциональную реакцию. Физическая зависимость от кокаина может быть результатом длительного воздействия избытка дофамина в синапсах, что приводит к его подавлению.некоторых постсинаптических рецепторов. После того, как действие препарата прекратится, человек может впасть в депрессию из-за снижения вероятности связывания нейромедиатора с рецептором. Флуоксетин является селективным ингибитором обратного захвата серотонина (СИОЗС), который блокирует повторный захват серотонина пресинаптической клеткой, что увеличивает количество серотонина, присутствующего в синапсе, и, кроме того, позволяет ему оставаться там дольше, обеспечивая возможность естественного воздействия высвободил серотонин. [42] AMPT предотвращает превращение тирозина в L-DOPA , предшественника дофамина; резерпин предотвращает накопление дофамина в пузырьках ; и депренил ингибирует моноаминоксидазу (MAO) -B и, таким образом, увеличивает уровень дофамина.
| Препарат, средство, медикамент | Взаимодействует с: | Рецепторное взаимодействие: | Тип | Последствия |
|---|---|---|---|---|
| Ботулинический токсин (ботокс) | Ацетилхолин | - | Антагонист | Блокирует выброс ацетилхолина в ПНС Предотвращает сокращение мышц |
| Яд паука Чёрной Вдовы | Ацетилхолин | - | Агонист | Способствует высвобождению ацетилхолина в ПНС Стимулирует мышечные сокращения |
| Неостигмин | Ацетилхолин | - | - | Нарушает активность ацетилхолинеразы Увеличивает эффекты ACh на рецепторы Используется для лечения миастении. |
| Никотин | Ацетилхолин | Никотиновая (скелетная мышца) | Агонист | Повышает активность АХ Повышает внимание Усиливающие эффекты |
| d-тубокурарин | Ацетилхолин | Никотиновая (скелетная мышца) | Антагонист | Снижает активность рецептора. |
| Кураре | Ацетилхолин | Никотиновая (скелетная мышца) | Антагонист | Снижает активность АХ Предотвращает сокращение мышц |
| Мускарин | Ацетилхолин | Мускариновый (сердце и гладкие мышцы) | Агонист | Повышает активность АХ Токсичный |
| Атропин | Ацетилхолин | Мускариновый (сердце и гладкие мышцы) | Антагонист | Блокирует сужение зрачка Блокирует выработку слюны |
| Скополамин ( гиосцин ) | Ацетилхолин | Мускариновый (сердце и гладкие мышцы) | Антагонист | Лечит укачивание, послеоперационную тошноту и рвоту. |
| AMPT | Дофамин / норэпинефрин | - | - | Инактивирует тирозингидроксилазу и подавляет выработку дофамина. |
| Резерпин | Допамин | - | - | Предотвращает накопление дофамина и других моноаминов в синаптических везикулах Вызывает седативный эффект и депрессию |
| Апоморфин | Допамин | Рецептор D2 (пресинаптические ауторецепторы / постсинаптические рецепторы) | Антагонист (низкая доза) / прямой агонист (высокая доза) | Низкая доза: блокирует ауторецепторы Высокая доза: стимулирует постсинаптические рецепторы. |
| Амфетамин | Дофамин / норэпинефрин | - | Косвенный агонист | Высвобождает дофамин, норадреналин и серотонин. Блокирует обратный захват [25] [26] |
| Метамфетамин | Дофамин / норэпинефрин | - | - | Высвобождает дофамин и норадреналин. Блокирует обратный захват |
| Метилфенидат | Допамин | - | - | Блокирует обратный захват Повышает внимание и контроль над импульсами при СДВГ |
| Кокаин | Допамин | - | Косвенный агонист | Блокирует обратный захват в пресинапс Блокирует зависимые от напряжения натриевые каналы Может использоваться как местное обезболивающее (глазные капли) |
| Депренил | Допамин | - | Агонист | Подавляет МАО-В Предотвращает разрушение дофамина |
| Хлорпромазин | Допамин | Рецепторы D2 | Антагонист | Блокирует рецепторы D2 Снимает галлюцинации |
| MPTP | Допамин | - | - | Приводит к симптомам, подобным болезни Паркинсона |
| PCPA | Серотонин (5-HT) | - | Антагонист | Нарушает синтез серотонина, блокируя активность триптофангидроксилазы |
| Ондансетрон | Серотонин (5-HT) | 5-HT 3 рецепторы | Антагонист | Уменьшает побочные эффекты химиотерапии и лучевой терапии Уменьшает тошноту и рвоту |
| Буспирон | Серотонин (5-HT) | Рецепторы 5-HT 1A | Частичный агонист | Лечит симптомы тревоги и депрессии |
| Флуоксетин | Серотонин (5-HT) | поддерживает обратный захват 5-HT | СИОЗС | Подавляет обратный захват серотонина Лечит депрессию, некоторые тревожные расстройства и ОКР [42]. Распространенные примеры: Prozac и Sarafem. |
| Фенфлурамин | Серотонин (5-HT) | - | - | Вызывает выброс серотонина Подавляет обратный захват серотонина Используется как подавитель аппетита |
| Диэтиламид лизергиновой кислоты | Серотонин (5-HT) | Постсинаптические рецепторы 5-HT 2A | Прямой агонист | Вызывает искажения зрительного восприятия Стимулирует рецепторы 5-HT 2A в переднем мозге |
| Метилендиоксиметамфетамин ( МДМА ) | Серотонин (5-HT) / норэпинфрин | - | - | Стимулирует высвобождение серотонина и норадреналина и подавляет обратный захват Вызывает возбуждающее и галлюциногенное действие. |
| Стрихнин | Глицин | - | Антагонист | Вызывает сильные мышечные спазмы [44] |
| Дифенгидрамин | Гистамин | Пересекает гематоэнцефалический барьер, вызывая сонливость | ||
| Тетрагидроканнабинол (THC) | Эндоканнабиноиды | Каннабиноидные (CB) рецепторы | Агонист | Обладает обезболивающим и седативным действием Повышает аппетит Познавательные эффекты |
| Римонабант | Эндоканнабиноиды | Каннабиноидные (CB) рецепторы | Антагонист | Подавляет аппетит Используется при отказе от курения |
| MAFP | Эндоканнабиноиды | - | - | Подавляет FAAH Используется в исследованиях для повышения активности каннабиноидной системы |
| AM1172 | Эндоканнабиноиды | - | - | Блокирует обратный захват каннабиноидов Используется в исследованиях для повышения активности каннабиноидной системы |
| Анандамид (эндогенный) | - | Каннабиноидные (CB) рецепторы; 5-HT 3 рецепторы | - | Уменьшить тошноту и рвоту |
| Кофеин | Аденозин | Аденозиновые рецепторы | Антагонист | Блокирует аденозиновые рецепторы Повышает бодрствование |
| PCP | Глутамат | Рецептор NMDA | Косвенный антагонист | Блокирует сайт связывания PCP Предотвращает попадание ионов кальция в нейроны Ухудшает обучение |
| AP5 | Глутамат | Рецептор NMDA | Антагонист | Блокирует сайт связывания глутамата на рецепторе NMDA Нарушает синаптическую пластичность и определенные формы обучения |
| NMDA | Глутамат | Рецептор NMDA | Агонист | Используется в исследованиях для изучения рецептора NMDA Ионотропный рецептор |
| AMPA | Глутамат | Рецептор AMPA | Агонист | Используется в исследованиях для изучения рецептора AMPA Ионотропный рецептор |
| Кетамин | Глутамат | Каинатный рецептор | Антагонист | Используется в исследованиях для изучения каинатных рецепторов. Вызывает состояние транса, облегчает боль и успокаивает |
| Аллиглицин | ГАМК | - | - | Подавляет синтез ГАМК Вызывает судороги |
| Muscimol | ГАМК | Рецептор ГАМК | Агонист | Вызывает седативный эффект |
| Бикукулин | ГАМК | Рецептор ГАМК | Антагонист | Причины судорог |
| Бензодиазепины | ГАМК | Рецептор ГАМК А | Косвенные агонисты | Анксиолитик, седативный эффект, нарушение памяти, расслабление мышц |
| Барбитураты | ГАМК | Рецептор ГАМК А | Косвенные агонисты | Седативный эффект, нарушение памяти, расслабление мышц |
| Алкоголь | ГАМК | Рецептор ГАМК | Косвенный агонист | Седативный эффект, нарушение памяти, расслабление мышц |
| Пикротоксин | ГАМК | Рецептор ГАМК А | Косвенный антагонист | Высокие дозы вызывают судороги |
| Тиагабин | ГАМК | - | Антагонист | Антагонист транспортера ГАМК Повышение доступности ГАМК Снижает вероятность судорог |
| Моклобемид | Норэпинефрин | - | Агонист | Блокирует МАО-А для лечения депрессии |
| Идазоксан | Норэпинефрин | альфа-2 адренергические ауторецепторы | Агонист | Блокирует ауторецепторы альфа-2 Используется для изучения норадреналиновой системы |
| Фузариновая кислота | Норэпинефрин | - | - | Подавляет активность дофамин-бета-гидроксилазы, которая блокирует выработку норадреналина. Используется для изучения норадреналиновой системы без влияния на дофаминовую систему. |
| Опиаты ( опиум , морфин , героин и оксикодон ) | Опиоиды | Опиоидный рецептор [45] | Агонисты | Обезболивающий, седативный и усиливающий эффекты |
| Налоксон | Опиоиды | - | Антагонист | Снимает симптомы опиатной интоксикации или передозировки (например, проблемы с дыханием) |
Агонисты [ править ]
Этот раздел нуждается в расширении за счет: охвата полных агонистов и их отличия от частичных агонистов и обратных агонистов. Вы можете помочь, добавив к нему . ( Август 2015 г. ) |
Агонист - это химическое вещество, способное связываться с рецептором, таким как рецептор нейромедиатора, и инициировать ту же реакцию, которая обычно вызывается связыванием эндогенного вещества. [46] Таким образом, агонист нейромедиатора инициирует тот же рецепторный ответ, что и передатчик. В нейронах агонист может активировать рецепторы нейромедиаторов прямо или косвенно. Агонисты прямого связывания могут быть далее охарактеризованы как полные агонисты , частичные агонисты , обратные агонисты . [47] [48]
Прямые агонисты действуют аналогично нейротрансмиттеру, связываясь непосредственно с ассоциированным с ним рецепторным сайтом (ами), который может быть расположен на пресинаптическом нейроне или постсинаптическом нейроне, или на обоих. [49] Обычно рецепторы нейротрансмиттеров расположены на постсинаптическом нейроне, а ауторецепторы нейротрансмиттеров расположены на пресинаптическом нейроне, как в случае моноаминовых нейротрансмиттеров ; [25] в некоторых случаях нейротрансмиттер использует ретроградную нейротрансмиссию , тип обратной связи в нейронах, где нейромедиатор высвобождается постсинаптически и связывается с рецепторами-мишенями, расположенными на пресинаптическом нейроне. [50] [примечание 1] Никотин, соединение, обнаруженное в табаке , является прямым агонистом большинства никотиновых рецепторов ацетилхолина , в основном расположенных в холинергических нейронах . [45] Опиаты , такие как морфин , героин , гидрокодон , оксикодон , кодеин и метадон , являются агонистами μ-опиоидных рецепторов ; это действие опосредует их эйфорические и болеутоляющие свойства. [45]
Непрямые агонисты увеличивают связывание нейромедиаторов с их рецепторами-мишенями, стимулируя высвобождение или предотвращая обратный захват нейротрансмиттеров. [49] Некоторые непрямые агонисты вызывают высвобождение нейротрансмиттера и предотвращают его повторный захват . Амфетамин , например, является непрямым агонистом постсинаптических рецепторов дофамина, норэпинефрина и серотонина в каждом из соответствующих нейронов; [25] [26] он производит высвобождение нейротрансмиттеров в пресинаптическом нейроне и впоследствии в синаптическую щель, а также предотвращает их обратный захват из синаптической щели путем активации TAAR1 , пресинаптического нейрона.Рецептор , связанный с G-белком , и связывание с сайтом на VMAT2 , типе переносчика моноаминов, расположенного на синаптических пузырьках внутри моноаминовых нейронов . [25] [26]
Антагонисты [ править ]
Антагонист - это химическое вещество, которое действует в организме, снижая физиологическую активность другого химического вещества (как опиата); особенно тот, который противодействует действию на нервную систему лекарственного средства или вещества, встречающегося в организме естественным образом, путем объединения и блокирования его нервного рецептора. [51]
Существует два основных типа антагонистов: антагонисты прямого действия и антагонисты непрямого действия:
- Антагонист прямого действия, который занимает место на рецепторах, которые в противном случае занимают сами нейротрансмиттеры. Это приводит к тому, что нейротрансмиттеры блокируются от связывания с рецепторами. Наиболее распространен атропин.
- Антагонисты непрямого действия - препараты, подавляющие высвобождение / выработку нейромедиаторов (например, резерпин ).
Антагонисты наркотиков [ править ]
Антагонистическое лекарство - это лекарство, которое прикрепляется (или связывается) к участку, называемому рецептором, без активации этого рецептора для получения биологической реакции. Поэтому говорят, что он не обладает внутренней активностью. Антагонист может также называться «блокатором» рецептора, потому что он блокирует действие агониста на сайте. Фармакологические эффекты антагониста, таким образом, приводят к предотвращению связывания агонистов соответствующего рецепторного сайта (например, лекарств, гормонов, нейромедиаторов) с ним и его активации. Антагонисты могут быть «конкурентными» или «необратимыми».
Конкурентный антагонист конкурирует с агонистом за связывание с рецептором. По мере увеличения концентрации антагониста связывание агониста прогрессивно ингибируется, что приводит к снижению физиологического ответа. Высокая концентрация антагониста может полностью подавить ответ. Однако это ингибирование может быть отменено увеличением концентрации агониста, поскольку агонист и антагонист конкурируют за связывание с рецептором. Следовательно, конкурентные антагонисты можно охарактеризовать как сдвигающие соотношение доза-ответ для агониста вправо. В присутствии конкурентного антагониста требуется повышенная концентрация агониста, чтобы вызвать тот же ответ, который наблюдается в отсутствие антагониста.
Необратимый антагонист настолько сильно связывается с рецептором, что делает рецептор недоступным для связывания с агонистом. Необратимые антагонисты могут даже образовывать ковалентные химические связи с рецептором. В любом случае, если концентрация необратимого антагониста достаточно высока, количество несвязанных рецепторов, остающихся для связывания агониста, может быть настолько низким, что даже высокие концентрации агониста не вызывают максимального биологического ответа. [52]
Предшественники [ править ]
Биосинтетические пути катехоламинов и следовых аминов в мозге человека [53] [54] [55] |
Хотя потребление предшественников нейромедиаторов действительно увеличивает синтез нейротрансмиттеров, данные о том, увеличивается ли высвобождение нейротрансмиттеров и срабатывание постсинаптических рецепторов, неоднозначны . Даже при повышенном высвобождении нейромедиаторов неясно, приведет ли это к долгосрочному увеличению силы сигнала нейромедиатора, поскольку нервная система может адаптироваться к таким изменениям, как усиление синтеза нейромедиаторов, и, следовательно, может поддерживать постоянную активность. [56] [ ненадежный медицинский источник? ] Некоторые нейротрансмиттеры могут играть роль в депрессии, и есть некоторые данные, позволяющие предположить, что прием предшественников этих нейромедиаторов может быть полезным при лечении легкой и умеренной депрессии. [56][ ненадежный медицинский источник? ] [57]
Катехоламины и предшественники следов аминов [ править ]
L- ДОФА , предшественник дофамина, который проникает через гематоэнцефалический барьер , используется при лечении болезни Паркинсона . Для пациентов с депрессией, у которыхнаблюдаетсянизкая активность нейротрансмиттера норадреналина , имеется мало доказательств пользы от введения предшественников нейромедиаторов. L-фенилаланин и L-тирозин являются предшественниками дофамина , норадреналина и адреналина . Эти преобразования требуют витамина B6 , витамина C и S-аденозилметионина.. Несколько исследований предполагают потенциальные антидепрессивные эффекты L-фенилаланина и L-тирозина, но есть много возможностей для дальнейших исследований в этой области. [56] [ ненадежный медицинский источник? ]
Предшественники серотонина [ править ]
Введение L-триптофан , предшественник серотонина , видно , чтобы удвоить производство серотонина в мозге. Он значительно эффективнее плацебо при лечении легкой и умеренной депрессии. [56] [ ненадежный медицинский источник? ] Это преобразование требует витамин С . [24] 5-гидрокситриптофан (5-HTP), также являющийся предшественником серотонина , более эффективен, чем плацебо. [56] [ ненадежный медицинский источник? ]
Заболевания и расстройства [ править ]
Заболевания и расстройства также могут влиять на определенные системы нейротрансмиттеров. Ниже перечислены расстройства, связанные с увеличением, уменьшением или дисбалансом определенных нейромедиаторов.
Дофамин :
Например, проблемы с выработкой дофамина (в основном в черной субстанции ) могут привести к болезни Паркинсона , расстройству, которое влияет на способность человека двигаться так, как он хочет, что приводит к скованности, тремору или тряске и другим симптомам. Некоторые исследования показывают, что слишком мало или слишком много дофамина или проблемы с его использованием в мыслящих и чувствующих областях мозга могут играть роль в таких расстройствах, как шизофрения или синдром дефицита внимания с гиперактивностью (СДВГ). Дофамин также вызывает привыкание и употребление наркотиков, поскольку большинство рекреационных наркотиков вызывают приток дофамина в мозг (особенно опиоиды и метамфетамины).), доставляющее удовольствие, поэтому потребители постоянно испытывают тягу к наркотикам.
Серотонин :
Аналогичным образом, после того, как некоторые исследования показали, что препараты, которые блокируют рециркуляцию или обратный захват серотонина, похоже, помогают некоторым людям с диагнозом депрессия, было высказано предположение, что у людей с депрессией может быть уровень серотонина ниже нормы. Несмотря на широкую популяризацию, эта теория не получила подтверждения в последующих исследованиях. [58] Таким образом, селективные ингибиторы обратного захвата серотонина (СИОЗС) используются для увеличения количества серотонина в синапсах.
Глутамат :
Кроме того, проблемы с производством или использованием глутамата были предположительно и предположительно связаны со многими психическими расстройствами, включая аутизм , обсессивно-компульсивное расстройство (ОКР), шизофрению и депрессию . [59] Имея слишком много глутамата был связан с неврологических заболеваний , таких как болезнь Паркинсона , рассеянный склероз , болезнь Альцгеймера , инсульт и ALS (боковой амиотрофический склероз). [60]
Дисбаланс нейротрансмиттеров [ править ]
Как правило, не существует научно установленных «норм» для соответствующих уровней или «балансов» различных нейромедиаторов. В большинстве случаев прагматически невозможно даже измерить уровни нейромедиаторов в мозге или теле в определенные моменты времени. Нейротрансмиттеры регулируют высвобождение друг друга, и слабый постоянный дисбаланс в этой взаимной регуляции был связан с темпераментом у здоровых людей. [61] [62] [63] [64] [65]Сильный дисбаланс или сбои в работе нейротрансмиттерных систем связаны со многими заболеваниями и психическими расстройствами. К ним относятся болезнь Паркинсона, депрессия, бессонница, синдром дефицита внимания и гиперактивности (СДВГ), беспокойство, потеря памяти, резкие изменения веса и зависимости. Хронический физический или эмоциональный стресс может способствовать изменениям в нейромедиаторной системе. Генетика также играет роль в активности нейротрансмиттеров. Помимо использования в рекреационных целях, лекарства, которые прямо или косвенно взаимодействуют с одним или несколькими передатчиком или его рецептором, обычно назначаются при психиатрических и психологических проблемах. В частности, препараты, взаимодействующие с серотонином и норадреналином.прописываются пациентам с такими проблемами, как депрессия и тревожность, хотя мнение о том, что существует множество веских медицинских доказательств в поддержку таких вмешательств, подвергалось широкой критике. [66] Исследования показали, что дисбаланс дофамина влияет на рассеянный склероз и другие неврологические расстройства. [67]
Устранение нейротрансмиттеров [ править ]
Нейромедиатор должен быть разрушен, как только он достигнет постсинаптической клетки, чтобы предотвратить дальнейшую передачу возбуждающего или тормозящего сигнала. Это позволяет производить новые сигналы от соседних нервных клеток. Когда нейротрансмиттер секретируется в синаптическую щель, он связывается со специфическими рецепторами постсинаптической клетки, тем самым генерируя постсинаптический электрический сигнал. Затем передатчик должен быть быстро удален, чтобы позволить постсинаптической клетке участвовать в другом цикле высвобождения, связывания и генерации сигнала нейромедиатора. Нейротрансмиттеры терминируются тремя разными способами:
- Диффузия - нейромедиатор отделяется от рецептора, выходя из синаптической щели, здесь он поглощается глиальными клетками .
- Расщепление ферментов - его расщепляют специальные химические вещества, называемые ферментами . Обычно астроциты поглощают избыточные нейротрансмиттеры и передают их ферментам или перекачивают их непосредственно в пресинаптический нейрон.
- Reuptake - повторное поглощение нейромедиатора нейроном. Транспортеры или мембранные транспортные белки перекачивают нейротрансмиттеры из синаптической щели обратно в терминалы аксона (пресинаптический нейрон), где они хранятся. [68]
Например, холин поглощается и перерабатывается пресинаптическим нейроном для синтеза большего количества ACh. Другие нейротрансмиттеры, такие как дофамин , способны диффундировать от целевых синаптических соединений и выводиться из организма через почки или разрушаться в печени. Каждый нейротрансмиттер имеет очень специфические пути деградации в регуляторных точках, на которые может воздействовать регулирующая система организма или лекарства.
См. Также [ править ]
- BK канал № Уровень сотовой связи
- Поцелуй и беги слияние
- Натуральное нейроактивное вещество
- Нейроэндокринный
- Нейроэндокринология
- Нейропсихофармакология
- Аналог нейротрансмиттера
- Выпуск нейротрансмиттера
Заметки [ править ]
- ^ В центральной нервной системе анандамид, другие эндоканнабиноиды, используют ретроградную нейротрансмиссию, поскольку их высвобождение является постсинаптическим, в то время как их целевой рецептор, каннабиноидный рецептор 1 (CB1), является пресинаптическим. [50] конопля растение содержит Δ 9 тетрагидроканнабинола , который является прямым агонистом СВ1. [50]
- ^ ГАМК - непротеиногенная аминокислота.
Ссылки [ править ]
- ^ Лодиш, H .; Берк, А .; Зипурский, С.Л. (2000). Молекулярная клеточная биология: Раздел 21.4 Нейротрансмиттеры, синапсы и передача импульсов (4-е изд.). Нью-Йорк: WH Freeman.
- ^ Черри, Кендра. "Что такое нейротрансмиттер?" . Проверено 6 октября 2014 года .
- ^ "База данных нейропептидов" .
- ^ «Нейропептиды. Руководство IUPHAR / BPS по фармакологии» .
- ^ Элиас, Л. Дж, & Сосье, DM (2005). Нейропсихология: клинические и экспериментальные основы. Бостон: Пирсон
- ^ Саладин, Кеннет С. Анатомия и физиология: единство формы и функции . Макгроу Хилл. 2009 ISBN 0-07-727620-5
- ^ Университет, С. Марк Бридлав, Университет штата Мичиган, Нил В. Уотсон, Саймон Фрейзер (2013). Биологическая психология: введение в поведенческую, когнитивную и клиническую нейробиологию (седьмое изд.). Сандерленд, Массачусетс: Sinauer Associates. ISBN 978-0878939275.
- ^ a b Whishaw, Брайан Колб, Ян К. (2014). Введение в мозг и поведение (4-е изд.). Нью-Йорк, штат Нью-Йорк: Издательство Worth. С. 150–151. ISBN 978-1429242288.
- ↑ Барре Виджая Прасад (2020). Изучение биологических основ поведения человека . Соединенные Штаты Америки: IGI Global. п. 81. ISBN 978-1799-8286-17.
- ^ a b Роберт Сапольски (2005). «Биология и поведение человека: неврологические истоки индивидуальности, 2-е издание». Обучающая компания.
см. страницы 13 и 14 Путеводителя
- ^ Снайдер SH, Innis RB (1979). «Пептидные нейромедиаторы». Анну. Rev. Biochem . 48 : 755–82. DOI : 10.1146 / annurev.bi.48.070179.003543 . PMID 38738 .
- ^ Кодиров Sodikdjon А., Такизава Шуичи, Джозеф Джейми, Кандель Эрик Р., Шумяцкий Глеб П. Большаков Вадим Юрьевич (2006). «Синаптически высвобождаемый цинк обеспечивает долгосрочное усиление путей кондиционирования страха» . PNAS . 103 (41): 15218–23. DOI : 10.1073 / pnas.0607131103 . PMC 1622803 . PMID 17005717 . CS1 maint: несколько имен: список авторов ( ссылка )
- ^ "Международный симпозиум по оксиду азота - доктор Джон Эндрюс - MaRS" . MaRS . Архивировано из оригинального 14 октября 2014 года.
- ^ «Дофамин: биологическая активность» . Руководство IUPHAR / BPS по фармакологии . Международный союз фундаментальной и клинической фармакологии . Проверено 29 января +2016 .
- ^ Grandy Д.К., Миллер М., Ли JX (февраль 2016). « » TAARgeting Addiction «-The Alamo Медведи Свидетель на другую революцию: Обзор Пленарного симпозиума 2015 Behavior, биологию и химия конференция» . Зависимость от наркотиков и алкоголя . 159 : 9–16. DOI : 10.1016 / j.drugalcdep.2015.11.014 . PMC 4724540 . PMID 26644139 .
TAAR1 - это рецептор с высоким сродством к МЕТ / АМФН и ДА.
- ↑ Lin Y, Hall RA, Kuhar MJ (октябрь 2011 г.). «CART-пептидная стимуляция передачи сигналов, опосредованной G-белком, в дифференцированных клетках PC12: идентификация PACAP 6–38 как антагониста рецептора CART» . Нейропептиды . 45 (5): 351–358. DOI : 10.1016 / j.npep.2011.07.006 . PMC 3170513 . PMID 21855138 .
- ^ Шиер, Дэвид; Батлер, Джеки; Льюис, Рики. Анатомия и физиология человека Хоула (четырнадцатое изд.). Нью-Йорк, штат Нью-Йорк. ISBN 978-0-07-802429-0. OCLC 881146319 .
- ^ Whishaw, Брайан Колб, Ян В. (2014). Введение в мозг и поведение (4-е изд.). Нью-Йорк, штат Нью-Йорк: Издательство Worth. ISBN 978-1429242288.
- Перейти ↑ Gross L (2006). « » Поддержка «игроков взять на себя ведущую роль в защите мозга чрезмерной стимуляции» . PLOS Biol . 4 (11): e371. DOI : 10.1371 / journal.pbio.0040371 . PMC 1609133 . PMID 20076484 .
- ^ Ян JL, Сикора P, Wilson DM, Мэтсон М.П., Бор В.А. (август 2011). «Возбуждающий нейротрансмиттер глутамат стимулирует восстановление ДНК, повышая сопротивляемость нейронов» . Мех. Aging Dev . 132 (8–9): 405–11. DOI : 10.1016 / j.mad.2011.06.005 . PMC 3367503 . PMID 21729715 .
- ^ Антагонисты рецепторов орексина - новый класс снотворных , Национальный фонд сна.
- ^ «Рецепторы ацетилхолина» . Ebi.ac.uk . Проверено 25 августа 2014 года .
- ^ Шактер, Гилберт и Вегер. Психология. Соединенные Штаты Америки, 2009. Вып.
- ^ a b Бристольский университет. «Введение в серотонин» . Проверено 15 октября 2009 года .
- ^ a b c d e Миллер GM (январь 2011 г.). «Возникающая роль следового аминосвязанного рецептора 1 в функциональной регуляции переносчиков моноаминов и дофаминергической активности» . J. Neurochem . 116 (2): 164–176. DOI : 10.1111 / j.1471-4159.2010.07109.x . PMC 3005101 . PMID 21073468 .
- ^ a b c d Eiden LE, Weihe E (январь 2011 г.). «VMAT2: динамический регулятор моноаминергической нейрональной функции мозга, взаимодействующий с наркотиками, вызывающими злоупотребление» . Анна. NY Acad. Sci . 1216 (1): 86–98. Bibcode : 2011NYASA1216 ... 86E . DOI : 10.1111 / j.1749-6632.2010.05906.x . PMC 4183197 . PMID 21272013 .
VMAT2 является везикулярным переносчиком ЦНС не только для биогенных аминов DA, NE, EPI, 5-HT и HIS, но, вероятно, также для следовых аминов TYR, PEA и тиронамина (THYR) ... [Следы аминергических] нейронов в ЦНС млекопитающих можно идентифицировать как нейроны, экспрессирующие VMAT2 для хранения, и биосинтетический фермент декарбоксилазу ароматических аминокислот (AADC).
- ^ a b c Malenka RC, Nestler EJ, Hyman SE (2009). «Глава 6: Широко распространяющиеся системы: моноамины, ацетилхолин и орексин». В Sydor A, Brown RY (ред.). Молекулярная нейрофармакология: Фонд клинической неврологии (2-е изд.). Нью-Йорк: McGraw-Hill Medical. п. 155. ISBN 9780071481274.
Различные субрегионы VTA получают глутаматергические входы от префронтальной коры, орексинергические входы от латерального гипоталамуса, холинергические, а также глутаматергические и ГАМКергические входные сигналы от латеродорсального тегментального ядра и педункулопонтинного ядра, норадренергические входы от серотонного ядра, серотонинергического ядра, серо-рапинергического ядра и ГАМКергические входы от прилежащего ядра и вентрального паллидума.
- ^ Malenka RC, Нестлер EJ, Хайман SE (2009). «Глава 6: Широко распространяющиеся системы: моноамины, ацетилхолин и орексин». В Sydor A, Brown RY (ред.). Молекулярная нейрофармакология: Фонд клинической неврологии (2-е изд.). Нью-Йорк: McGraw-Hill Medical. С. 145, 156–157. ISBN 9780071481274.
Нисходящие волокна NE модулируют афферентные болевые сигналы. ... Голубое пятно (LC), расположенное на дне четвертого желудочка в ростральном мосту, содержит более 50% всех норадренергических нейронов головного мозга; он иннервирует как передний мозг (например, он обеспечивает практически весь НЭ коре головного мозга), так и области ствола и спинного мозга. ... Другие норадренергические нейроны в головном мозге встречаются в рыхлых скоплениях клеток в стволе мозга, включая латеральные тегментальные области. Эти нейроны в основном проецируются в ствол мозга и спинной мозг. NE, наряду с 5HT, ACh, гистамином и орексином, является важным регулятором цикла сна-бодрствования и уровней возбуждения. ... Стрельба из LC также может усилить беспокойство ...Стимуляция β-адренорецепторов в миндалевидном теле приводит к усилению памяти на стимулы, закодированные под сильными отрицательными эмоциями ... Адреналин встречается только в небольшом количестве центральных нейронов, все они расположены в мозговом веществе. Адреналин участвует в висцеральных функциях, таких как контроль дыхания.
- ^ а б в г Ранг, HP (2003). Фармакология . Эдинбург: Черчилль Ливингстон. стр. 474 для норадреналиновой системы, стр. 476 для дофаминовой системы, стр. 480 для серотониновой системы и стр. 483 для холинергической системы. ISBN 978-0-443-07145-4.
- ^ Б с д е Iwańczuk W, Guźniczak P (2015). «Нейрофизиологические основы феноменов сна, возбуждения, осознания и сознания. Часть 1» . Anaesthesiol Intensive Ther . 47 (2): 162–167. DOI : 10,5603 / AIT.2015.0015 . PMID 25940332 .
Восходящая ретикулярная активирующая система (ARAS) отвечает за устойчивое состояние бодрствования. ... В таламической проекции преобладают холинергические нейроны, происходящие из педункулопонтинного тегментального ядра моста и среднего мозга (PPT) и латеродорсального тегментального ядра моста и ядер среднего мозга (LDT) [17, 18]. Гипоталамическая проекция включает норадренергические нейроны голубого пятна (LC) и серотонинергические нейроны дорсального и срединного ядер шва (DR), которые проходят через латеральный гипоталамус и достигают аксонов гистаминергического туберомамиллярного ядра (TMN), вместе формируя путь, идущий в передний мозг, кору и гиппокамп. Кортикальное возбуждение также использует дофаминергические нейроны черной субстанции (SN), вентральной области тегментов (VTA) и периакведуктальной серой зоны (PAG).Меньшее количество холинергических нейронов моста и среднего мозга посылает проекции в передний мозг по вентральному пути, минуя таламус [19, 20].
- ^ a b c d e Malenka RC, Nestler EJ, Hyman SE (2009). «Глава 12: Сон и возбуждение». В Sydor A, Brown RY (ред.). Молекулярная нейрофармакология: Фонд клинической неврологии (2-е изд.). Нью-Йорк, США: McGraw-Hill Medical. п. 295. ISBN 9780071481274.
ARAS представляет собой сложную структуру, состоящую из нескольких различных цепей, включая четыре моноаминергических пути ... Путь норэпинефрина происходит от голубого пятна (LC) и связанных ядер ствола мозга; серотонинергические нейроны также происходят из ядер шва в стволе мозга; дофаминергические нейроны берут начало в вентральной тегментальной области (VTA); а гистаминергический путь происходит от нейронов туберомаммиллярного ядра (TMN) заднего гипоталамуса. Как обсуждалось в главе 6, эти нейроны широко распространяются по всему мозгу из ограниченных скоплений клеточных тел. Норэпинефрин, серотонин, дофамин и гистамин обладают сложными модулирующими функциями и в целом способствуют бодрствованию. PT в стволе головного мозга также является важным компонентом ARAS.Активность холинергических нейронов PT (REM-on-клетки) способствует быстрому сну. Во время бодрствования клетки REM-on ингибируются подмножеством ARAS норэпинефрина и серотониновых нейронов, называемых REM-клетками.
- ^ Rinaman L (февраль 2011). «Норадренергические нейроны A2 заднего мозга: различные роли в вегетативных, эндокринных, когнитивных и поведенческих функциях» . Американский журнал физиологии. Регуляторная, интегративная и сравнительная физиология . 300 (2): Р222-35. DOI : 10,1152 / ajpregu.00556.2010 . PMC 3043801 . PMID 20962208 .
- ^ Malenka RC, Нестлер EJ, Хайман SE (2009). «Глава 6: Широко распространяющиеся системы: моноамины, ацетилхолин и орексин». В Sydor A, Brown RY (ред.). Молекулярная нейрофармакология: Фонд клинической неврологии (2-е изд.). Нью-Йорк: McGraw-Hill Medical. С. 147–148, 154–157. ISBN 9780071481274.
Нейроны из SNc плотно иннервируют дорсальное полосатое тело, где они играют критическую роль в обучении и выполнении моторных программ. Нейроны из VTA иннервируют вентральное полосатое тело (прилежащее ядро), обонятельную луковицу, миндалевидное тело, гиппокамп, орбитальную и медиальную префронтальную кору и поясную извилину. Нейроны VTA DA играют решающую роль в мотивации, поведении, связанном с вознаграждением, внимании и различных формах памяти. ... Таким образом, действуя в различных конечных областях, дофамин придает мотивационную значимость ("желание") самой награде или связанным с ней сигналам (область оболочки прилежащего ядра), обновляет значение, придаваемое различным целям в свете этого нового опыта (орбитальная префронтальная кора головного мозга), помогает консолидировать несколько форм памяти (миндалевидное тело и гиппокамп),и кодирует новые моторные программы, которые облегчат получение этой награды в будущем (ядро прилежащего ядра и спинное полосатое тело). ... DA имеет несколько действий в префронтальной коре. Он способствует «когнитивному контролю» поведения: отбору и успешному мониторингу поведения для облегчения достижения выбранных целей. Аспекты когнитивного контроля, в которых DA играет роль, включают рабочую память, способность хранить информацию «в режиме онлайн», чтобы направлять действия, подавление доминирующего поведения, которое конкурирует с целенаправленными действиями, и контроль внимания и, следовательно, способность преодолеть отвлекающие факторы. ... Норадренергические проекции от LC, таким образом, взаимодействуют с дофаминергическими проекциями от VTA, чтобы регулировать когнитивный контроль. ...DA имеет несколько действий в префронтальной коре. Он способствует «когнитивному контролю» поведения: отбору и успешному мониторингу поведения для облегчения достижения выбранных целей. Аспекты когнитивного контроля, в которых DA играет роль, включают рабочую память, способность хранить информацию «в режиме онлайн», чтобы направлять действия, подавление доминирующего поведения, которое конкурирует с целенаправленными действиями, и контроль внимания и, следовательно, способность преодолеть отвлекающие факторы. ... Норадренергические проекции от LC, таким образом, взаимодействуют с дофаминергическими проекциями от VTA, чтобы регулировать когнитивный контроль. ...DA имеет несколько действий в префронтальной коре. Он способствует «когнитивному контролю» поведения: отбору и успешному мониторингу поведения для облегчения достижения выбранных целей. Аспекты когнитивного контроля, в которых DA играет роль, включают рабочую память, способность хранить информацию «в режиме онлайн», чтобы направлять действия, подавление доминирующего поведения, которое конкурирует с целенаправленными действиями, и контроль внимания и, следовательно, способность преодолеть отвлекающие факторы. ... Норадренергические проекции от LC, таким образом, взаимодействуют с дофаминергическими проекциями от VTA, чтобы регулировать когнитивный контроль. ...Аспекты когнитивного контроля, в которых DA играет роль, включают рабочую память, способность хранить информацию «в режиме онлайн», чтобы направлять действия, подавление доминирующего поведения, которое конкурирует с целенаправленными действиями, и контроль внимания и, следовательно, способность преодолеть отвлекающие факторы. ... Норадренергические проекции от LC, таким образом, взаимодействуют с дофаминергическими проекциями от VTA, чтобы регулировать когнитивный контроль. ...Аспекты когнитивного контроля, в которых DA играет роль, включают рабочую память, способность хранить информацию «в режиме онлайн», чтобы направлять действия, подавление доминирующего поведения, которое конкурирует с целенаправленными действиями, и контроль внимания и, следовательно, способность преодолеть отвлекающие факторы. ... Норадренергические проекции от LC, таким образом, взаимодействуют с дофаминергическими проекциями от VTA, чтобы регулировать когнитивный контроль. ...Таким образом, норадренергические проекции из LC взаимодействуют с дофаминергическими проекциями из VTA, регулируя когнитивный контроль. ...Таким образом, норадренергические проекции из LC взаимодействуют с дофаминергическими проекциями из VTA, регулируя когнитивный контроль. ...
- ^ Calipari Е.С., Бэготы RC, Purushothaman я, Дэвидсон TJ, Yorgason JT, Пенья CJ, Уокер ДМ, Pirpinias СТ, Гиз КГ, Рамакришнано С, Дейссеротом К, Нестлер Е.Ю. (февраль 2016). «Визуализация in vivo идентифицирует временную сигнатуру нейронов со средними шипами D1 и D2 в кокаиновой награде» . Proc. Natl. Акад. Sci. США . 113 (10): 2726–31. Bibcode : 2016PNAS..113.2726C . DOI : 10.1073 / pnas.1521238113 . PMC 4791010 . PMID 26831103 .
Предыдущая работа продемонстрировала, что оптогенетическая стимуляция MSN D1 способствует вознаграждению, тогда как стимуляция MSN D2 вызывает отвращение.
- ^ Икемото S (2010). «Схема вознаграждения мозга за пределами мезолимбической дофаминовой системы: нейробиологическая теория» . Neurosci Biobehav Rev . 35 (2): 129–50. DOI : 10.1016 / j.neubiorev.2010.02.001 . PMC 2894302 . PMID 20149820 .
Недавние исследования внутричерепного самостоятельного введения нейрохимических веществ (лекарств) показали, что крысы учатся самостоятельно вводить различные лекарства в мезолимбические дофаминовые структуры - заднюю вентральную тегментальную область, прилежащее ядро медиальной оболочки и медиальный обонятельный бугорок. ... В 1970-х годах было признано, что обонятельный бугорок содержит стриарный компонент, который заполнен ГАМКергическими средними шиповидными нейронами, получающими глутаматергические входные сигналы от кортикальных областей и дофаминергические входные сигналы от ВТА и проецирующиеся в вентральный паллидум так же, как прилежащее ядро.
Рисунок 3: Вентральное полосатое тело и самостоятельное введение амфетамина - ^ Malenka RC, Нестлер EJ, Хайман SE (2009). «Глава 6: Широко распространяющиеся системы: моноамины, ацетилхолин и орексин». В Sydor A, Brown RY (ред.). Молекулярная нейрофармакология: Фонд клинической неврологии (2-е изд.). Нью-Йорк: McGraw-Hill Medical. С. 175–176. ISBN 9780071481274.
В головном мозге гистамин синтезируется исключительно нейронами с их клеточными телами в туберомаммиллярном ядре (TMN), которое находится внутри заднего гипоталамуса. У человека примерно 64000 гистаминергических нейронов на каждой стороне. Эти клетки распространяются по всему головному и спинному мозгу. Области, которые получают особенно плотные проекции, включают кору головного мозга, гиппокамп, неостриатум, прилежащее ядро, миндалевидное тело и гипоталамус. ... В то время как наиболее охарактеризованная функция гистаминовой системы в головном мозге - регуляция сна и возбуждения, гистамин также участвует в обучении и памяти ... Также оказывается, что гистамин участвует в регуляции питания и энергетического баланса.
- ^ Malenka RC, Нестлер EJ, Хайман SE (2009). «Глава 6: Широко распространяющиеся системы: моноамины, ацетилхолин и орексин». В Sydor A, Brown RY (ред.). Молекулярная нейрофармакология: Фонд клинической неврологии (2-е изд.). Нью-Йорк: McGraw-Hill Medical. С. 158–160. ISBN 9780071481274.
[] Дорсальный шов преимущественно иннервирует кору головного мозга, таламус, полосатое тело (хвостатое ядро и прилежащее ядро) и дофаминергические ядра среднего мозга (например, черная субстанция и вентральная тегментальная область), в то время как средний шов иннервирует гиппокамп. перегородка и другие структуры лимбического отдела переднего мозга. ... очевидно, что 5HT влияет на сон, возбуждение, внимание, обработку сенсорной информации в коре головного мозга, а также на важные аспекты эмоций (вероятно, включая агрессию) и регуляцию настроения. ... Ростральные ядра, которые включают в себя линейное ядро, дорсальный шов, медиальный шов и понтийный шов, иннервируют большую часть мозга, включая мозжечок. Хвостовые ядра, которые включают raphe magnus, raphe pallidus и raphe obscuris, имеют более ограниченные выступы, которые заканчиваются в мозжечке,ствол мозга и спинной мозг.
- ^ Нестлер, Эрик Дж. «ПУТИ ВОЗНАГРАЖДЕНИЯ МОЗГА» . Медицинская школа Икана на горе Синай . Nestler Lab . Проверено 16 августа 2014 года .
Дорсальный шов является основным местом расположения серотонинергических нейронов в головном мозге, которые, подобно норадренергическим нейронам, всесторонне модулируют функцию мозга, регулируя состояние активации и настроение организма.
- ^ Марстон OJ, Garfield AS, Heisler LK (июнь 2011). «Роль центральных систем серотонина и меланокортина в контроле энергетического баланса». Европейский журнал фармакологии . 660 (1): 70–79. DOI : 10.1016 / j.ejphar.2010.12.024 . PMID 21216242 .
- ^ Malenka RC, Нестлер EJ, Хайман SE (2009). «Глава 6: Широко распространяющиеся системы: моноамины, ацетилхолин и орексин». В Sydor A, Brown RY (ред.). Молекулярная нейрофармакология: Фонд клинической неврологии (2-е изд.). Нью-Йорк: McGraw-Hill Medical. С. 167–175. ISBN 9780071481274.
Базальные холинергические ядра переднего мозга состоят из медиального ядра перегородки (Ch1), вертикального ядра диагональной перемычки (Ch2), горизонтального отгиба диагональной перемычки (Ch3) и базального ядра Мейнерта (Ch4). Холинергические ядра ствола мозга включают педункулопонтинное ядро (Ch5), латеродорсальное тегментальное ядро (Ch6), медиальную габенулу (Ch7) и парабигеминальное ядро (Ch8).
- ^ "Разговоры нейронов: как клетки мозга общаются" . Brainfacts.org . Проверено 2 декабря 2014 .
- ^ а б Ядав В.К., Рю Дж. Х., Суда Н., Танака К. Ф., Гингрич Дж. А., Шютц Дж., Глориё Ф. Х., Чианг С. Ю., Зажак Дж. Д., Инсогна К. Л., Манн Дж. Дж., Хен Р., Дуси П., Карсенти Дж. (ноябрь 2008 г.). «Lrp5 контролирует образование костей, подавляя синтез серотонина в двенадцатиперстной кишке» . Cell . 135 (5): 825–37. DOI : 10.1016 / j.cell.2008.09.059 . PMC 2614332 . PMID 19041748 .
- Перейти ↑ Carlson, NR, & Birkett, MA (2017). Физиология поведения (12-е изд.). Пирсон, стр. 100–115. ISBN 978-0134080918
- ^ "Центр контроля заболеваний Стрихнин | Факты о Стрихнине | Готовность к чрезвычайным ситуациям и реагирование на них" . Emergency.cdc.gov . Проверено 7 мая 2018 .
- ^ a b c «Таблица нейротрансмиттеров и лекарств» . Ocw.mit.edu . Проверено 25 августа 2014 года .
- ^ «Агонист - определение и многое другое из бесплатного словаря Merriam-Webster» . Merriam-webster.com . Проверено 25 августа 2014 года .
- ^ Атак Дж., Лаврейсен Х. (2010) Агонист. В: Столерман И.П. (ред.) Энциклопедия психофармакологии. Шпрингер, Берлин, Гейдельберг. https://doi.org/10.1007/978-3-540-68706-1_1565
- ↑ Рот, Брайан Л. (17 февраля 2016 г.). «СТРАДЫ ДЛЯ Нейробиологов» . Нейрон . 89 (4): 683–694. DOI : 10.1016 / j.neuron.2016.01.040 . PMC 4759656 . PMID 26889809 .
- ^ а б Ричард К. Райс; Дэвид А. Фьеллин; Шеннон С. Миллер (2009). Принципы наркологической медицины (4-е изд.). Филадельфия: Уолтерс Клувер / Липпинкотт Уильямс и Уилкинс. С. 709–710. ISBN 9780781774772. Проверено 16 августа 2015 года .
- ^ a b c Флорес А., Мальдонадо Р., Беррендеро Ф (2013). «Перекрестный разговор между каннабиноидом и гипокретином в центральной нервной системе: что мы знаем до сих пор» . Front Neurosci . 7 : 256. DOI : 10,3389 / fnins.2013.00256 . PMC 3868890 . PMID 24391536 .
• Рисунок 1. Схема экспрессии CB1 мозга и орексинергических нейронов, экспрессирующих OX1 или OX2.
• Рисунок 2. Синаптические механизмы передачи сигналов в каннабиноидной и орексиновой системах. - ^ "Антагонист" . Медицинское определение антагониста . Проверено 5 ноября 2014 года .
- ^ Goeders, Ник E. (2001). «Антагонист» . Энциклопедия наркотиков, алкоголя и привыкания . Проверено 2 декабря 2014 .
- ^ Broadley KJ (март 2010). «Сосудистые эффекты следовых аминов и амфетаминов». Фармакология и терапия . 125 (3): 363–375. DOI : 10.1016 / j.pharmthera.2009.11.005 . PMID 19948186 .
- ^ Lindemann L, Hoener MC (май 2005). «Возрождение следовых аминов, вдохновленное новым семейством GPCR». Направления фармакологических наук . 26 (5): 274–281. DOI : 10.1016 / j.tips.2005.03.007 . PMID 15860375 .
- Перейти ↑ Wang X, Li J, Dong G, Yue J (февраль 2014 г.). «Эндогенные субстраты мозга CYP2D». Европейский журнал фармакологии . 724 : 211–218. DOI : 10.1016 / j.ejphar.2013.12.025 . PMID 24374199 .
- ^ a b c d e Мейерс, Стивен (2000). «Использование предшественников нейротрансмиттеров для лечения депрессии» (PDF) . Обзор альтернативной медицины . 5 (1): 64–71. PMID 10696120 . Архивировано 5 августа 2004 года из оригинального (PDF) .
- ^ Ван Praag, HM (1981). «Управление депрессией с помощью предшественников серотонина». Биол Психиатрия . 16 (3): 291–310. PMID 6164407 .
- ↑ Хили, Дэвид (21 апреля 2015 г.). «Серотонин и депрессия» . BMJ . 350 : h1771. DOI : 10.1136 / bmj.h1771 . ISSN 1756-1833 . PMID 25900074 . S2CID 38726584 .
- ^ «Основы мозга NIMH» . Национальные институты здоровья США . Проверено 29 октября 2014 года .
- ^ Bittigau, P .; Икономиду, К. (ноябрь 1997 г.). «Глутамат при неврологических заболеваниях». Журнал детской неврологии . 12 (8): 471–485. DOI : 10.1177 / 088307389701200802 . ISSN 0883-0738 . PMID 9430311 . S2CID 1258390 .
- ^ Неттер, П. (1991) Биохимические переменные в изучении темперамента. В Strelau, J. & Angleitner, A. (Eds.), Исследования темперамента: Международные перспективы теории и измерения 147–161. Нью-Йорк: Пленум Пресс.
- ^ Трофимова I, Роббинс TW (2016). «Темперамент и системы возбуждения: новый синтез дифференциальной психологии и функциональной нейрохимии» . Неврология и биоповеденческие обзоры . 64 : 382–402. DOI : 10.1016 / j.neubiorev.2016.03.008 . PMID 26969100 . S2CID 13937324 .
- ^ Cloninger CR, Svrakic DM, Przybeck TR. Психобиологическая модель темперамента и характера » Arch Gen Psychiatry 1993; 50: 975-990.
- ^ Трофимова, IN (2016). «Взаимосвязь между функциональными аспектами деятельности и нейрохимической моделью темперамента взрослого человека». В: Арнольд М.С. (ред.) Темпераменты: индивидуальные различия, социальные и экологические влияния и влияние на качество жизни. Нью-Йорк: Nova Science Publishers, Inc .: 77–147.
- ^ Depue Р.А., Morrone-Strupinsky СП (2005). «Нейроповеденческая модель партнерской связи: последствия для концептуализации человеческой черты принадлежности». Поведенческие науки и науки о мозге . 28 (3): 313–350. DOI : 10.1017 / s0140525x05000063 . PMID 16209725 .
- ^ Лео, J., & Lacasse, J. (10 октября 2007). СМИ и теория химического дисбаланса депрессии. Получено 1 декабря 2014 г. с сайта http://psychrights.org/articles/TheMediaandChemicalImbalanceTheoryofDepression.pdf.
- ^ Добряков, Екатерина; Genova, Helen M .; ДеЛука, Джон; Уайли, Гленн Р. (12 марта 2015 г.). "Гипотеза дисбаланса дофамина усталости при рассеянном склерозе и других неврологических расстройствах" . Границы неврологии . 6 : 52. DOI : 10,3389 / fneur.2015.00052 . PMC 4357260 . PMID 25814977 .
- ^ "Общая, органическая и биологическая химия структур жизни" Карен К. Тимберлейк с.661
Внешние ссылки [ править ]
| Викискладе есть медиафайлы по теме нейротрансмиттера . |
| В Викиучебнике есть книга по темам: Нейробиология / Клеточная нейробиология / Нейротрансмиттеры. |
- Молекулярная клеточная биология. 4-е издание. Раздел 21.4: Нейротрансмиттеры, синапсы и передача импульсов
- Фотогалерея молекулярных выражений: Коллекция нейротрансмиттеров
- Нейротрансмиттеры головного мозга
- Эндогенные нейроактивные внеклеточные преобразователи сигналов
- Нейротрансмиттер в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)
- сайт нейробиологии для детей
- сайт исследователя мозга