12О6-
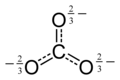
12, один из оксоуглеродных анионов. Черные кружки - атомы углерода, красные кружки - атомы кислорода. Каждый синий ореол представляет половину отрицательного заряда.
В химии оксоуглеродный анион - это отрицательный ион, состоящий исключительно из атомов углерода и кислорода и, следовательно, имеющий общую формулу C
ИксОп -
удля некоторых целых чисел x , y и n .
Наиболее распространенными оксоуглеродными анионами являются карбонатные , CO2-
3, и оксалат , C
2О2-
4. Однако существует большое количество стабильных анионов этого класса, в том числе несколько из них, которые используются в исследованиях или в промышленности. Также есть много нестабильных анионов, таких как CO-
2и CO-
4, которые мимолетно существуют во время некоторых химических реакций; и многие гипотетические виды, такие как CO4-
4, которые были предметом теоретических исследований, но пока не наблюдались.
Стабильные оксоуглеродные анионы образуют соли с большим разнообразием катионов . Нестабильные анионы могут сохраняться в очень разреженном газообразном состоянии, например, в межзвездных облаках . Большинство оксоуглеродных анионов имеют соответствующие фрагменты в органической химии , соединениями которых обычно являются сложные эфиры . Так, например, оксалатный фрагмент [–O– (C = O) 2 –O–] находится в сложном эфире диметилоксалата H 3 C – O– (C = O) 2 –O – CH 3 .
Электронная структура карбонат-иона [ править ]
Карбонат-ион имеет плоскую тригональную структуру, точечная группа D 3h . Три связи CO имеют одинаковую длину 136 пм, а 3 угла ОСО равны 120 °. Атом углерода имеет 4 пары валентных электронов, что показывает, что молекула подчиняется правилу октетов . Это один из факторов, который способствует высокой стабильности иона, которая встречается в таких породах, как известняк . Электронная структура описывается двумя основными теориями, которые используются, чтобы показать, как 4 пары электронов распределены в молекуле, которая имеет только 3 связи CO.
Согласно теории валентной связи электронная структура карбонат-иона представляет собой резонансный гибрид трех канонических форм.
В каждой канонической форме есть две одинарные связи и одна двойная связь. Три канонические формы вносят равный вклад в резонансный гибрид, поэтому три связи CO имеют одинаковую длину.
В теории молекулярных орбиталей ось 3-го порядка обозначается как ось z молекулы. Три σ-связи образуются перекрытием s, p x и p y орбиталей на атоме углерода с p- орбиталью на каждом атоме кислорода. Кроме того, делокализованная π-связь образуется в результате перекрытия орбитали p z на атоме углерода с орбиталью p z на каждом атоме кислорода, которая перпендикулярна плоскости молекулы.
Обратите внимание, что те же схемы связывания могут применяться для нитрат-иона NO 3 - , который изоэлектронен карбонат-иону.
Точно так же двукратно симметричная структура карбоксилатной группы CO-
2, может быть описан как резонансный гибрид двух канонических форм в теории валентных связей или с 2 связями σ и делокализованной связью π в теории молекулярных орбиталей.
Родственные соединения [ править ]
Оксокарбоновые кислоты [ править ]
Оксоуглеродный анион C
ИксОп -
уможно рассматривать как результат удаления всех протонов из соответствующей кислоты C x H n O y . Карбонат CO2-
3, например, можно рассматривать как анион угольной кислоты H 2 CO 3 . Иногда «кислота» на самом деле представляет собой спирт или другой вид; это случай, например, ацетилендиолата C
2О2-
2что даст ацетилендиол C 2 H 2 O 2 . Однако анион часто более стабилен, чем кислота (как в случае карбоната); [1], а иногда кислота неизвестна или ожидается, что она крайне нестабильна (как в случае метантетракарбоксилата C (COO - ) 4 ).
Нейтрализованные виды [ править ]
Каждый оксоуглеродный анион C
ИксОп -
ув принципе может быть сопоставлен с электрически нейтральным (или окисленным ) вариантом C x O y , оксоуглеродом ( оксидом углерода) с тем же составом и структурой, за исключением отрицательного заряда. Однако, как правило, эти нейтральные оксоуглероды менее стабильны, чем соответствующие анионы. Так, например, стабильный карбонатный анион соответствует крайне нестабильному нейтральному триоксиду углерода CO 3 ; [2] оксалат C
2О2-
4соответствуют еще менее стабильному 1,2-диоксетандиону C 2 O 4 ; [3] и стабильный кроконат- анион C
5О2-
5соответствует нейтральному циклопентанепентону C 5 O 5 , который обнаружен только в следовых количествах. [4]
Уменьшенные варианты [ править ]
И наоборот, некоторые оксоуглеродные анионы могут быть восстановлены с образованием других анионов с той же структурной формулой, но с большим отрицательным зарядом. Таким образом, родизонат C
6О2-
6может быть восстановлен до аниона тетрагидроксибензохинона (THBQ) C
6О4-
6а затем к бензолгексолату C
6О6-
6. [5]
Кислотные ангидриды [ править ]
Оксоуглеродный анион C
ИксОп -
утакже может быть связан с ангидридом соответствующей кислоты. Последний был бы еще одна с формулой оксидов углерода C х O у - п / 2 ; а именно, кислота минус п / 2 молекулы воды Н 2 O. Стандартный пример является связь между карбонатом CO2-
3и диоксид углерода CO 2 . Соответствие не всегда четко определено, поскольку может существовать несколько способов выполнения этой формальной дегидратации, включая соединение двух или более анионов с образованием олигомера или полимера . В отличие от нейтрализации, эта формальная дегидратация иногда дает довольно стабильные оксоуглероды, такие как меллитный ангидрид C 12 O 9 из меллитата C
12О6-
12через меллитовую кислоту C 12 H 6 O 12 [6] [7] [8]
Гидрогенизированные анионы [ править ]
Для каждого оксоуглеродного аниона C
ИксОп -
ув принципе существует n −1 частично гидрированных анионов с формулами H
kC
ИксО( п - к ) -
у, где k изменяется от 1 до n −1. Эти анионы обычно обозначаются приставками «водород» -, «дигидроген» -, «триводород» - и т. Д. Некоторые из них, однако, имеют специальные названия: гидрокарбонат HCO.-
3обычно называют бикарбонатом , а гидрогеноксалат HC
2О-
4известен как биноксалат .
Гидрированные анионы могут быть стабильными, даже если полностью протонированная кислота не является стабильной (как в случае бикарбоната).
Список оксоуглеродных анионов [ править ]
Вот неполный список известных или предполагаемых анионов оксоуглерода.
| Диаграмма | Формула | Имя | Кислота | Ангидрид | Нейтрализовано |
|---|---|---|---|---|---|
| : CO2- 2 | карбонит | HCO 2 H | CO | CO 2 | |
| CO2- 3 | карбонат | СН 2 О 3 | CO 2 | CO 3 | |
| CO2- 4 | пероксокарбонат | CO 3 | CO 4 | ||
| CO4- 4 | ортокарбонат | C (OH) 4 метантетрол | CO 2 | CO 4 | |
| C 2О2- 2 | ацетилендиолат | C 2 H 2 O 2 ацетилендиол | С 2 О 2 | ||
| C 2О2- 4 | оксалат | С 2 Н 2 О 4 | С 2 О 3 , С 4 О 6 | С 2 О 4 | |
| C 2О2- 5 | дикарбонат | С 2 Н 2 О 5 | С 2 О 4 | ||
| C 2О2- 6 | пероксодикарбонат | ||||
| C 3О2- 3 | дельтат | С 3 О (ОН) 2 | С 3 О 3 | ||
| C 3О2- 5 | мезоксалат | С 3 Н 2 О 5 | |||
| C 4О2- 4 | ацетилендикарбоксилат | С 4 Н 2 О 4 | |||
| C 4О2- 4 | скварат | С 4 О 2 (ОН) 2 | С 4 О 4 | ||
| C 4О2- 6 | диоксосукцинат | С 4 Н 2 О 6 | |||
| C 5О2- 5 | кроконат | С 5 О 3 (ОН) 2 | С 5 О 5 | ||
| C 5О4- 8 | метантетракарбоксилат | С 5 Н 4 О 8 | |||
| C 6О2- 6 | родизонат | С 4 О 4 (COH) 2 | С 6 О 6 | ||
| C 6О4- 6 | бензохинонетраолат; THBQ анион | (CO) 2 (COH) 4 THBQ | С 6 О 6 | ||
| C 6О6- 6 | бензолгексолат | C 6 (OH) 6 бензолгексол | С 6 О 6 | ||
| C 6О4- 8 | этилентетракарбоксилат | С 6 Н 4 О 8 | С 6 О 6 | ||
| C 8О4- 9 | фурантетракарбоксилат | С 8 Н 4 О 9 | |||
| C 10О4- 10 | бензохинонтетракарбоксилат | C10ЧАС4О10 | C10О8 | ||
| C 12О6- 12 | мелодировать | С 6 (COOH) 6 | С 12 О 9 |
Некоторые другие оксоуглеродные анионы были обнаружены в следовых количествах, например, C
6О-
6, однократно ионизированная версия родизоната. [9]
См. Также [ править ]
- Оксокарбон
- Силикат
- Перкарбонат натрия (на самом деле пергидрат карбоната )
Ссылки [ править ]
- ^ «Инфракрасные и масс-спектральные исследования льда H 2 O + CO 2, облученного протонами : свидетельство наличия угольной кислоты» , Мур, MH; Ханна, РК
- ^ DeMore WB; Якобсен CW (1969). «Образование триоксида углерода при фотолизе озона в жидком диоксиде углерода». Журнал физической химии . 73 (9): 2935–2938. DOI : 10.1021 / j100843a026 .
- ^ Герман Ф. Кордес; Герберт П. Рихтер; Карл А. Хеллер (1969). «Масс-спектрометрические доказательства существования 1,2-диоксетандиона (димер диоксида углерода). Хемилюминесцентный промежуточный продукт». Варенье. Chem. Soc . 91 (25): 7209. DOI : 10.1021 / ja01053a065 .
- ^ Шредер, Детлеф; Шварц, Гельмут; Дуа, Суреш; Бланксби, Стивен Дж .; Боуи, Джон Х. (май 1999 г.). «Масс-спектрометрические исследования оксоуглеродов C n O n ( n = 3–6)». Международный журнал масс-спектрометрии . 188 (1-2): 17-25. Bibcode : 1999IJMSp.188 ... 17S . DOI : 10.1016 / S1387-3806 (98) 14208-2 .
- ^ Хайян Чен, Мишель Арман, Матье Курти, Мэн Цзян, Клэр П. Грей, Франк Долхем, Жан-Мари Тараскон и Филипп Пуазо (2009), «Литиевая соль тетрагидроксибензохинона: к разработке устойчивой литий-ионной батареи» Варенье. Chem. Soc. , 131 (25), стр 8984-8988. DOI : 10.1021 / ja9024897
- ↑ J. Liebig, F. Wöhler (1830), "Ueber die Zusammensetzung der Honigsteinsäure" Poggendorfs Annalen der Physik und Chemie , vol. 94, Issue 2, pp.161–164. Онлайн-версия, по состоянию на 08.07.2009.
- ^ Мейер H, Штайнер K (1913). «Über ein neues Kohlenoxyd C 12 O 9 (новый оксид углерода C 12 O 9 )» . Berichte der Deutschen Chemischen Gesellschaft . 46 : 813–815. DOI : 10.1002 / cber.191304601105 .
- ^ Ганс Мейер; Карл Штайнер (1913). "Über ein neues Kohlenoxyd C 12 O 9 " . Berichte der Deutschen Chemischen Gesellschaft . 46 : 813–815. DOI : 10.1002 / cber.191304601105 .
- ^ Ричард Б. Wyrwas и Кэролайн Chick Джарролд (2006), «Производство C
6О-
6из олигомеризации CO на анионах молибдена ». J. Am. Chem. Soc., том 128, выпуск 42, страницы 13688–13689. doi : 10.1021 / ja0643927