| |||
| Имена | |||
|---|---|---|---|
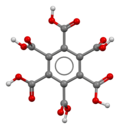
| Название ИЮПАК Бензол-1,2,3,4,5,6-гексакарбоновая кислота | |||
| Другие имена Графитовая кислота Бензолгексакарбоновая кислота | |||
| Идентификаторы | |||
3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.007.495 | ||
PubChem CID | |||
| UNII | |||
Панель управления CompTox ( EPA ) | |||
| |||
| |||
| Характеристики | |||
| С 12 Н 6 О 12 | |||
| Молярная масса | 342,16 г / моль | ||
| Плотность | 1,68 г / см 3 , 2,078 (вычислено) [2] | ||
| Температура плавления | > 300 ° С (572 ° F, 573 К) | ||
| Точка кипения | 678 ° C (1252 ° F, 951 K) (расчет) [2] | ||
| Кислотность (p K a ) | 1,40, 2,19, 3,31, 4,78, 5,89, 6,96 [3] | ||
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Меллитовая кислота , также называемая графитовой кислотой или бензолгексакарбоновой кислотой , - это кислота, впервые обнаруженная в 1799 году Мартином Генрихом Клапротом в минерале меллите (медовый камень), который представляет собой соль алюминия кислоты. [4] Он кристаллизуется в тонких шелковистых иголках и растворяется в воде и спирте .
Подготовка [ править ]
Меллитовая кислота может быть получена нагреванием меллита с карбонатом аммония , выпариванием избытка соли аммония и добавлением аммиака к раствору. Осажденный оксид алюминия отфильтровывают, то фильтрат упаривают , и соль аммония кислоты очищают с помощью перекристаллизации . Затем соль аммония превращается в соль свинца путем осаждения ацетатом свинца , а соль свинца затем разлагается сероводородом . Кислота также может быть получена окислением чистого углерода , графита илигексаметилбензол , щелочным перманганатом калия на холоде или горячей концентрированной азотной кислотой . [5]
Реакции [ править ]
Это очень стабильное соединение; хлор , концентрированная азотная кислота и йодоводородная кислота с ним не реагируют. При сухой перегонке он разлагается на диоксид углерода и пиромеллитовую кислоту C 10 H 6 O 8 ; при перегонке с известью дает диоксид углерода и бензол. Длительное переваривание кислоты с избытком пентахлорида фосфора приводит к образованию хлорангидрида, который кристаллизуется в иглах и плавится при 190 ° C. При нагревании аммониевой соли кислоты до 150–160 ° C при выделении аммиака смесь парамида (меллимид, молекулярная формула C
6(CONHCO)
3), и получают эухроат аммония . Смесь может быть разделена растворением эухроата аммония водой. Парамид - белый аморфный порошок, не растворимый в воде и спирте.
Высокая стабильность солей меллитовой кислоты и их присутствие в качестве конечного продукта окисления полициклических ароматических углеводородов , присутствующих в Солнечной системе, делают их возможным органическим веществом в марсианской почве . [6]
Меллитаты (и соли других бензолполикарбоновых кислот ) железа и кобальта обладают интересными магнитными свойствами. [7]
См. Также [ править ]
- Меллитовый ангидрид
Ссылки [ править ]
- ^ MSDS для меллитовой кислоты [ постоянная мертвая ссылка ]
- ^ a b Данные куратора: Прогнозируемые свойства: 2244 . ChemSpider.com.
- ^ Brown, HC, et al., В Baude, EA и Nachod, FC, Определение органических структур физическими методами , Academic Press, Нью-Йорк, 1955.
- ^ Beiträge цур Chemischen Kenntniss дер Mineralkörper, Группа 3 (на немецком языке ). п. 114.
- ^ WebElements.com
- ^ С. А. Беннер; KG Devine; Л.Н. Матвеева; Д.Х. Пауэлл (2000). «Пропавшие органические молекулы на Марсе» . Труды Национальной академии наук . 97 (6): 2425–2430. DOI : 10.1073 / pnas.040539497 . PMC 15945 . PMID 10706606 .
- ^ Kurmoo МЫ, Estournes С, Окой Y, Кумагайте Н, Иноуэ К (2005) неорганической химии Объем 44, стр 217
Дальнейшее чтение [ править ]
Генри Энфилд Роско, Карл Шолеммер, «Mellitene Group», « Трактат по химии : V.III: Химия углеводородов и их производных по органической химии: PV : 529. Д. Эпплтон и Ко» (1889).
![]() Эта статья включает текст из публикации, которая сейчас находится в общественном достоянии : Chisholm, Hugh, ed. (1911). « Меллитовая кислота ». Британская энциклопедия . 18 (11-е изд.). Издательство Кембриджского университета. п. 95.
Эта статья включает текст из публикации, которая сейчас находится в общественном достоянии : Chisholm, Hugh, ed. (1911). « Меллитовая кислота ». Британская энциклопедия . 18 (11-е изд.). Издательство Кембриджского университета. п. 95.